Clear Sky Science · de
PEO-ummantelte Flüssigkeitsstrahlen erhöhen die Stabilität der Probenzufuhr für serielle femtosekunden-Röntgenkristallographie
Scharfere Filme von Molekülen
Zu verstehen, wie die Maschinerie des Lebens arbeitet, bedeutet oft, Proteine in Aktion mit Röntgen‑„Kameras“ zu filmen, die Millionen von Bildern pro Sekunde aufnehmen. Um jedoch diese Filme auf atomarer Skala zu erstellen, müssen Wissenschaftler einen stetigen Strom winziger Kristalle in den Strahl bringen, ohne kostbare Proben zu verschwenden oder empfindliche Hardware zu verstopfen. Diese Arbeit zeigt, dass das Einhüllen schneller Flüssigkeitsstrahlen in eine dünne Schicht eines gebräuchlichen Polymers, Polyethylenoxid (PEO), diese Ströme deutlich stabiler macht und so neue Einblicke in die ultrakurzen Bewegungen komplexer Proteine eröffnet.
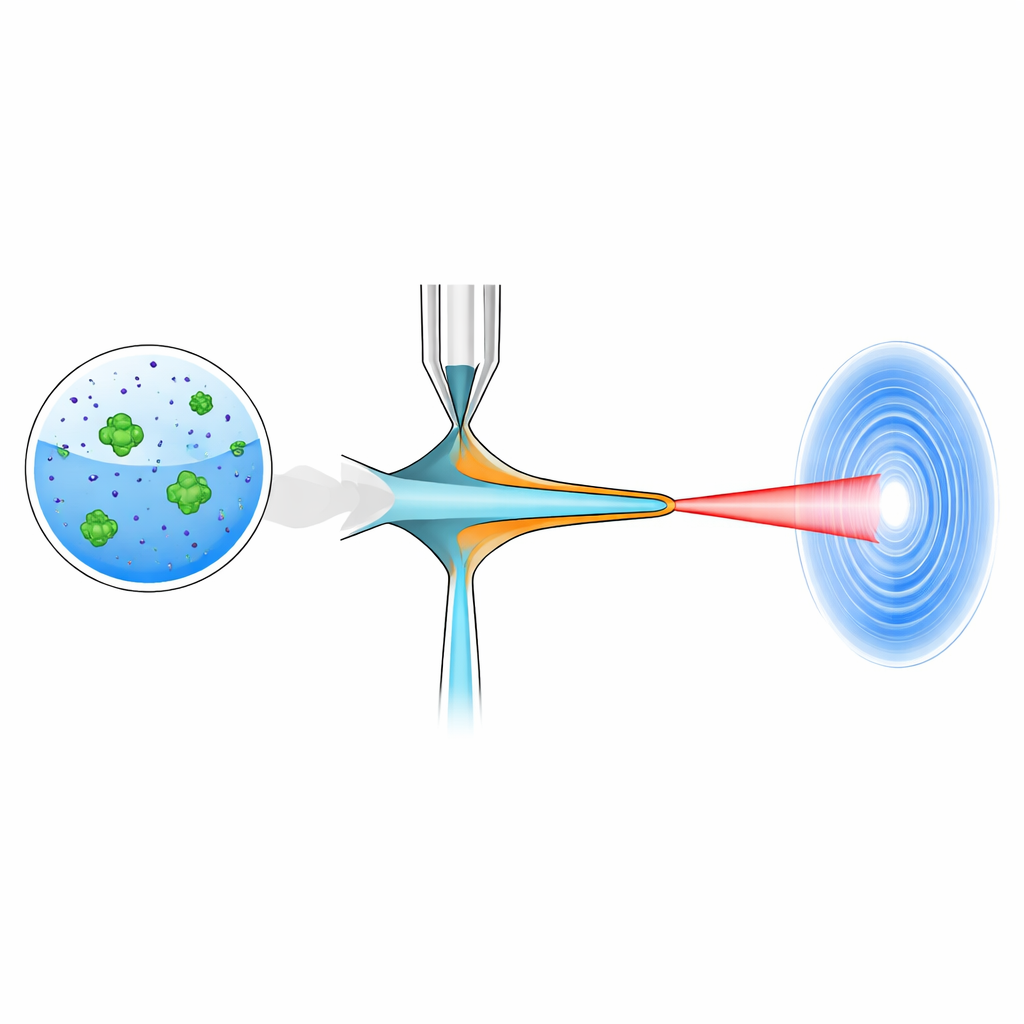
Warum winzige Strahlen wichtig sind
Moderne Röntgen-Freie-Elektronen-Laser liefern unglaublich helle Lichtblitze, die nur einige Dutzend Femtosekunden dauern — kurz genug, dass ein Proteinkristall Beugung erzeugt, bevor er zerstört wird. In der seriellen femtosekunden-Kristallographie treffen Millionen solcher Blitze jeweils auf ein frisches Mikrokristall, das in einem haarfeinen Flüssigkeitsstrahl durch den Strahl transportiert wird. Je öfter ein Röntgenpuls tatsächlich einen Kristall trifft (die „Hit‑Rate“) und je mehr dieser Treffer in Strukturen interpretiert werden können (die „Indexierungsrate“), desto schneller können Wissenschaftler vollständige 3D-Bilder aufbauen. Der Strahl muss dabei dünn, schnell und ausgesprochen stabil sein — besonders bei Megahertz-Wiederholraten, bei denen die Pulse weniger als eine Mikrosekunde auseinanderliegen.
Grenzen heutiger Flüssigkeitsströme
Standardinjektoren pressen einen einzelnen Flüssigkeitsstrom mit einer umgebenden Gasphase (gasdynamische virtuelle Düsen) oder fügen eine zweite Flüssigkeitsschicht als stabilisierende Ummantelung hinzu (Doppelfluss-Fokusdüsen). Diese Ansätze funktionieren gut für wässrige Proben, doch viele der interessantesten Membranproteine wachsen nur als Kristalle in zähen, sirupartigen Lösungen reich an Polyethylenglykol (PEG). Solche viskosen Gemische lassen sich nur schwer zu einem feinen Strahl ziehen, was zu Wackeln, Zerfall und einem höheren Verstopfungsrisiko führt. Versuche, sie mit einer Ethanol‑Ummantelung zu stabilisieren, verlängern zwar oft den Strahl, zwingen die Forschenden jedoch häufig, die Probenflussrate zu reduzieren — wodurch die Trefferquote sinkt und die Datensammlung länger dauert.
Eine Polymerhülle für superstabile Ströme
Die Autorinnen und Autoren testeten eine andere Strategie: die Umhüllung der kristallführenden Flüssigkeit mit einer verdünnten PEO‑Lösung statt mit Ethanol. Unter den extremen Dehnkräften in der Nähe der Düsenspitze strecken sich die langen PEO‑Ketten und bilden eine viskoelastische Schale um den Kernstrom. Diese Hülle macht den Strahl deutlich dünner und mehr als viermal länger als vergleichbare Wasser‑ oder Ethanol‑ummantelte Strahlen, während gleichzeitig sehr geringe Hintergrundstreuung erhalten bleibt — essenziell für klare Beugungsbilder. Lange Strahlen, die mitunter über einen Millimeter hinausgehen, ermöglichen Pump‑Probe‑Experimente mit Zeitverzögerungen von einigen zehn Mikrosekunden und schließen damit eine Lücke zwischen den schnellsten XFEL‑Studien und langsameren Synchrotronmessungen.
Tests an realen Proteinen
Um zu prüfen, ob das mit biologischen Zielmolekülen funktioniert, lieferten die Forschenden Mikrokristalle einer kleinen Modell‑Enzymverbindung (Lysozym) und des Photosystems II, eines großen Membrankomplexes der Photosynthese. Für Lysozym in sowohl nieder‑ als auch mittelviskosen Pufferlösungen hielten PEO‑ummantelte Strahlen gute Hit‑ und Indexierungsraten bei deutlich reduzierter Probenflussrate aufrecht, sodass vollständige Datensätze weiterhin in nur wenigen Minuten gesammelt werden konnten. Für Photosystem II in besonders dickem, PEG‑reichen Puffer — Bedingungen, die dafür bekannt sind, schwierig zu zerstäuben — erzeugte die PEO‑Schale lange, gerade Strahlen und lieferte die bislang besten Flüssigkeitsstrahl‑Daten am European XFEL, obwohl die Trefferquote moderat blieb. Simulationen der Kristallwahrscheinlichkeiten im Strahl bestätigten, dass bei passend abgestimmter Röntgenstrahlgröße und Kristallgröße Trefferquoten von 3–5 % routinemäßig erreichbar sein sollten.

Reaktionen unterwegs mischen
Aufbauend auf diesem Erfolg entwarfen die Forschenden eine neue „Dreifluss“-Düse, die Mikromischen und PEO‑Ummantelung in einem einzigen 3D‑gedruckten Bauteil kombiniert. Zwei innere Kanäle bringen eine Proteinsuspension und eine Reaktantenlösung zusammen, sodass Moleküle beginnen können, während sie über einige zehn Millisekunden in einem schmalen Mischkanal ineinander diffundieren, zu reagieren. Ein dritter Kanal fügt dann die PEO‑Lösung hinzu, und Gasströmung fokussiert alles zu einem einzigen viskoelastischen Strahl. Dieser kompakte Injektor ist für „Mix‑and‑Inject“-Experimente ausgelegt, bei denen Forschende verfolgen, wie Enzyme oder andere Proteine nach Bindung eines Substrats oder einer Redoxreaktion ihre Form ändern.
Klarere, schnellere Einblicke in das Leben in Bewegung
Einfach ausgedrückt zeigt die Studie, dass eine flexible Polymerhülle Flüssigkeitsstrahlen unter den rauen Bedingungen schneller Röntgenexperimente deutlich stabiler macht. Die gestreckten PEO‑Ketten wirken wie mikroskopische Stoßdämpfer und halten den Strahl lange genug zusammen, damit viele Pulse frische Kristalle untersuchen können — selbst in klebrigen, PEG‑reichen Lösungen, die zuvor Probleme verursachten. Dadurch können Forschende realistischere Probenbedingungen verwenden, ein breiteres Spektrum an Zeitverzögerungen erkunden und hochwertigere Strukturdatensätze effizienter sammeln. Diese verbesserte Kontrolle winziger Flüssigkeitsströme bringt uns näher daran, routinemäßig die schnellsten Schritte der Photosynthese, der Enzymkatalyse und anderer grundlegender biologischer Prozesse mit bisher unerreichter Detailtiefe zu filmen.
Zitation: Vakili, M., Bajt, S., Bielecki, J. et al. PEO-sheathed liquid jets increase sample delivery stability for serial femtosecond X-ray crystallography. Sci Rep 16, 10497 (2026). https://doi.org/10.1038/s41598-026-44308-8
Schlüsselwörter: serielle femtosekunden-Kristallographie, Flüssigkeitsstrahl-Probenzufuhr, Polyethylenoxid-Ummantelung, Röntgen-Freie-Elektronen-Laser, zeitaufgelöste Proteinkristallographie