Clear Sky Science · de
Spiegeln und Instabilität von Transthyretin und Korrelationen mit Kern‑Biomarkern bei der Alzheimer‑Krankheit
Warum das für die Gehirngesundheit wichtig ist
Die Alzheimer‑Krankheit entsteht nicht über Nacht; sie entwickelt sich über Jahre still und beginnt mit subtilen Gedächtnisproblemen, bevor sie zur vollen Demenz fortschreitet. Ärztinnen und Ärzte können bereits mehrere chemische Hinweise im Liquor und im Blut messen, die diesen Prozess verfolgen, doch sie erfassen nicht jeden Aspekt dessen, was im Gehirn schiefgeht. Diese Studie konzentriert sich auf Transthyretin, ein Transportprotein im Blut und Liquor, das möglicherweise hilft, die klebrigen Amyloid‑Moleküle, die mit Alzheimer in Verbindung stehen, zu binden. Zu verstehen, wie sich dieses Protein im Verlauf der Erkrankung verhält, könnte den Weg zu früherer Diagnostik und neuen Behandlungsstrategien ebnen.
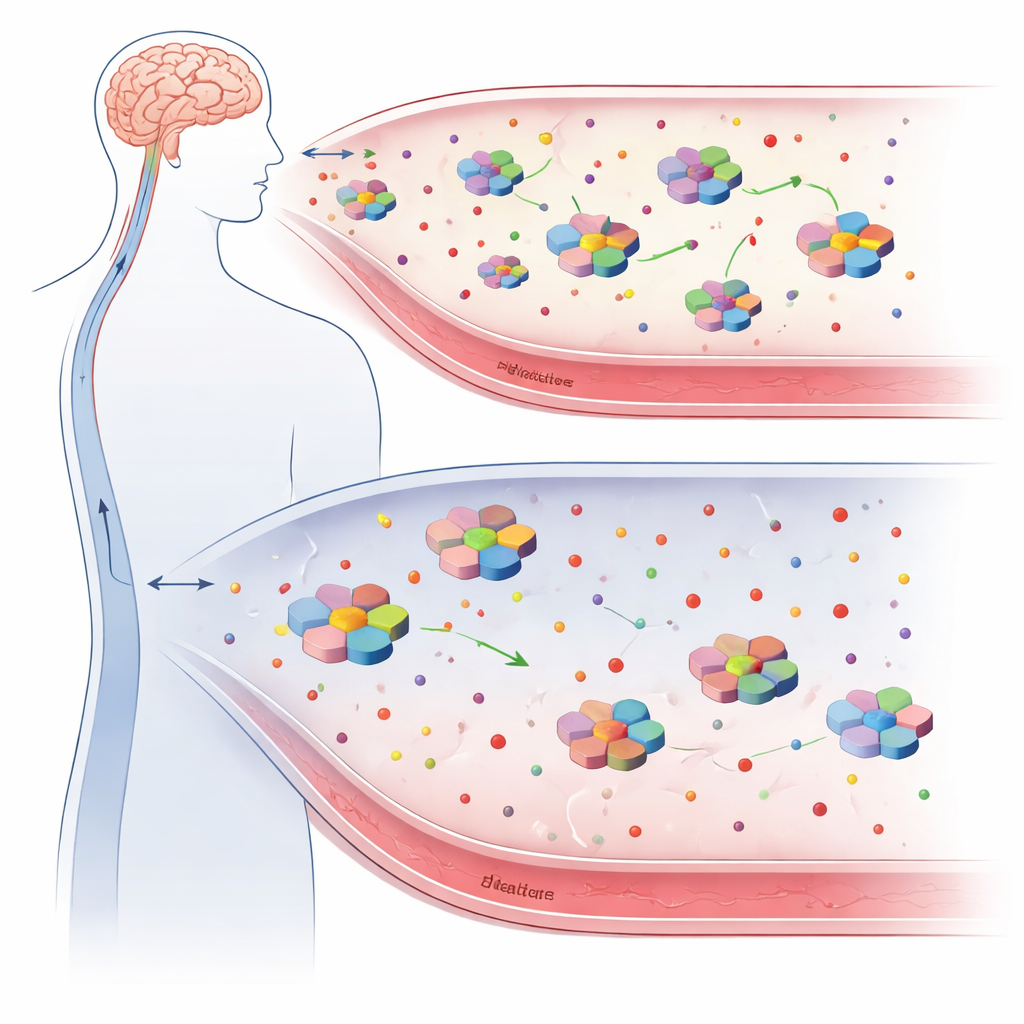
Ein Helferprotein im Rampenlicht
Transthyretin ist vor allem als Transporter von Schilddrüsenhormonen und vitamin‑A‑verwandten Verbindungen im Körper bekannt, hat in den letzten Jahrzehnten aber auch aus einem anderen Grund Aufmerksamkeit erregt: Es kann an Amyloid‑Beta binden, das Protein, das sich bei Alzheimer in Plaques verklumpt. Tierversuche legen nahe, dass Transthyretin, wenn es reichlich vorhanden und strukturell stabil ist, Amyloid‑Beta binden, dessen Aggregation verhindern und sogar dessen Abtransport aus dem Gehirn in den Blutkreislauf unterstützen kann. Fallen die Transthyretin‑Spiegel oder wird seine vierteilige Struktur instabil, kann diese Schutzwirkung nachlassen und möglicherweise mehr Amyloid‑Schaden erlauben.
Patienten entlang des Alzheimer‑Pfads verfolgen
Die Forschenden untersuchten 66 Menschen, bei denen im Liquor eindeutige Laborzeichen für Alzheimer‑typische Veränderungen vorlagen. Einige befanden sich in einem früheren Stadium mit leichter kognitiver Beeinträchtigung, in dem Gedächtnis‑ und Denkstörungen auffällig sind, das Alltagsleben aber noch weitgehend unabhängig bleibt. Andere hatten sich zur vollen Demenz entwickelt. Von jeder Person wurden Blut und Liquor entnommen und sowohl die Menge an Transthyretin als auch die Stabilität seiner vierteiligen (tetrameren) Struktur gemessen. Diese Messgrößen wurden mit etablierten Alzheimer‑Markern verglichen, darunter verschiedene Formen von Amyloid‑Beta, das Tau‑Protein und Indikatoren für Nervenzellschaden.
Veränderungen in frühen gegenüber späten Krankheitsstadien
Im Blut wiesen Menschen mit Demenz niedrigere Transthyretin‑Spiegel auf als jene mit leichter kognitiver Beeinträchtigung, und dieser Abfall war besonders ausgeprägt bei Frauen. Im Liquor erschienen die Gesamtkonzentrationen von Transthyretin hingegen zwischen den beiden Stadien ähnlich, was darauf hindeutet, dass Blut- und Gehirnkompartimente unterschiedlich reguliert werden. Bei genauerer Betrachtung der Gruppe mit leichter Beeinträchtigung zeigte sich ein klareres Muster: Personen mit geringeren Transthyretin‑Werten im Liquor hatten tendenziell höhere Tau‑Werte, höhere Neurofilament‑Light‑Chain‑Spiegel und erhöhte Mengen bestimmter Amyloid‑Beta‑Formen — Hinweise auf intensiveren Hirnschaden und stärkeren Amyloid‑Stress. Gleichzeitig war bei instabilerem Transthyretin im Liquor ein Schlüsselamyloidfragment (Aβ42) niedriger, was mit stärkerer Amyloidablagerung im Gehirn übereinstimmt.
Verbindungen zu Genen und direkten Labortests
Die Studie berücksichtigte außerdem einen bekannten genetischen Risikofaktor, die APOE‑ε4‑Variante. Unter Trägern dieses Risikogens zeigten diejenigen, die zur Demenz fortgeschritten waren, nicht nur niedrigere Transthyretin‑Werte im Blut, sondern auch Anzeichen größerer Transthyretin‑Instabilität im Liquor. Das deutet darauf hin, dass APOE‑ε4 das schützende Protein in der Gehirnumgebung fragiler machen könnte. Um zu prüfen, ob Amyloid selbst Transthyretin destabilisieren kann, führten die Forschenden ein Laborexperiment durch: Sie mischten gereinigtes Transthyretin mit Aβ42, dem Amyloidfragment, das am stärksten mit Alzheimer verknüpft ist, und inkubierten die Mischung schonend. Dabei beobachteten sie, dass der Kontakt mit Aβ42 Transthyretin von seiner stabilen vierteiligen Form in weniger stabile Fragmente drängte — ein Befund, der die Idee stützt, dass steigende Amyloidlasten die Struktur und Funktion von Transthyretin untergraben können.
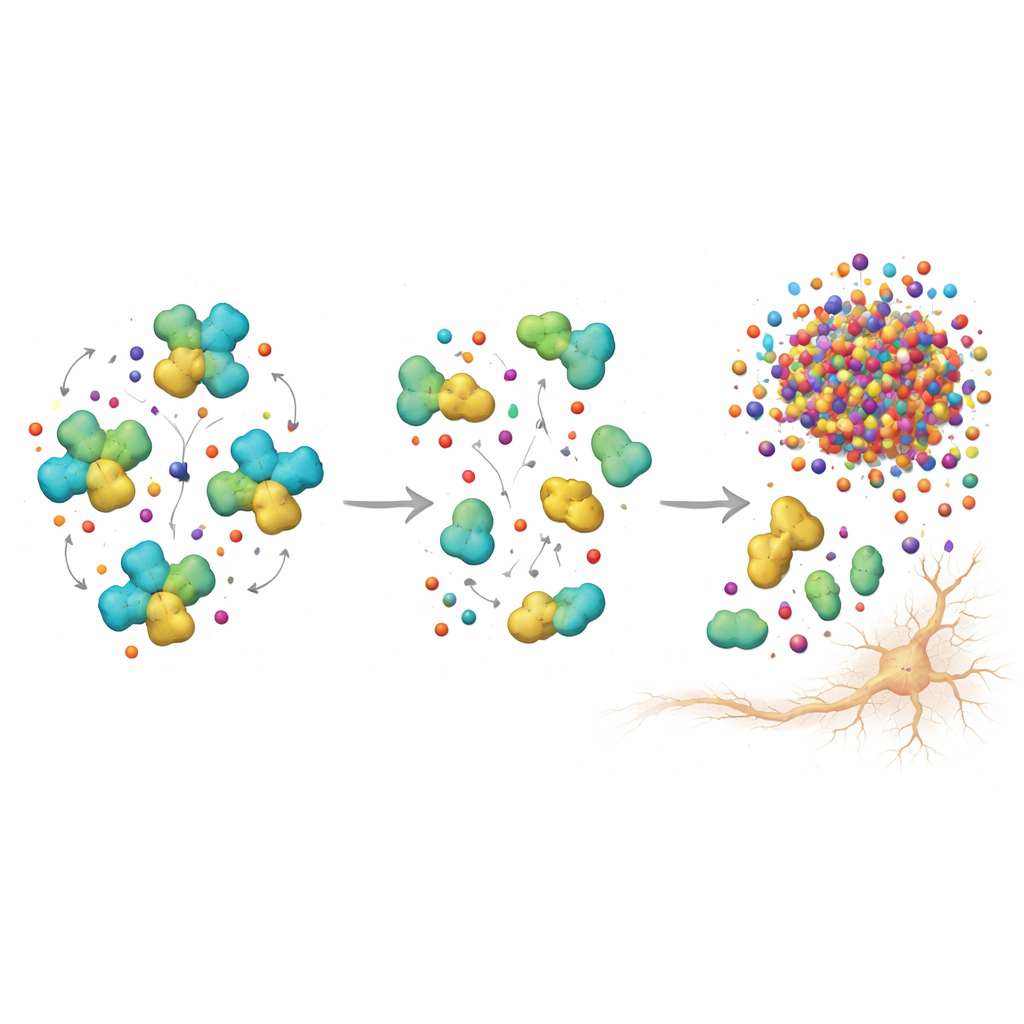
Was das für Diagnostik und Therapie in der Zukunft bedeutet
Kurz gesagt deutet diese Arbeit darauf hin, dass Transthyretin als früh reagierender Faktor bei der Alzheimer‑Krankheit fungiert. In der Phase leichter Beeinträchtigung spiegeln seine Menge und Stabilität im Liquor eng die Amyloidakkumulation und die ersten Anzeichen von Nervenzellschaden wider. Später, wenn die Demenz etabliert ist, sind die Transthyretin‑Spiegel im Blut deutlich niedriger, doch die engen Verknüpfungen zu Hirnmarkern schwächen sich möglicherweise ab, weil andere Prozesse dominanter werden. Für Laien lautet die Erkenntnis, dass Transthyretin wie ein schützender Müllsammler für schädliches Amyloid wirkt; wenn Amyloid zunimmt, kann es diesen Sammler destabilisieren und damit eine natürliche Abwehr schwächen. Die Verfolgung von Menge und struktureller Integrität von Transthyretin könnte Klinikerinnen und Klinikern helfen, Personen mit erhöhtem Risiko früher zu erkennen, und langfristig auf Therapien hinweisen, die darauf abzielen, dieses Protein zu stabilisieren, um die Gehirngesundheit zu erhalten.
Zitation: Gião, T., Tábuas-Pereira, M., Baldeiras, I. et al. Levels and instability of transthyretin and correlations with core biomarkers in Alzheimer’s disease. Sci Rep 16, 13024 (2026). https://doi.org/10.1038/s41598-026-41717-7
Schlüsselwörter: transthyretin, Alzheimer‑Krankheit, Amyloid‑Beta, leichte kognitive Beeinträchtigung, Biomarker