Clear Sky Science · ar
مستويات وعدم استقرار الترانستيرتين والارتباطات مع المؤشرات الحيوية الأساسية في مرض ألزهايمر
لماذا هذا مهم لصحة الدماغ
لا يظهر مرض ألزهايمر بين ليلة وضحاها؛ بل يتطور بصمت على مدى سنوات، ويبدأ بمشكلات ذاكرة طفيفة قبل أن يتقدم إلى الخَرَف الكامل. يمكن للأطباء بالفعل قياس عدة دلائل كيميائية في السائل النخاعي والدم تتتبع هذه العملية، لكنها لا تلتقط كل جوانب ما يخطئ في الدماغ. تركز هذه الدراسة على الترانستيرتين، وهو بروتين ناقل في الدم والسائل النخاعي قد يساعد في التقاط جزيئات الأميلويد اللزجة المرتبطة بألزهايمر. فهم كيفية تصرف هذا البروتين مع تقدم المرض قد يفتح أبوابًا لتشخيص مبكر واستراتيجيات علاجية جديدة.
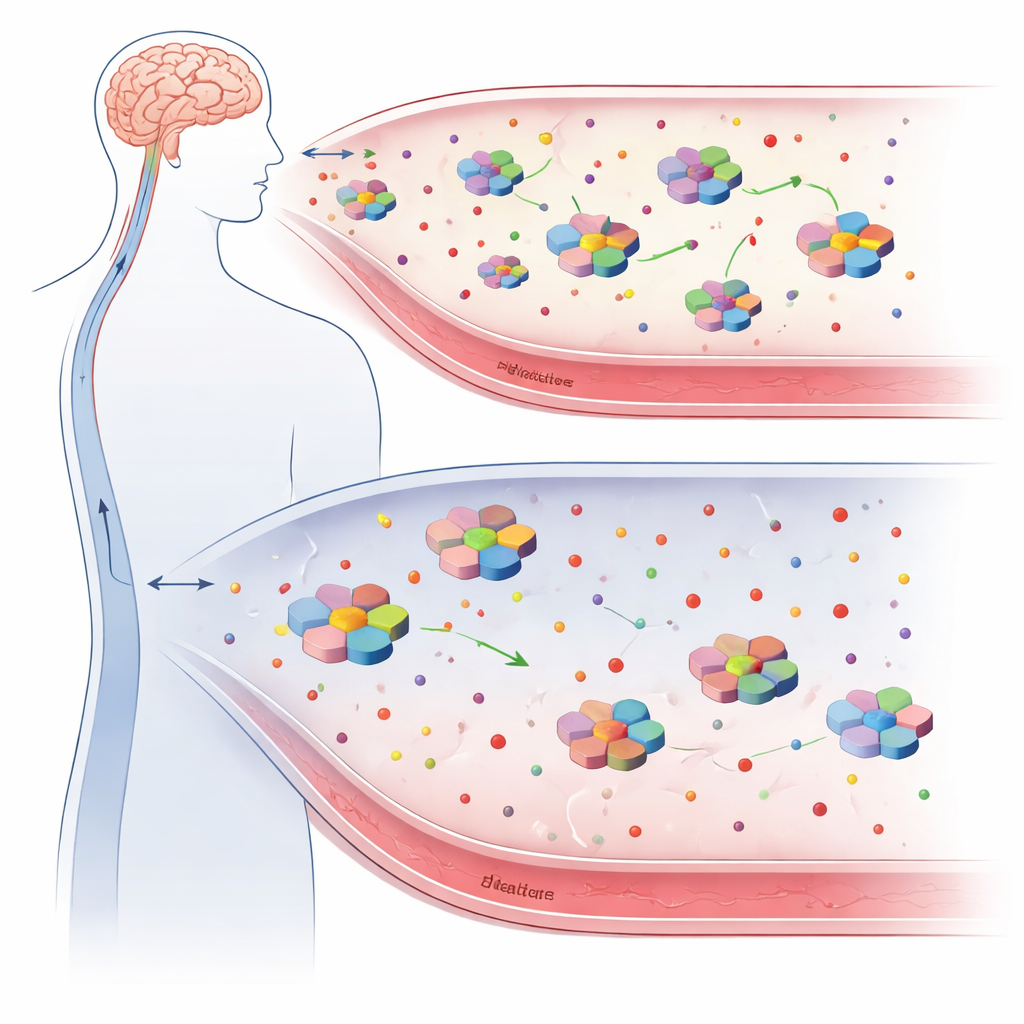
بروتين مساعد تحت الأضواء
يشتهر الترانستيرتين بنقله لهرمون الغدة الدرقية ومركبات مرتبطة بفيتامين A في الجسم، ولكن خلال العقود الماضية جذب الاهتمام لسبب آخر: يمكنه الارتباط ببيتا أميلويد، البروتين الذي يتكتل مكوّنًا لويحات في مرض ألزهايمر. تشير تجارب على الحيوانات إلى أنه عندما يكون الترانستيرتين متوفراً وبنيته سليمة، يمكنه أسر بيتا أميلويد ومنعه من التجمع، بل والمساعدة في نقله خارج الدماغ إلى مجرى الدم. عندما تنخفض مستويات الترانستيرتين، أو تصبح بنيته الرباعية غير مستقرة، قد تضعف هذه الحماية، مما يسمح باحتمال حدوث مزيد من أضرار الأميلويد.
متابعة المرضى على امتداد مسار ألزهايمر
درس الباحثون 66 شخصًا كان لديهم جميعًا أدلة مخبرية واضحة على تغيّرات من نمط ألزهايمر في السائل النخاعي. كان بعضهم في مرحلة ضعف الإدراك الخفيف المبكرة، حيث تكون مشاكل الذاكرة والتفكير ملحوظة لكن الحياة اليومية لا تزال مستقلة إلى حد كبير. الآخرون تقدموا إلى الخَرَف الكامل. من كل شخص جمع الفريق الدم والسائل النخاعي، ثم قاسوا كمية الترانستيرتين الموجودة ومدى استقرار بنيته الرباعية (التتتراميرية). قورنت هذه القياسات مع مؤشرات ألزهايمر القياسية، بما في ذلك أشكال مختلفة من بيتا أميلويد، والبروتين التاُو المرتبط بالألياف العصبية، ومؤشرات تلف الخلايا العصبية.
ما الذي يتغير في المراحل المبكرة مقابل المتأخرة
في الدم، كان لدى الأشخاص المصابين بالخرف مستويات ترانستيرتين أقل من أولئك ذوي مشاكل الإدراك الخفيفة، وكان هذا الانخفاض بارزًا بشكل خاص لدى النساء. ومع ذلك، في السائل النخاعي، بدت مستويات الترانستيرتين الإجمالية متشابهة بين المرحلتين، مما يوحي بأن تنظيم المقصورات الدموية والدماغية يختلف. عندما نظر الفريق عن كثب إلى مجموعة الضعف الإدراكي الخفيف المبكرة، ظهر نمط أوضح: الأفراد الذين كان لديهم ترانستيرتين أقل في السائل النخاعي ميّالون لوجود مستويات أعلى من التاُو، وسلسلة الخيوط العصبية الخفيفة (neurofilament light chain)، وأشكال معينة من بيتا أميلويد—وهي إشارات لضرر دماغي أشد وإجهاد أميلويد أكبر. في الوقت نفسه، عندما كان الترانستيرتين في السائل النخاعي أكثر عدم استقرار، كانت مستويات قطعة أميلويد رئيسية واحدة (Aβ42) أقل، بما يتماشى مع تراكم أميلويد أكثر كثافة داخل الدماغ نفسه.
روابط مع الجينات والاختبارات المخبرية المباشرة
أخذت الدراسة أيضًا بعين الاعتبار عامل خطر جيني معروف، وهو متغير APOE ε4. بين حاملي هذا الجين، أظهر الذين تقدموا إلى الخرف ليس فقط ترانستيرتين أقل في الدم بل أيضًا علامات على عدم استقرار أكبر للترانستيرتين في السائل النخاعي. يقترح هذا أن APOE ε4 قد يجعل البروتين الواقي أكثر هشاشة داخل بيئة الدماغ. لاختبار ما إذا كان الأميلويد نفسه يمكن أن يزعزع استقرار الترانستيرتين، أجرى العلماء تجربة مخبرية: مزجوا ترانستيرتين نقي مع Aβ42، قطعة الأميلويد المرتبطة أشد الارتباط بألزهايمر، وحضنوا المزيج بلطف. لوحظ أن التماس مع Aβ42 دفع الترانستيرتين بعيدًا عن شكله الرباعي المستقر نحو قطع أقل استقرارًا، مما يدعم فكرة أن زيادة عبء الأميلويد يمكن أن تضعف بنية ووظيفة الترانستيرتين.
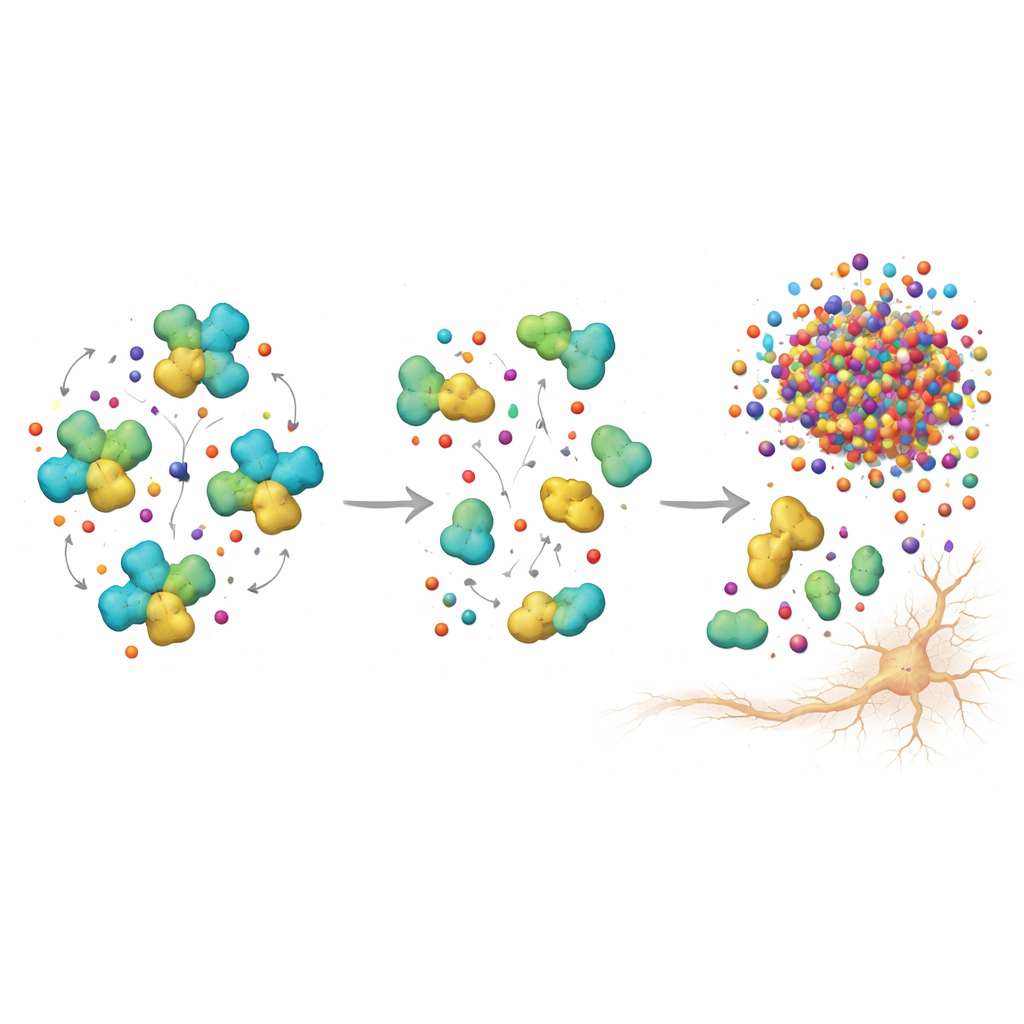
ما معنى هذا للتشخيص والعلاج في المستقبل
ببساطة، تشير هذه الدراسة إلى أن الترانستيرتين يعمل كمستجيب مبكر في مرض ألزهايمر. في مرحلة الضعف الإدراكي الخفيف، تعكس مستوياته واستقراره في السائل النخاعي تراكم الأميلويد وبدايات تلف الخلايا العصبية عن قرب. لاحقًا، بعد تأسيس الخرف، تنخفض مستويات الترانستيرتين في الدم بوضوح، لكن الروابط الوثيقة بمؤشرات الدماغ تتلاشى، ربما لأن عمليات أخرى تصبح مهيمنة. للخلاصة العامة: يبدو أن الترانستيرتين يعمل كجامع نفايات واقٍ للأميلويد الضار؛ ومع تراكم الأميلويد قد يزعزع هذا الجامع، مما يضعف نظام دفاع طبيعي. تتبع كمية الترانستيرتين—وما إذا كانت بنيته لا تزال سليمة—قد يساعد الأطباء على تحديد الأشخاص ذوي الخطر الأعلى مبكرًا وقد يشير في نهاية المطاف إلى علاجات تهدف إلى تثبيت هذا البروتين للحفاظ على صحة الدماغ.
الاستشهاد: Gião, T., Tábuas-Pereira, M., Baldeiras, I. et al. Levels and instability of transthyretin and correlations with core biomarkers in Alzheimer’s disease. Sci Rep 16, 13024 (2026). https://doi.org/10.1038/s41598-026-41717-7
الكلمات المفتاحية: الترانستيرتين, مرض ألزهايمر, بيتا أميلويد, ضعف الإدراك الخفيف, المؤشرات الحيوية