Clear Sky Science · de
Ein Einzelzell- und Raum-Zeit-Atlas der frühen menschlichen Riechentwicklung
Wie unser Geruchssinn beginnt
Der Geruchssinn prägt, wie wir Nahrung, Gefahr und sogar andere Menschen wahrnehmen, doch wir wissen überraschend wenig darüber, wie dieses System im menschlichen Fötus zuerst entsteht. Diese Studie nutzt moderne genetische Kartierungsmethoden, um einen detaillierten Atlas der frühen menschlichen Nase zu erstellen, mit Schwerpunkt auf dem Gewebe, das später Gerüche wahrnehmen wird. Indem die Forschenden Tausende einzelner Zellen und ihre Lage in der sich entwickelnden Nasenhöhle verfolgten, zeigen sie, wie die riechende Auskleidung der Nase aufgebaut wird und wann deren Nervenzellen erstmals ihre Geruchsrezeptoren einschalten.
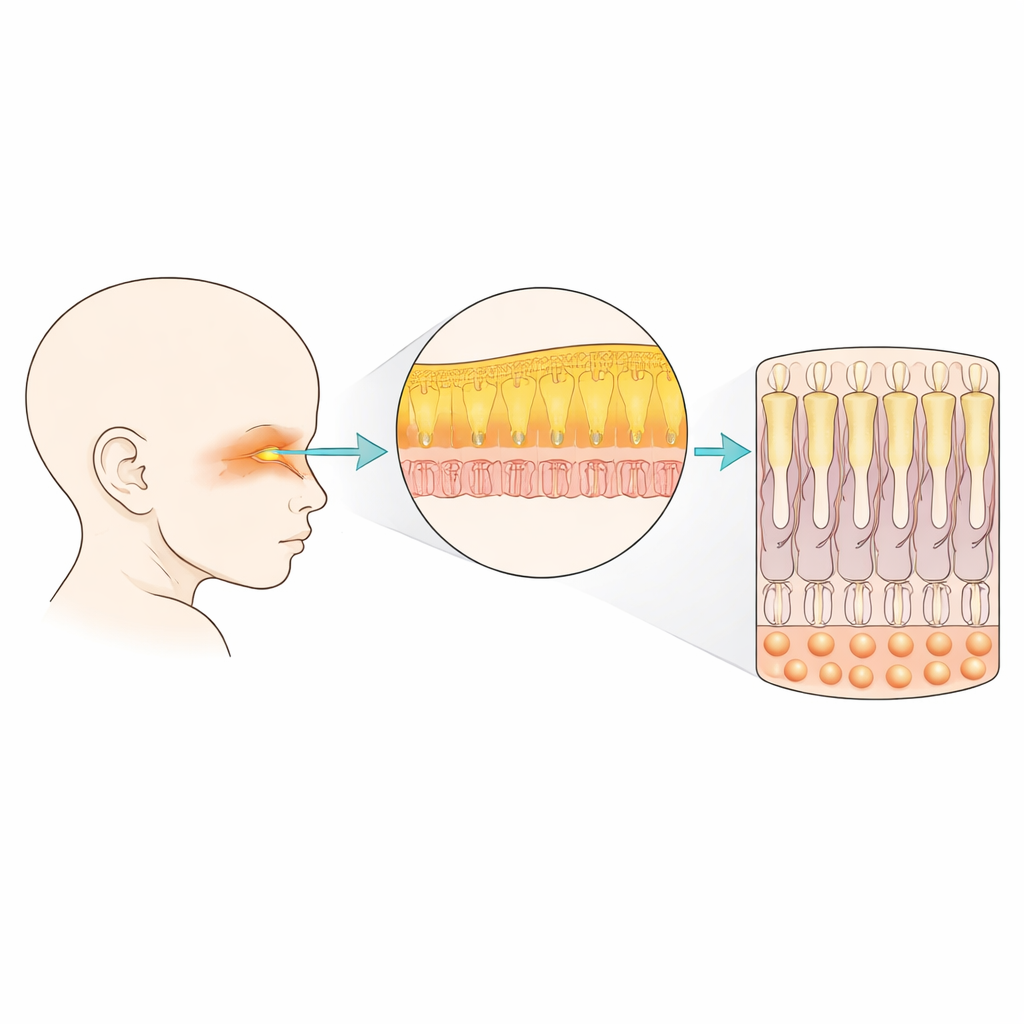
Bausteine der frühen Nase
Die menschliche Nase ist mehr als ein einfacher Luftkanal. Bereits im ersten Trimester enthält sie Knorpel, Knochen, Blutgefäße, Immunzellen sowie verschiedene Typen von Nerven- und Stütz-Zellen. Das Team untersuchte Nasengewebe von menschlichen Föten im Alter von 7 bis 12 Wochen nach der Befruchtung und analysierte fast 42.000 einzelne Zellkerne. Aus diesen Daten konnten die Forschenden die Zellen in 32 unterschiedliche Gruppen einteilen, darunter Nervenzellen, deren Vorläufer, Strukturzellen und die Auskleidungszellen sowohl des riechenden als auch des atemwegsbedeckenden Bereichs der Nase. Das zeigte, wie früh die Nasenregion bereits einem komplexen Mini-Organ ähnelt und nicht nur einem einfachen Zellblatt.
Formung der riechenden Auskleidung
Innerhalb dieses komplexen Gewebes konzentrierten sich die Forschenden auf das Riechepithel — den spezialisierten Streifen aus Gewebe, der die riechenden Nervenzellen beherbergt. Sie identifizierten die Hauptakteure: basale, stammzellähnliche Zellen an der Basis, Zwischenvorläufer, unreife Riechsinneszellen sowie Stützzellen und mikroville Zellen näher an der Oberfläche. Im Verlauf der Entwicklung beobachteten sie einen klaren Wandel: anfangs sind teilende Stamm- und Vorläuferzellen weit verbreitet; später weichen sie einer wachsenden Zahl unreifer Neurone und Stützzellen. Durch den Vergleich von Genaktivitätsmustern leiteten die Autorinnen und Autoren ab, wie basale Zellen mehrere Zweige des Gewebes hervorbringen und sowohl die neuronale Linie als auch nicht-neuronale Stützlinien versorgen, was darauf hindeutet, dass die lebenslange Fähigkeit der Nase, ihre Riechzellen zu erneuern, bereits sehr früh in der Entwicklung angelegt ist.
Kartierung der Zellen in ihrer natürlichen Nachbarschaft
Zu wissen, welche Zelltypen existieren, ist nur die halbe Geschichte; ebenso wichtig ist, wo sie im Gewebe liegen. Um jeden Zelltyp wieder in seinen physischen Kontext einzuordnen, nutzte das Team eine Technik, die die Positionen von hunderten verschiedenen RNA-Molekülen in dünnen Schnitten fötaler Köpfe aufzeichnet. Diese räumliche Karte bestätigte, dass das Riechepithel und das benachbarte respiratorische Epithel getrennte, aber aneinandergrenzende Bereiche bilden. Sie zeigte auch, dass die riechende Region nicht einheitlich ist: ihre vorderen und hinteren Abschnitte sowie obere und untere Bereiche weisen unterschiedliche Dicken und Zellzusammensetzungen auf. Wichtige Entwicklungssignale bilden gemusterte Zonen im umliegenden Gewebe, was darauf hindeutet, dass lokale chemische Hinweise dazu beitragen, wo Riechzellen entstehen und wie sich das Epithel entlang der Nasenhöhle ausdehnt.
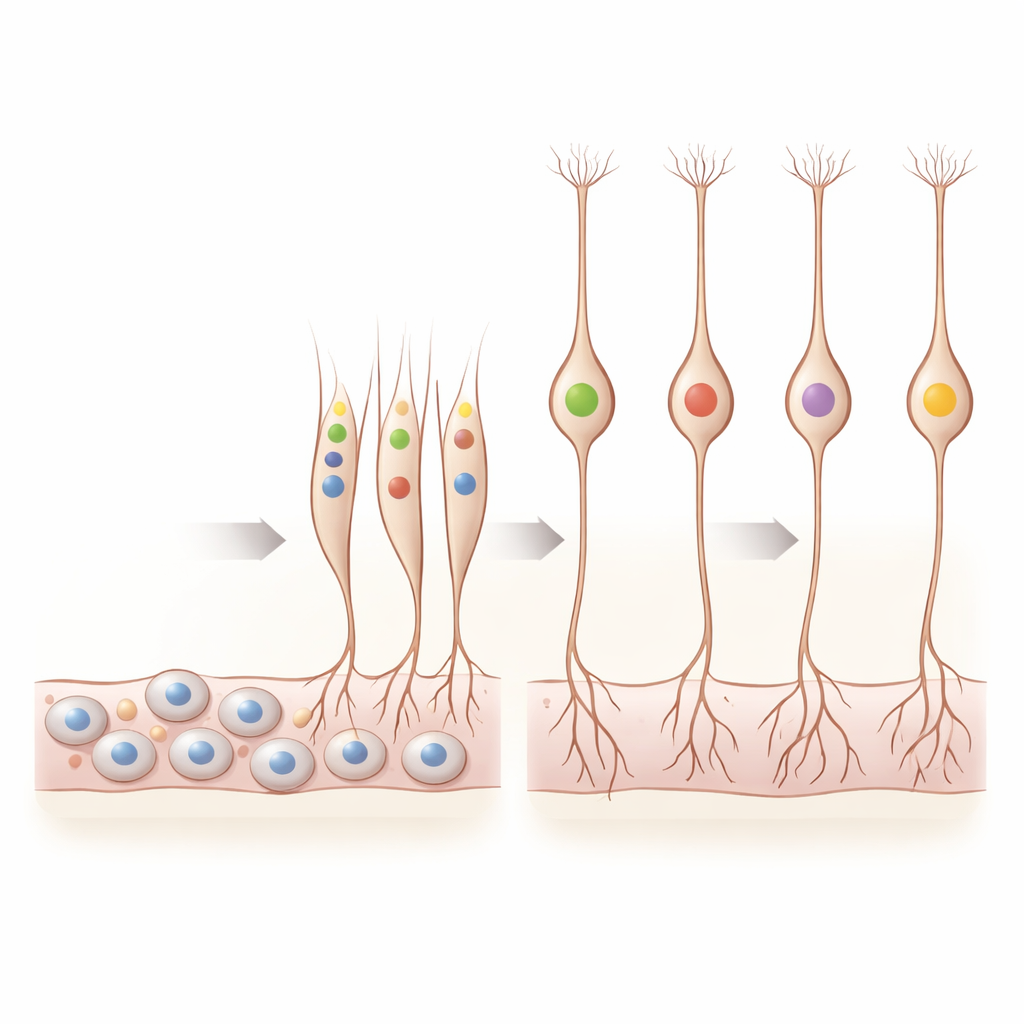
Wann Neurone entscheiden, was sie riechen
Ein zentrales Rätsel der Riechbiologie ist, wie jede Sinneszelle letztlich genau einen Geruchsrezeptor aus den Hunderten, die in unserer DNA codiert sind, nutzt. Indem die Forschenden Rezeptorgene in einzelnen fötalen Neuronen untersuchten, fanden sie heraus, dass diese „eine Zelle–ein Rezeptor“-Regel bereits im ersten Trimester Gestalt annimmt. Sie detektierten 169 verschiedene aktivierte Geruchsrezeptorgene, überwiegend in unreifen Riechsinneszellen. Viele Vorläuferzellen zeigten keine Rezeptoraktivität, doch sobald die Neurone zu reifen begannen, drückte ein wachsender Anteil einen einzelnen dominanten Rezeptor aus, während nur eine kleine Minderheit kurzzeitig zwei oder mehr zeigte. Im Verlauf der untersuchten Wochen wurden Zellen mit starker Dominanz eines Rezeptors häufiger, und Rezeptorsignale waren räumlich eng auf das Riechepithel beschränkt.
Was das für Gesundheit und Krankheit bedeutet
Zusammen zeigen diese Ergebnisse, dass die grundlegende Architektur und die Kernregeln des menschlichen Geruchssystems bemerkenswert früh vor der Geburt festgelegt werden. Die Nasenschleimhaut enthält bereits die meisten der wichtigen Zelltypen, die auch bei Erwachsenen vorkommen; Stammzellen sind in Erneuerungsbahnen organisiert, und sich entwickelnde Neurone verpflichten sich innerhalb bestimmter Regionen des Gewebes zu einzelnen Geruchsrezeptoren. Dieser Atlas bietet eine Referenzkarte für Forschende, die angeborene Fehlbildungen der Nase, vererbten Geruchsverlust und Erkrankungen untersuchen, bei denen Riechstörungen ein frühes Warnzeichen für Hirnkrankheiten sind. Indem er aufzeigt, wann und wo Vorgänge normal ablaufen sollen, liefert er einen Leitfaden zum Verständnis — und schließlich zur Korrektur — dessen, was schiefläuft, wenn sich der Geruchssinn nicht richtig entwickelt.
Zitation: Mbouamboua, Y., Lebrigand, K., Nampoothiri, S. et al. A single-cell and spatial atlas of early human olfactory development. Nat Commun 17, 3537 (2026). https://doi.org/10.1038/s41467-026-71595-6
Schlüsselwörter: Riechentwicklung, Einzelzell-Atlas, räumliche Transkriptomik, Riechrezeptoren, fötales Nasenepithel