Clear Sky Science · de
Maschinelles Lernen unterstütztes Einzelmolekül‑Sensing zur standardfreien Quantifizierung von per‑ und polyfluorierten Carbonsäuren
Warum das für die tägliche Wassersicherheit wichtig ist
Unsichtbare Industriechemikalien, bekannt als PFAS, haben sich in Flüsse, Trinkwasser und sogar in unser Blut eingeschlichen. Unter ihnen sind per‑ und polyfluorierte Carbonsäuren (PFCAs) besonders besorgniserregend, doch sie sind extrem schwer genau zu messen, weil Referenzstandards nur für einen winzigen Bruchteil der tausenden PFAS existieren. Diese Studie stellt eine neue Methode vor, um einzelne PFCA‑Moleküle eins nach dem anderen zu „zählen“, während sie durch ein winziges biologisches Loch passieren, und nutzt Maschinelles Lernen, um ihre elektrischen Fingerabdrücke zu erkennen—ohne für jede Verbindung einen passenden Laborstandard zu benötigen.
Verborgene Chemikalien in einer komplexen Familie
PFAS bilden eine weitläufige Familie fluorreicher Chemikalien, die in Produkten von antihaftbeschichtetem Kochgeschirr bis zu Feuerlöschschaum eingesetzt werden. Viele unterscheiden sich nur um wenige Atome, doch diese kleinen strukturellen Veränderungen können dramatisch beeinflussen, wie sie sich in der Umwelt bewegen, in Organismen anreichern oder die Gesundheit beeinträchtigen. Traditionelle Techniken wie Flüssig‑ oder Gaschromatographie in Kombination mit Massenspektrometrie können viele PFAS mit hoher Empfindlichkeit nachweisen, benötigen aber in der Regel ein reines Standardmuster jeder Substanz, um sie zuverlässig zu identifizieren und zu quantifizieren. Bisher gibt es kommerzielle Standards für etwas mehr als hundert PFAS—weniger als ein Prozent der bekannten Verbindungen—wodurch Regulierungsbehörden und Wissenschaftler zu großen Teilen im Unklaren über den Rest bleiben.
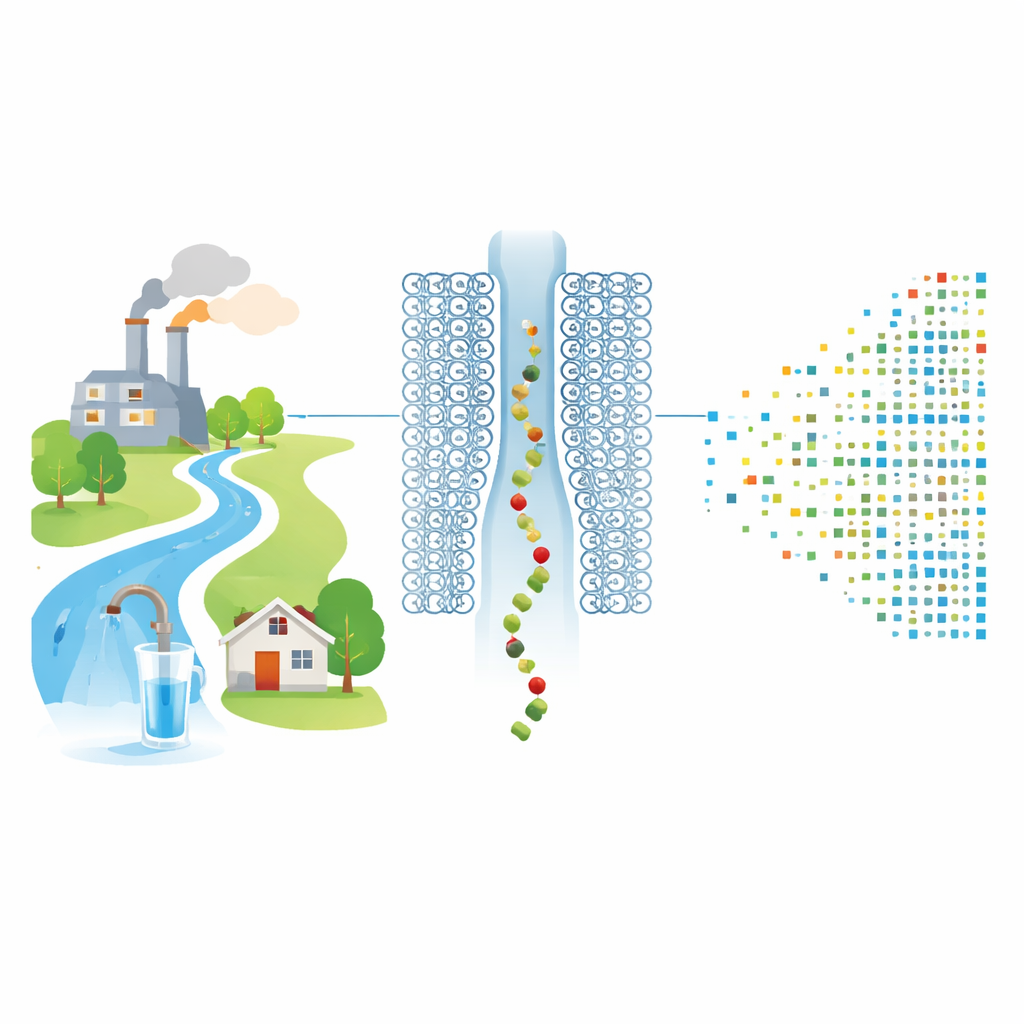
Einzelmoleküle durch ein winziges Tor zählen
Die Forscher schließen diese Lücke mithilfe einer Proteinnanopore: eines ringförmigen Moleküls, das ein einzelnes Loch in einer Lipidmembran bildet. Wird eine Spannung angelegt, fließen Ionen durch die Pore und erzeugen einen stabilen elektrischen Strom. Das Team bindet chemisch einzelne PFCA‑Moleküle an kurze positiv geladene Peptid‑„Leitfäden“, die wie Perlen auf einer Schnur in die Nanopore gezogen werden. Sobald jedes PFCA–Peptid‑Paar in die Pore eintritt und sie besetzt, blockiert es teilweise den Ionenfluss und verursacht einen kurzen Stromabfall, dessen Tiefe und Dauer von Größe und Form des Moleküls in der Pore abhängen.
Poresignale in ein molekulares Maß umwandeln
Ein wichtiger Durchbruch dieser Arbeit ist, dass sich diese Stromabfälle wie ein präzises Messlineal verhalten. Durch die Kombination von Experimenten mit molekularen Simulationen zeigen die Autoren, dass bei einer Reihe von PFCA‑Molekülen bis zu 14 Kohlenstoffatomen die Tiefe der Stromblockade nahezu linear mit dem Molekülvolumen zunimmt. Mit anderen Worten: Sobald Nanopore und Peptid gewählt sind, sagt allein das Volumen vorher, wie stark der Strom blockiert wird. Dadurch konnte das Team die elektrische Signatur anderer, komplexerer PFCAs vorhersagen—etwa mit Wasserstoff‑ oder Chlor‑Substitutionen, Seitenketten oder aromatischen Ringen—und experimentell bestätigen, dass die Vorhersagen innerhalb der geringen Messfehlergrenzen mit der Realität übereinstimmen.
Maschinelles Lernen, das ähnlich aussehende Schadstoffe erkennt
Weil viele PFCA‑Verwandte so ähnlich in der Größe sind, dass sich ihre Blockaden überlappen, nutzten die Wissenschaftler die volle Informationsfülle des Nanopore‑Signals. Sie extrahierten Dutzende Merkmale aus jedem Ereignis, darunter Dauer, Rauschverhalten und wie sich die Form ändert, wenn das Signal bei unterschiedlichen Frequenzen digital gefiltert wird. Mit maschinellen Lernmodellen, die auf diesen multidimensionalen Fingerabdrücken trainiert wurden, erreichten sie nahezu perfekte (etwa 99,9 %) Identifikationsraten über 13 PFCA‑Typen, einschließlich eng verwandter Isomere. Durch sorgfältige Auswahl der 21 informativsten Merkmale reduzierten sie die Modellkomplexität und verbesserten gleichzeitig die Leistung—selbst wenn die Zielchemikalie in einer Mischung von interferierenden PFCAs in 100‑fach höherer Konzentration verborgen war.
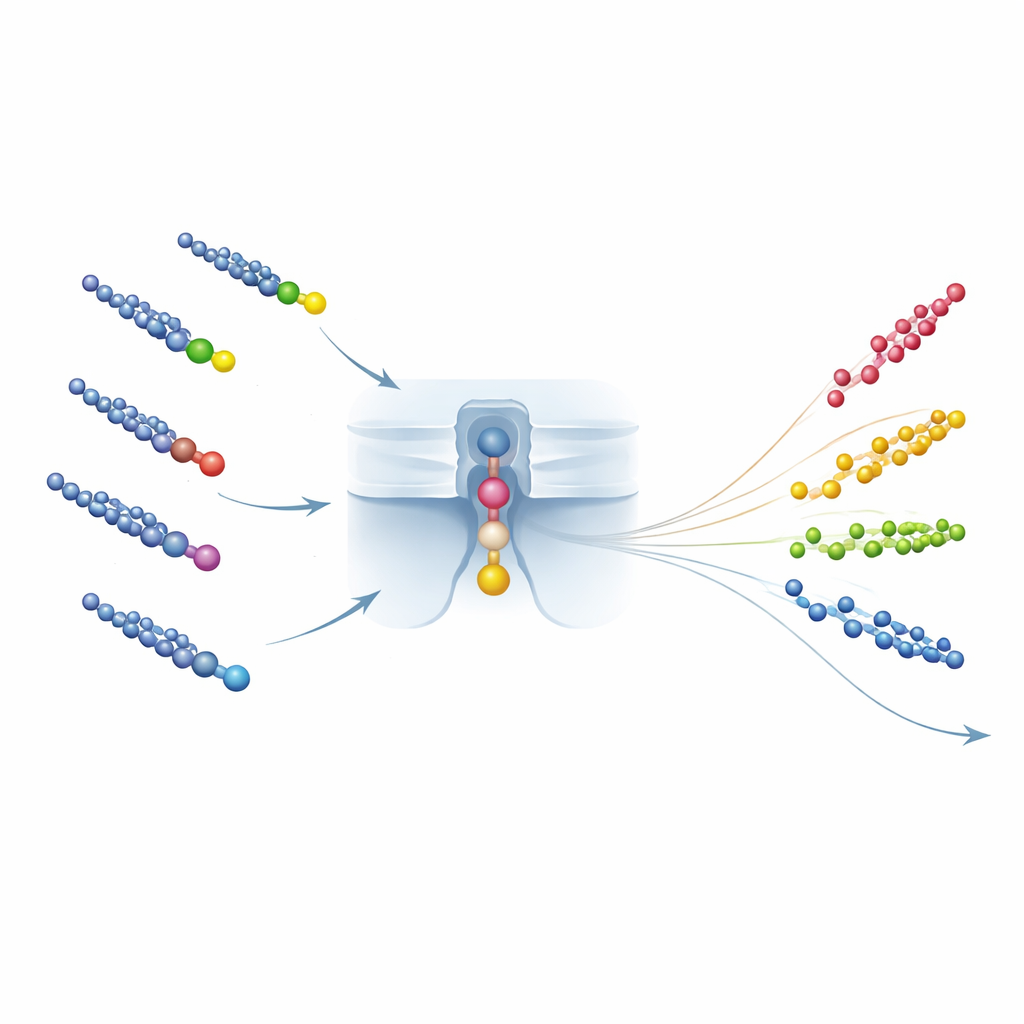
Von Einzelmolekülzählungen zu realen Wassertests
Neben der Identifikation muss die Methode auch messen, wie viel von jedem PFCA vorhanden ist. Hier nutzt das Team die Rate, mit der PFCA–Peptid‑Paare von der Nanopore erfasst werden: Die mittlere Zeit zwischen Ereignissen verkürzt sich mit steigender Konzentration. Durch geschicktes Peptiddesign wird sichergestellt, dass diese Erfassungsrate hauptsächlich durch die Ladung des Peptids und die elektrische Landschaft der Pore bestimmt wird und weit weniger durch die Art des gebundenen PFCA. Das bedeutet, dass eine einzige Kalibrierkurve—die Ereignisfrequenz mit der Konzentration verknüpft—für viele PFCAs verwendet werden kann, was die von den Autoren beschriebene „eine Kalibrierkurve für alle“ ermöglicht. Sie validieren diese Universalität in Mischungen und in komplexen Proben wie Leitungswasser und Serum und zeigen genaue Zählungen selbst in Anwesenheit vieler anderer Chemikalien; für die ultrakurze PFCA Trifluoressigsäure erreichen sie Nachweisgrenzen, die mit den besten Massenspektrometriemethoden vergleichbar sind.
Ein neuer Weg, PFAS ohne individuelle Standards nachzuverfolgen
Insgesamt skizziert diese Arbeit einen Weg, um ein breites Spektrum PFCA‑Verschmutzungen zu überwachen, ohne für jede Verbindung einen maßgeschneiderten Standard zu benötigen. Eine sorgfältig entwickelte Nanopore und ein Peptid‑Sonde schaffen eine einfache lineare Verbindung zwischen Molekülgröße und Signal, während Maschinelles Lernen subtile Signalmerkmale herausarbeitet, um selbst nahezu identische Isomere zu unterscheiden. Durch weiteres Abstimmen der Eintritts‑ und Austritts‑„Barrieren“ der Pore zeigen die Autoren in Experimenten und Simulationen, wie dieselbe Strategie auf längerketten‑PFCAs und möglicherweise auf das weitere PFAS‑Spektrum ausgeweitet werden könnte. Für die breite Öffentlichkeit bedeutet das eine vielversprechende neue Möglichkeit, Chemikalien sichtbar zu machen und zu messen, die lange Zeit in unserem Wasser und unserer Umwelt weitgehend unsichtbar blieben.
Zitation: Zuo, J., Li, HS., Tang, W. et al. Machine learning assisted single-molecule sensing towards standard-free quantification of per- and polyfluoroalkyl carboxylic acids. Nat Commun 17, 3923 (2026). https://doi.org/10.1038/s41467-026-70718-3
Schlüsselwörter: PFAS, Nanoporen‑Sensing, Einzelmolekül‑Detektion, Maschinelles Lernen, Wasserkontaminanten