Clear Sky Science · de
Analyse isobarischer quantitativer Proteomikdaten mit TMT-Integrator und der FragPipe-Computationsplattform
ProteINmessungen in klare Bilder verwandeln
Die moderne Biologie muss oft Tausende von Proteinen über viele Patientenproben, Zelltypen oder Behandlungen hinweg vergleichen. Messungen mit heutigen Massenspektrometern erzeugen gewaltige Datenmengen, die zwar mächtig, aber schwer zu handhaben sind. Dieser Artikel stellt TMT-Integrator vor, ein in die FragPipe-Plattform integriertes Softwarewerkzeug, das Forschenden hilft, komplexe Proteinmessungen in zuverlässige, leicht analysierbare Tabellen zu überführen. Durch das Bereinigen und Vergleichbarmachen dieser Daten über Experimente hinweg erleichtert die Methode das Verständnis von Erkrankungen wie Krebs, die Prüfung neuer Technologien und die Kombination von Proteindaten mit anderen molekularen Messgrößen wie RNA.
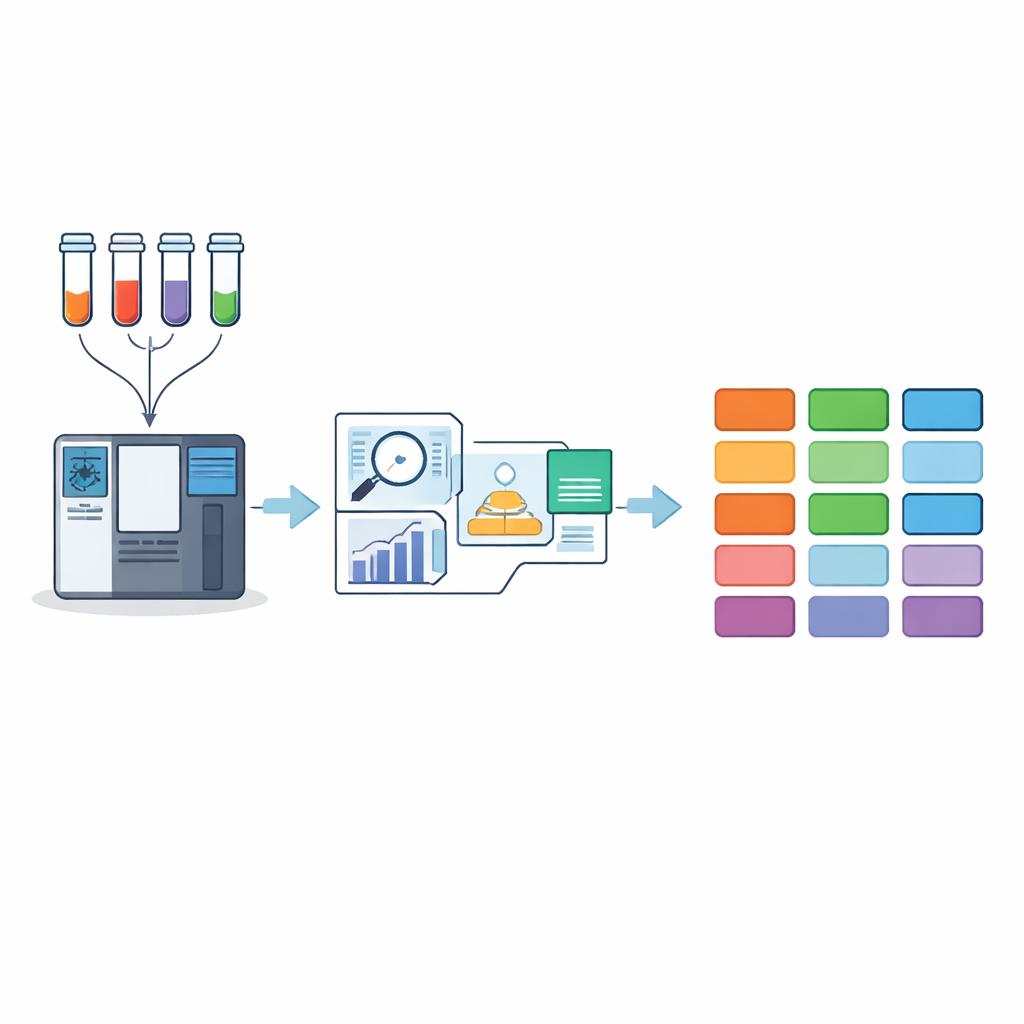
Viele Proben gleichzeitig messen
Die Studie konzentriert sich auf eine Familie chemischer Marker, die als isobare Tags bekannt sind, üblicherweise TMT und iTRAQ genannt. Diese Tags erlauben es Forschenden, viele verschiedene Proben zu mischen und in einem einzigen Lauf auf einem Massenspektrometer zu analysieren, was Experimente deutlich beschleunigt und technische Variabilität reduziert. Jede Probe erhält ein leicht unterschiedliches Tag, und wenn die Proteine im Instrument in Fragmente zerlegt werden, erzeugen die Tags charakteristische Signale, die zeigen, wie viel von jedem Protein aus welcher Probe stammt. Dieses sogenannte Multiplexing ist inzwischen Routine in großen Krebsstudien, bei der Suche nach Wirkstoffzielen und sogar in der Einzelzellproteomik. Rohsignale sind jedoch durch Rauschen, Interferenzen und Unterschiede zwischen Chargen beeinträchtigt, sodass anspruchsvolle Rechenverfahren erforderlich sind, um die Ergebnisse sinnvoll zu interpretieren.
Von Rohsignalen zu vertrauenswürdigen Zahlen
TMT-Integrator ist das Ende eines größeren FragPipe-Workflows, der mit der Identifizierung von Peptiden aus Massenspektren und deren Zuordnung zu Proteinen und Genen beginnt. Das Werkzeug verarbeitet detaillierte Tabellen von Peptid-Spektrum-Übereinstimmungen und Reporter-Ion-Signalen aus einem oder mehreren multiplexen Läufen und führt dann eine Reihe sorgfältig entworfener Schritte aus. Es filtert unzuverlässige Messungen heraus, wandelt Rohintensitäten in Verhältnisse relativ zu einer gewählten Referenzprobe um, fasst Peptidmessungen zu höheren Zusammenfassungen zusammen, entfernt Ausreißer und konvertiert die Verhältnisse anschließend zurück in intensivitätsähnliche „Abundanz“-Werte. Dieser Prozess lässt sich auf mehreren Ebenen anwenden, einschließlich Gene, Proteine, Peptidsequenzen und spezifische Modifikationsstellen wie Phosphorylierung. TMT-Integrator bietet außerdem flexible Normalisierungsoptionen und kann mit einer realen Referenzprobe, die in jeder Charge vorkommt, oder einer aus den Daten berechneten „virtuellen“ Referenz arbeiten.
Viele Chargen und viele Technologien handhaben
Eine große Herausforderung in umfangreichen Projekten ist, dass ein Satz von Labels nicht alle Proben abdecken kann, sodass Studien über mehrere Chargen oder „Plexe“ verteilt werden. Kleine Unterschiede zwischen diesen Plexen können echte biologische Veränderungen verschleiern. Die Autoren zeigen, wie die Ratio-zu-Referenz-Strategie von TMT-Integrator, kombiniert mit realen oder virtuellen Referenzkanälen, diese Plexe effektiv verbindet und gleichzeitig Batch-Effekte reduziert. An Datensätzen klarzelligen Nierenkrebses aus einem nationalen Krebsprogramm demonstrieren sie, dass FragPipe mit TMT-Integrator mehr Proteine und mehr Phosphorylierungsstellen erkennt als weit verbreitete Alternativen wie MaxQuant und Proteome Discoverer, insbesondere bei Proteinen mit niedriger Abundanz. Die resultierenden Proteinmessungen stimmen besser mit entsprechenden RNA-Daten überein, erfassen bekannte Beziehungen innerhalb von Proteinkomplexen und Signalwegen und zeigen geringeres Rauschen in Qualitätskontrollproben.
Hineinzoomen auf Proteinmodifikationen
Viele Signalereignisse in Zellen beruhen auf winzigen chemischen Markierungen an bestimmten Positionen von Proteinen. Diese „posttranslationale Modifikationen“ an Einzelstellen zu erfassen, ist technisch anspruchsvoll. TMT-Integrator verwendet Ort-Lokalisierungsinformationen aus einem speziellen Tool, um sowohl Multi-Site- als auch Single-Site-Ansichten modifizierter Peptide zu erstellen. In Phosphorylierungsdaten von Nierenkrebs liefert es eine umfangreiche Abdeckung modifizierter Proteine, Peptide und einzelner Stellen, trennt Tumor- und Normalproben klar und liefert konsistente Messungen über Replikatkontrollen hinweg. Im Vergleich zu MaxQuant meldet es mehr Stellen mit guter Vollständigkeit und bessere Übereinstimmung zwischen wiederholten Läufen und erzeugt Abundanz-ähnliche Tabellen, die sich leichter mit anderen Omics-Ebenen integrieren lassen.
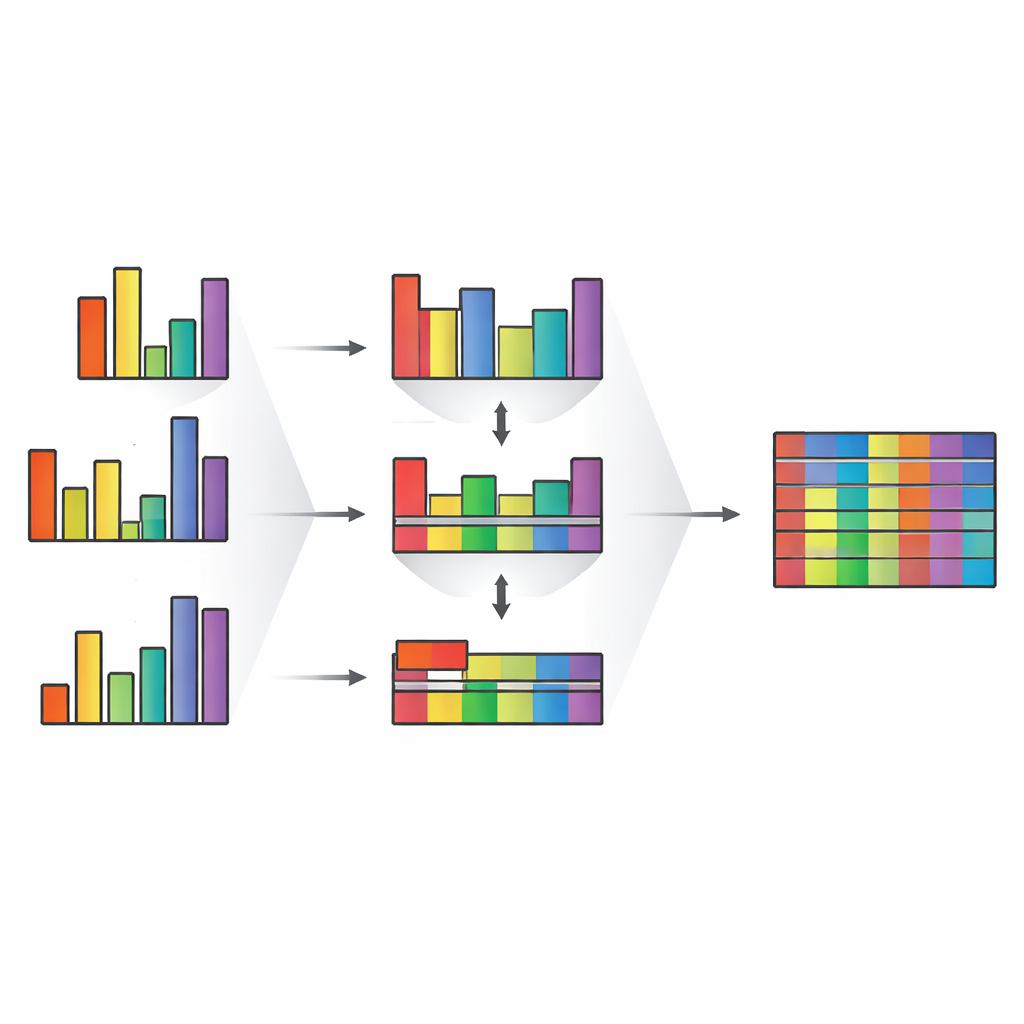
Bereit für Instrumente der nächsten Generation
Die Autoren testen TMT-Integrator auch an hochmodernen Datensätzen. Auf einem neuen Orbitrap Astral-Massenspektrometer vergleichen sie isobarische Markierung mit einem anderen Ansatz, der datenunabhängige Akquisition genannt wird, und finden, dass die TMT-Pipeline in FragPipe eine tiefe Abdeckung mit hoher Präzision und starker Übereinstimmung zur alternativen Methode erreicht. In einem separaten Datensatz mit 35-plex-Reagenzien, die reguläre und deuteriummarkierte Tags kombinieren, bewältigt die virtuelle Referenzstrategie des Programms erfolgreich subtile Verschiebungen in der Retentionszeit und liefert konsistente Protein-Fold-Changes zwischen Zelllinien, ohne in jedem Lauf spezielle Brückenproben zu benötigen. Diese Ergebnisse deuten darauf hin, dass das Werkzeug mit der raschen Weiterentwicklung von Hardware und Markierungschemien Schritt halten kann.
Was das für die biologische Forschung bedeutet
Insgesamt zeigt die Arbeit, dass TMT-Integrator als Teil von FragPipe komplexe, multiplexe Proteomikexperimente in präzise, interpretierbare Tabellen auf mehreren biologischen Ebenen überführen kann. Durch höhere Empfindlichkeit, Verringerung technischer Artefakte und Bereitstellung sowohl von Verhältnissen als auch Abundanz-Ausgaben hilft es Forschenden, sicherere Verknüpfungen zwischen Proteinen, Genen und Krankheitszuständen herzustellen. Für den allgemein Interessierten lautet die Kernbotschaft: Bessere Software zur Verarbeitung von Massenspektrometriedaten führt direkt zu klareren biologischen Geschichten, zuverlässigeren Biomarkern und einer solideren Grundlage für die Präzisionsmedizin.
Zitation: Chang, HY., Deng, Y., Li, R. et al. Analysis of isobaric quantitative proteomic data using TMT-Integrator and FragPipe computational platform. Nat Commun 17, 4010 (2026). https://doi.org/10.1038/s41467-026-70118-7
Schlüsselwörter: quantitative Proteomik, MASSENspektrometrie, isobarische Markierung, Datenanalyse-Pipelines, Proteinphosphorylierung