Clear Sky Science · de
Duale Dekonvolution in multiphotonener strukturierten Beleuchtungs-Mikroskopie für superauflösende Bildgebung in tiefem Gewebe
Tiefer blicken in lebendes Gewebe
Die moderne Biologie ist oft darauf angewiesen, winzigste Details in dicken Gewebestücken wie Gehirnabschnitten oder sich entwickelnden Embryonen zu sehen. Leider wird Licht beim Durchgang durch diese dichten Umgebungen gebrochen und gestreut, wodurch Bilder gerade dann unscharf werden, wenn Forscher scharfe Ansichten am meisten benötigen. Dieser Artikel stellt eine Methode vor, diese Bilder digital „zu entschmieren“, sodass ein gängiges fortgeschrittenes Mikroskop extrem feine Strukturen tief im Gewebe offenlegen kann—ohne zusätzliche teure oder komplexe Hardware.
Warum Tiefenbildgebung so schwierig ist
Fluoreszenzmikroskope erlauben es Forschern, bestimmte Moleküle zu markieren und zu beobachten, wie Zellen und Gewebe aufgebaut sind und sich verhalten. In den vergangenen Jahrzehnten haben mehrere „Superauflösungs“-Verfahren die traditionellen Schärfelimits überwunden und Details weit unter 200 Nanometern sichtbar gemacht. Die meisten dieser Methoden funktionieren jedoch nur in Proben nahe der Oberfläche gut. In dicken Geweben wie dem Mausgehirn werden sowohl das Licht zur Anregung der Fluorophore als auch das zum Detektor zurückkehrende Licht durch kleine Variationen in der Gewebestruktur verzerrt. Diese Verzerrungen, Aberrationen genannt, verwischen den Fokus des Mikroskops und löschen hochauflösende Informationen aus—insbesondere in Tiefen größer als einige Dutzend Mikrometer.
Von Hardware-Lösungen zu einer Softwarestrategie
Eine verbreitete Methode zur Bekämpfung von Aberrationen ist die hardwarebasierte adaptive Optik, bei der bewegliche Spiegel oder andere Bauteile die Lichtwellenfront umformen, um den scharfen Fokus wiederherzustellen. Zwar leistungsfähig, sind diese Systeme teuer, technisch anspruchsvoll und korrigieren oft nur für eine Farbe oder eine Richtung des Lichtwegs zugleich. Die Autoren schlagen stattdessen einen rechnerischen Ansatz vor, der mit einer in vielen Laboren bereits verbreiteten Mikroskopieform funktioniert: dem laserabgetasteten Multiphotonen-Mikroskop. Indem sie den üblichen einzelnen Lichtdetektor durch eine Kamera ersetzen, zeichnen sie einen reichen Stapel abgetasteter Bilder auf, der codiert, wie sowohl das einfallende Anregungslicht als auch die ausgehende Fluoreszenz vom Gewebe verzerrt wurden.
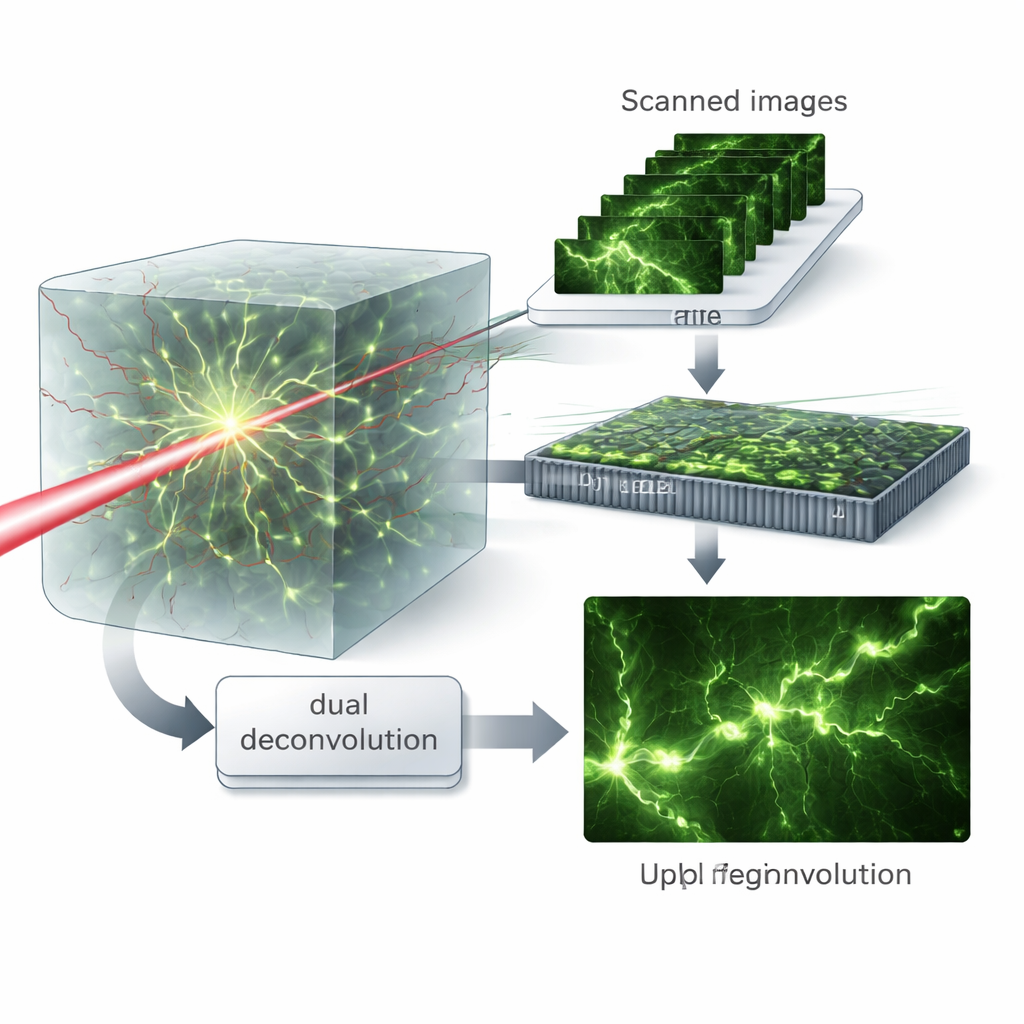
Virtuelle Muster und doppelte Bereinigung
Die zentrale Erkenntnis besteht darin, die abgetasteten Bilder so zu behandeln, als sei die Probe mit vielen verschiedenen feinen Lichtmustern beleuchtet worden—ein Konzept, das die Autoren virtuelle strukturierte Beleuchtung nennen. Das mathematische Neukombinieren dieser Daten im Frequenzbereich erlaubt es, die Rollen von Anregungs- und Emissionsprozessen zu trennen. Anschließend führen sie einen „dualen Dekonvolutions“-Algorithmus ein, der abwechselnd die Verwischung von beiden Seiten schätzt und korrigiert—das einfallende Licht und das austretende Licht—anstatt sie zu einer einzigen effektiven Unschärfe zusammenzufassen. Diese matrixbasierte Behandlung bewahrt mehr hochfrequente Details und ermöglicht es dem Algorithmus, feine Strukturen selbst bei starken Aberrationen wiederherzustellen.
Scharfere Ansichten in Simulationen und realen Proben
Um ihre Methode zu prüfen, nutzte das Team zunächst Computersimulationen der Zweiphotonen-Mikroskopie, einer Tiefenbildgebungstechnik, die Paare niederenergetischer Photonen verwendet, um Fluoreszenz nur im Fokuspunkt anzuregen. Unter starken simulierten Verzerrungen lieferten konventionelle Zweiphotonen- und standardmäßige strukturierte Beleuchtungs-Rekonstruktionen merklich verschwommene Bilder. Im Gegensatz dazu stellte die duale Dekonvolution klare Muster wieder her, deren Auflösung sich der Viertellänge der Fluoreszenzwellenlänge näherte—etwa 130 Nanometer—und damit den theoretischen Erwartungen entsprach. Die Autoren bauten anschließend eine kundenspezifische Zweiphotonen-Anordnung mit einer wissenschaftlichen Kamera und wandten ihren Algorithmus auf reale Proben an, darunter fluoreszierende Kügelchen, Testmuster hinter streuenden Schichten, kultivierte Zellen, Mausgewebe und ganze Zebrafische. Immer wieder traten Strukturen, die in konventionellen Bildern verschmiert oder doppelt erschienen, nach der Verarbeitung als klar getrennte Merkmale hervor, und feine neuronale Elemente wie dendritische Dornen blieben in Tiefen bis zu 180 Mikrometern im Mausgehirn auflösbar.
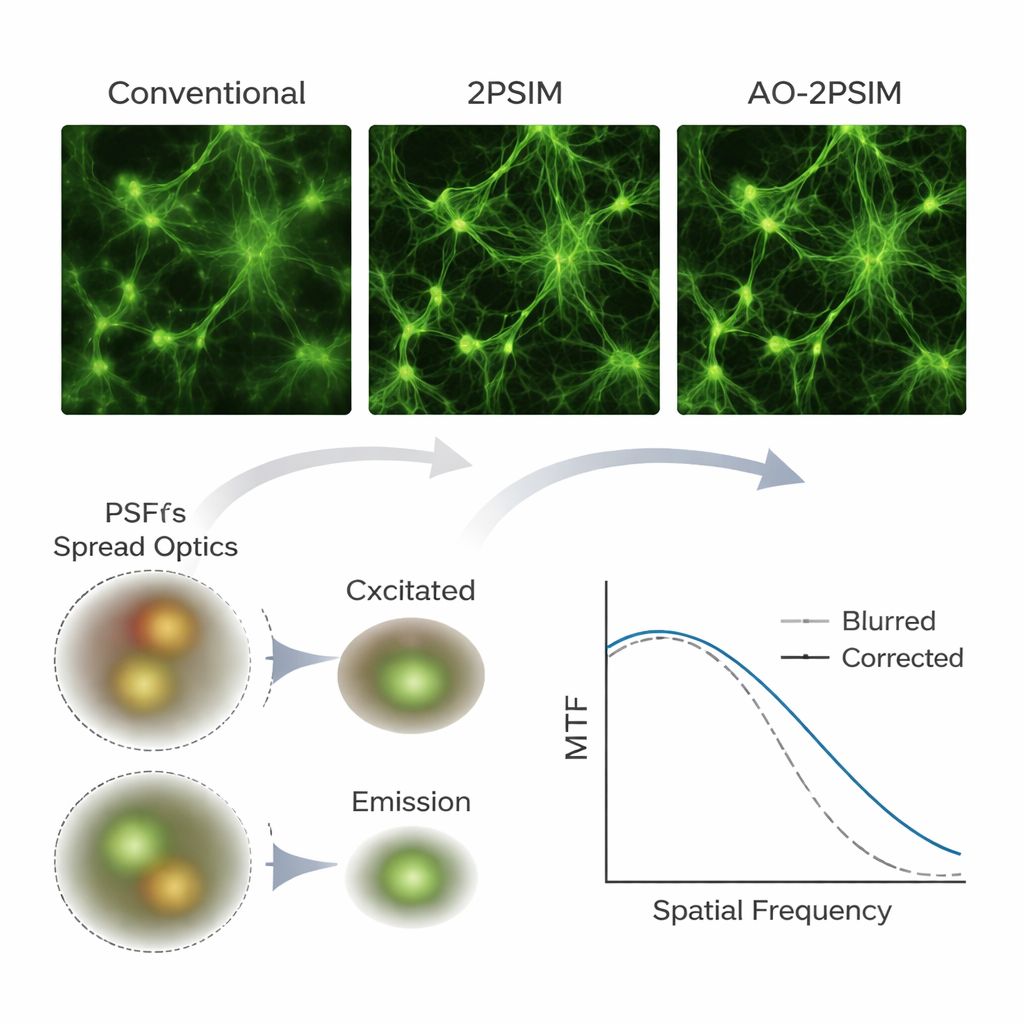
Was das für die biologische Bildgebung bedeutet
Für Nicht-Spezialisten lautet die Hauptbotschaft: Die Autoren haben gezeigt, wie sich vorhandene Multiphotonen-Mikroskope vor allem durch Software und ein Kamerauprade zu deutlich mächtigeren Werkzeugen für die Tiefengewebe-Bildgebung machen lassen. Durch sorgfältiges Modellieren und Korrigieren der Lichtumlenkung im Gewebe sowohl auf dem Hin- als auch auf dem Rückweg verdoppelt ihr dualer Dekonvolutionsansatz die übliche Auflösungsgrenze in herausfordernden, dicken Proben, ohne auf komplexe adaptive Spiegel angewiesen zu sein. Zwar hängt die Methode weiterhin davon ab, genügend Signal zu sammeln, und erfordert derzeit relativ langsames Abtasten, doch bietet sie einen praktischen, kosteneffizienten Weg zu routinemäßig ultrahochaufgelösten 3D-Ansichten von Gehirn und anderen Organen und ebnet den Weg für detailliertere Studien darüber, wie biologische Strukturen organisiert sind und sich im Laufe der Zeit verändern.
Zitation: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Schlüsselwörter: Superauflösungsmikroskopie, Zweiphotonen-Bildgebung, Adaptive Optik, Tiefengewebe-Bildgebung, Computational Imaging