Clear Sky Science · de
Zwei Typen axonaler muskarinerger Acetylcholinrezeptoren vermitteln die Bildung des Speichel-Cocktails bei der Zecke Ixodes ricinus
Warum Zeckenspeichel wichtig ist
Zecken sind mehr als nur lästige, juckende Tiere. Beim Blutsaugen injizieren sie eine komplexe Mischung aus Flüssigkeiten und Proteinen in unsere Haut, die den Blutfluss aufrechterhält, das Immunsystem dämpft und gefährlichen Mikroben helfen kann, in den Körper zu gelangen. Diese Arbeit erklärt, wie eine in Europa verbreitete Zeckenart, Ixodes ricinus, diesen Speichel‑„Cocktail“ während einer langen Blutmahlzeit präzise abstimmt. Indem die Autoren ein bislang verborgenses, nervenbasiertes Kontrollsystem aufdecken, zeigen sie neue verwundbare Stellen, die eines Tages genutzt werden könnten, um sowohl das Zeckenfüttern als auch die Übertragung von Krankheitserregern zu unterbinden.
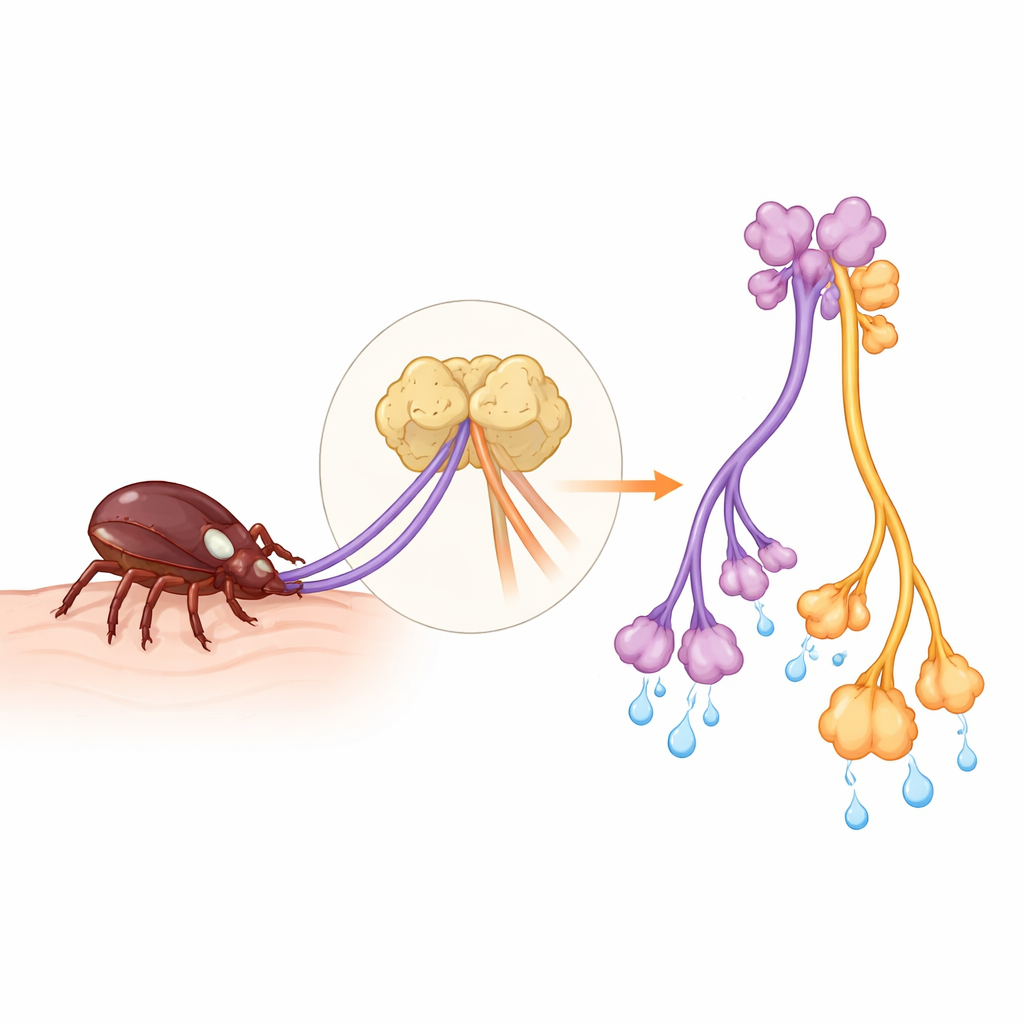
Zwei Regelknöpfe an Zeckennerven
Die Studie konzentriert sich auf einen vertrauten Hirnchemikalie, Acetylcholin, das beim Menschen alles von Herzschlag bis Verdauung steuert. Auch Zecken nutzen Acetylcholin, doch lange Zeit war nur bekannt, dass ein Wirkstoff namens Pilocarpin sie im Labor zum Speicheln bringt. Das natürliche, in‑Zecke vorhandene Kontrollsystem blieb rätselhaft. Die Forscher durchsuchten Zeckengenome und fanden zwei verschiedene Typen von acetylcholin‑empfindlichen Schaltern, sogenannte muskarinerge Rezeptoren, die an den langen Nervenzellfortsätzen (Axonen) sitzen, die vom zentralen Nervengewebe zu den Speicheldrüsen führen. Sie bezeichnen diese beiden Arten als Typ A und Typ B. Beide reagieren auf Acetylcholin, reagieren aber sehr unterschiedlich auf viele Wirkstoffe; Typ B zeigt ein ungewöhnliches, „nicht‑mammalisches“ Profil und stellt damit ein auf Wirbellose spezialisiertes Ziel dar.
Kartierung des Nervennetzes für Zeckenspeichel
Mithilfe fluoreszenzmarkierter Antikörper und hochauflösender Elektronenmikroskopie verfolgte das Team, wo diese beiden Rezeptortypen lokalisiert sind. Im zentralen Nervengewebe senden spezifische Gruppen von hormonfreisetzenden Nervenzellen Axone in den Drüsenbereich, und verschiedene Gruppen tragen entweder Typ‑A‑ oder Typ‑B‑Rezeptoren. Innerhalb der Speicheldrüsen selbst ist das Bild noch komplexer. Ein Ast von Axonen mit Typ‑A‑Rezeptoren zieht hauptsächlich in einen Acinus‑Typ (eine kleine sekretorische Einheit), der reich an proteingefüllten Zellen ist. Ein anderer Ast, der mit Typ‑B‑Rezeptoren bestückt ist, erreicht sowohl diesen proteinreichen Acinus‑Typ als auch einen zweiten Acinus‑Typ, der auf Flüssigkeitsproduktion spezialisiert ist. Die beiden Axonsysteme treffen nur in den proteinreichen Einheiten aufeinander, besetzen dort jedoch getrennte Zonen, was auf komplementäre Rollen bei der Steuerung von Zeitpunkt und Art der Sekretion hindeutet.
Eine lokale Chemiefabrik in den Drüsen
Die Wissenschaftler fragten dann, woher das Acetylcholin stammt, das diese Rezeptoren antreibt. Chemische Messungen zeigten, dass die Speicheldrüsen selbst höhere Acetylcholinwerte aufweisen als das zentrale Nervengewebe und dass diese Werte während der Nahrungsaufnahme ansteigen. Die Drüsen enthalten außerdem die genetischen Informationen für das Enzym, das Acetylcholin herstellt, und für den Transporter, der es in sekretorische Vesikel lädt. Zusammengenommen deutet dies darauf hin, dass Drüsenzellen als lokale Acetylcholinfabrik wirken und nahegelegene Nervenendigungen mit dem Neurotransmitter versorgen, anstatt sich ausschließlich auf Signale von weit entfernten Nervenzellkörpern zu verlassen. Als Reaktion darauf können die Axone mit Typ‑A‑ und Typ‑B‑Rezeptoren eigene Neuropeptide in den Blutraum und auf Drüsenzellen freisetzen und so lokale chemische Signale mit dem gesamten Flüssigkeitshaushalt und der Drüsenaktivität verknüpfen.
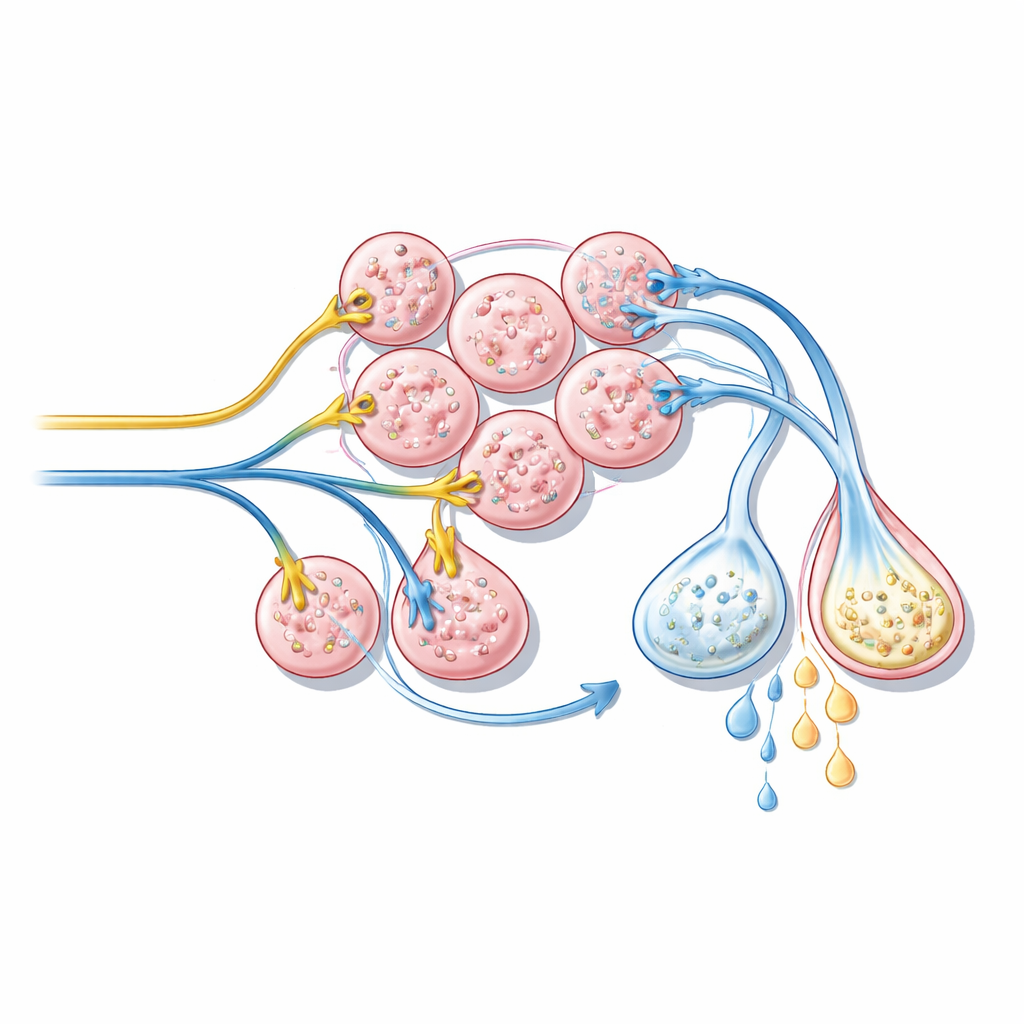
Wie zwei Schalter den Speichel‑Cocktail formen
Um zu sehen, was diese Rezeptoren tatsächlich bewirken, injizierte das Team teilweise gesaugte Zecken mit verschiedenen Wirkstoffen, die die Rezeptoren entweder aktivieren oder blockieren, und sammelte anschließend den resultierenden Speichel zur Analyse. Breite Aktivatoren beider Rezeptortypen lösten die größten Speichelmengen aus. Wirkstoffe, die hauptsächlich Typ‑A‑Rezeptoren ansprachen, führten weiterhin zu starker Flüssigkeitssekretion, während Bedingungen, unter denen nur Typ B aktiv blieb, viel kleinere Volumina ergaben, aber Speichel, der proteinreicher war. Detaillierte Proteinprofile zeigten, dass das allgemeine „Menü“ der Speichelproteine über die Bedingungen hinweg ähnlich ist, aber ihre relativen Mengen sich je nach dem treibenden Rezeptortyp verschieben. Zusammen deuten die Ergebnisse darauf hin, dass Typ A der Haupttreiber des Flüssigkeitsflusses ist, während Typ B die Freisetzung und das Ausspülen von Proteinbestandteilen feinabstimmt.
Was das für die Zeckenbekämpfung bedeutet
Alltäglich formuliert zeigt diese Arbeit, dass die Speichelproduktion der Zecke von zwei zusammenarbeitenden, nervenbasierten Schaltern gesteuert wird: einem, der den Hahn öffnet, und einem, der das Mischungsverhältnis und den Zeitpunkt des Ausspülens reguliert. Da Typ‑B‑Rezeptoren ein pharmakologisches Profil aufweisen, das sich deutlich von bekannten Säugetierrezeptoren unterscheidet, stellen sie ein besonders attraktives Ziel für neue, zeckenspezifische Wirkstoffe oder Impfstoffe dar. Eine Störung dieses Zwei‑Schalter‑Systems könnte Zecken daran hindern, ihren Speichel‑Cocktail zu kontrollieren, wodurch es für sie schwieriger würde, erfolgreich zu saugen und die Erreger zu übertragen, die Lyme‑Borreliose und andere Infektionen verursachen.
Zitation: Nìng, C., Valdés, J.J., Mateos-Hernández, L. et al. Two types of axonal muscarinic acetylcholine receptors mediate formation of saliva cocktail in the tick Ixodes ricinus. Nat Commun 17, 2867 (2026). https://doi.org/10.1038/s41467-026-68654-3
Schlüsselwörter: Zeckenspeichel, Acetylcholinrezeptoren, Ixodes ricinus, Vektor-Wirt-Interaktionen, Regulation der Speicheldrüse