Clear Sky Science · de
Dapagliflozin reguliert die Homöostase von Chondrozyten und schützt vor Osteoarthritis über die Ziele AMPKα und SGLT2
Neue Hoffnung für schmerzende Gelenke
Osteoarthritis ist eine führende Ursache für Schmerzen und Behinderungen, doch die meisten derzeitigen Behandlungen dämpfen nur den Schmerz, ohne den Verschleiß im Gelenk zu verlangsamen. Diese Studie untersucht, ob Dapagliflozin, eine bereits bei Typ‑2‑Diabetes eingesetzte Tablette, den glatten Knorpel, der unsere Gelenke polstert, schützen kann, und zeigt, wie es auf die Zellen wirkt, die dieses Gewebe aufbauen und erhalten.
Wie Gelenkknorpel verschleißt
In gesunden Gelenken balancieren Knorpelzellen ständig den Aufbau und den Abbau der Knorpelmatrix, die Knie und Hüften ihre glatte Gleitfähigkeit verleiht. Bei Osteoarthritis geht dieses Gleichgewicht verloren: Entzündliche Signale und Stress drängen die Zellen in einen überaktiven Abbaumodus, während die Neubildung von Knorpel langsamer erfolgt. Im Laufe der Zeit wird der Knorpel dünner, der darunterliegende Knochen versteift und schmerzhafte knöcherne Auswüchse können entstehen. Die Autoren konzentrierten sich auf diese Knorpelzellen, die von Menschen mit und ohne Osteoarthritis entnommen wurden, sowie auf ein gut etabliertes Mausmodell einer Gelenkverletzung, um zu prüfen, ob Dapagliflozin das System wieder ins Gleichgewicht bringen kann.
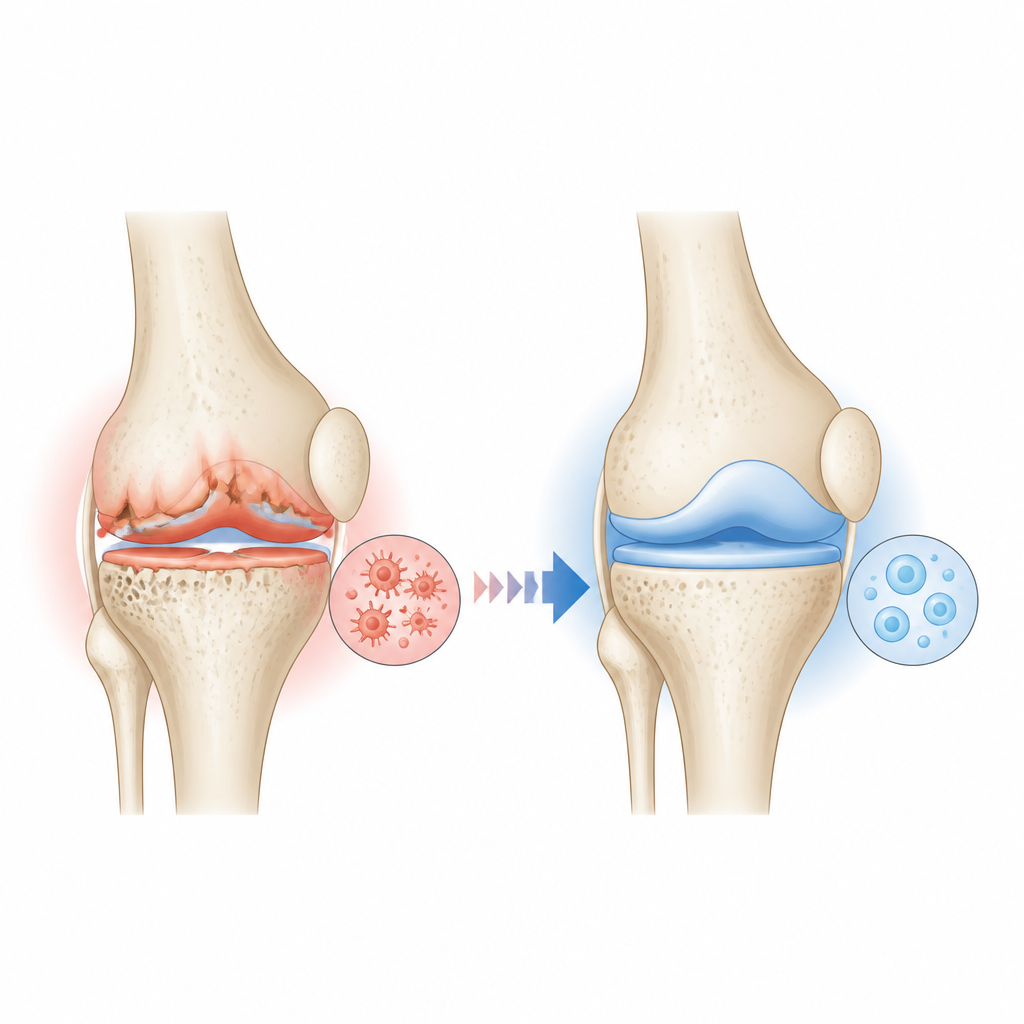
Ein Diabetesmittel, das gestresste Knorpelzellen beruhigt
In Zellkulturen menschlicher Knorpelzellen, die starken entzündlichen Signalen ausgesetzt waren, reduzierte Dapagliflozin Marker, die mit Abbau und Entzündung verbunden sind, und steigerte zugleich Gene und Proteine, die an Knorpelaufbau beteiligt sind. Dasselbe Muster zeigte sich, wenn Knorpelzellen und -gewebe von Menschen mit Osteoarthritis untersucht wurden: Höhere Dosen des Medikaments verringerten entzündliche und zerstörerische Moleküle und erhöhten wichtige strukturelle Komponenten des Knorpels. Färbemethoden, die die Knorpelmatrix sichtbar machen, zeigten, dass mit Dapagliflozin behandelte Zellen über Tage hinweg mehr ihres schützenden Materials behielten, was auf eine nachhaltige Verhaltensänderung der Zellen statt auf einen kurzlebigen Effekt hindeutet.
Schutz in verletzten Mäuseknien
Das Team wandte sich dann Mäusen zu, deren Kniebänder chirurgisch verändert wurden, um osteoarthritisähnliche Schäden auszulösen. Tiere, die nach der Operation oral Dapagliflozin erhielten, behielten dichteren, geordneteren Knorpel mit mehr Knorpelzellen und entwickelten weniger knöcherne Fortsätze im Vergleich zu unbehandelten Mäusen. Der darunterliegende Knochen, der bei Fortschreiten der Erkrankung typischerweise abnormal dick und dicht wird, sah bei den behandelten Tieren ebenfalls gesünder aus. Wichtig ist, dass das Medikament bei diesen sonst gesunden Mäusen das Körpergewicht oder den Blutzucker nicht signifikant veränderte, was auf eine direkte Wirkung am Gelenk selbst und nicht auf einen indirekten Nutzen durch Stoffwechselveränderungen hindeutet.
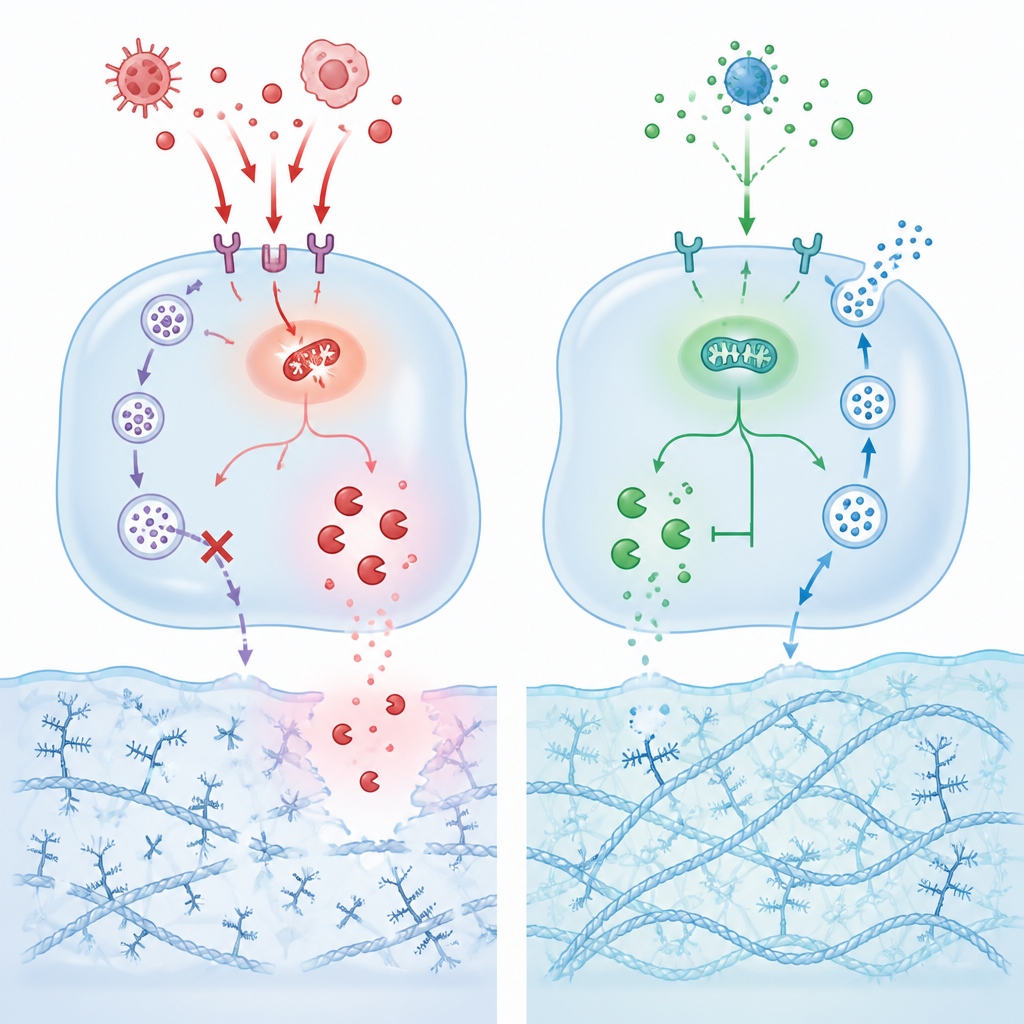
Wiederherstellung von Energie‑ und Aufräumsystemen der Zelle
Um zu klären, wie Dapagliflozin innerhalb von Knorpelzellen wirkt, analysierten die Forscher die globale Genaktivität und zentrale Signalumschalter. Sie fanden heraus, dass das Medikament AMPK aktiviert, einen zentralen Energiesensor in Zellen, und MAPK‑Wege dämpft, die Entzündung und Schäden fördern. Ungewöhnlich war, dass Dapagliflozin AMPK nicht durch Energie‑Stress aktivierte; stattdessen band es direkt an die AMPK‑Alpha‑Untereinheit und steigerte deren Aktivität, womit ein neues direktes Ziel aufgedeckt wurde. Gleichzeitig blockierte das Medikament die Wirkung von SGLT2, einem Transporterprotein, das in osteoarthritischem Knorpel in höheren Mengen vorhanden war und das bei Überaktivität Entzündungen fördert, den Recyclingprozess der Zellen (Autophagie) hemmt und Signale verstärkt, die dieses Aufräumen unterdrücken.
Zwei Ziele, die zusammenwirken
Durch selektive Reduktion von AMPK und SGLT2 in Knorpelzellen zeigten die Autoren, dass die knorpelschützenden Effekte von Dapagliflozin auf beiden beruhen. Seine Fähigkeit, den Zellen beim Aufbau von Knorpel zu helfen, erforderte AMPK, während die beruhigende Wirkung auf Entzündungen sowohl von AMPK als auch von SGLT2 abhängte. Die Blockade von SGLT2 oder die Nachahmung einer AMPK‑Aktivierung milderte die schädliche Aktivierung von MAPK und eines Wachstumswegs namens mTORC1 und stellte die Recycling‑Maschinerie wieder her, die gestressten Zellen beim Überleben hilft. Auf diese Weise wirkt Dapagliflozin wie ein Koordinator: Es schaltet direkt einen schützenden Energiesensor ein und dämpft gleichzeitig einen Transporter, der Zellen in Richtung Schädigung treibt.
Was das für Menschen mit Arthritis bedeuten könnte
Für Menschen mit Osteoarthritis deuten diese Befunde darauf hin, dass ein bereits klinisch weit verbreitetes Diabetesmedikament eines Tages helfen könnte, Gelenkknorpel zu schützen und nicht nur Schmerzen zu kaschieren. In Laborzellen und Mausgelenken verschob Dapagliflozin die Knorpelzellen zurück zu einem gesünderen Gleichgewicht von Aufbau und Abbau, reduzierte schädliche Entzündungen und belebte interne Aufräumsysteme, indem es gleichzeitig auf AMPK und SGLT2 wirkte. Während klinische Studien beim Menschen erforderlich sind, um Sicherheit, Dosierung und den tatsächlichen Nutzen bei Menschen mit schmerzenden Knien und Hüften zu prüfen, weist die Arbeit auf eine Zukunft hin, in der die gezielte Beeinflussung von Zellenergie und Recycling ein neuer Weg sein könnte, das Fortschreiten der Osteoarthritis zu verlangsamen.
Zitation: Liu, K., Li, Z., Wang, C. et al. Dapagliflozin regulates chondrocyte homeostasis and protects against osteoarthritis via targets AMPKα and SGLT2. Cell Death Discov. 12, 217 (2026). https://doi.org/10.1038/s41420-026-03016-y
Schlüsselwörter: Osteoarthritis, Knorpel, Dapagliflozin, AMPK, SGLT2