Clear Sky Science · de
Ein STAT3‑Degrader zeigt Wirksamkeit bei venetoclaxresistentem akuten myeloischen Leukämie
Warum Medikamentenresistenz bei Blutkrebs wichtig ist
Für Menschen mit akuter myeloischer Leukämie (AML), einer rasch fortschreitenden Krebserkrankung von Blut und Knochenmark, haben neue Therapien die frühen Ansprechraten verbessert, aber nicht das Langzeitüberleben. Ein weit verbreitet eingesetztes Medikament, Venetoclax, kann die Erkrankung in Remission bringen, doch viele Patientinnen und Patienten erleiden später einen Rückfall, weil die Krebszellen Wege finden, die Behandlung zu umgehen. Diese Studie untersucht, wie dieses Entkommen zustande kommt, und testet eine neue Wirkstoffklasse, die einen zentralen Überlebensschalter in Leukämiezellen demontieren soll — ein möglicher Weg für Patienten, die derzeit wenige Optionen haben.
Ein mächtiger Schalter, der kranke Blutzellen antreibt
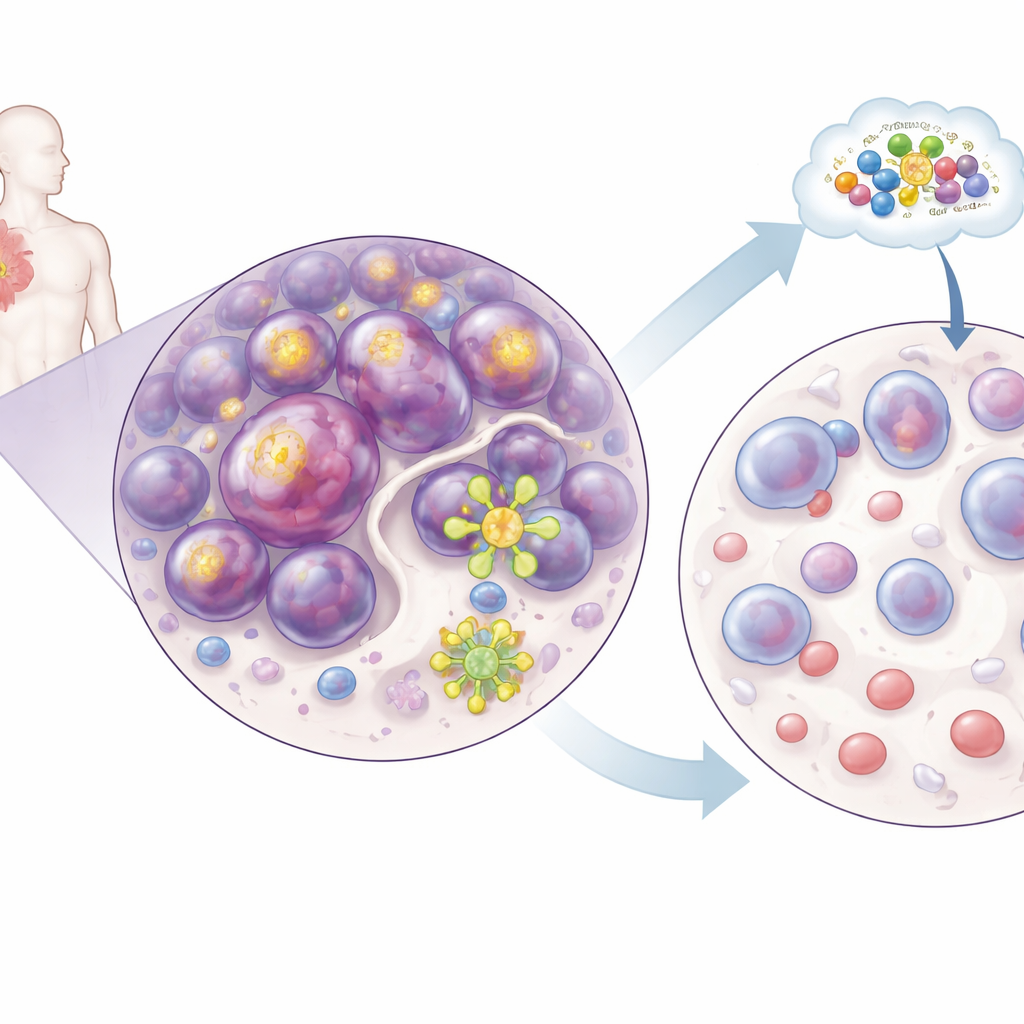
Die Forschenden konzentrierten sich auf ein Protein namens STAT3, das wie ein Ein‑/Ausschalter für viele Gene wirkt, die das Wachstum und Überleben von Blutzellen steuern. Wenn STAT3 ungewöhnlich aktiv ist, treibt es unreife Blutzellen zur Vermehrung und macht sie unempfindlich gegen normale Todes‑Signale. An genetisch veränderten Mäusen, deren blutbildende Zellen eine ständig aktive Form von STAT3 produzieren, zeigte das Team, dass STAT3 allein eine myeloische Bluterkrankung antreiben kann, die der menschlichen AML sehr ähnlich ist. Diese Mäuse entwickelten vergrößerte Milz und Leber, die mit unreifen weißen Blutkörperchen gefüllt waren, sowie eine starke Verlagerung hin zur Produktion myeloider Zellen statt eines gesunden, ausgewogenen Bluts. Damit etablierten die Autorinnen und Autoren STAT3 nicht nur als Beiwerk, sondern als direkten Motor der Leukämie.
Wie Venetoclax‑Resistenz die Kraftwerke der Zelle kapert
Venetoclax wirkt, indem es BCL2 blockiert — ein Protein, das beschädigte Zellen am Absterben hindert. Im Laufe der Zeit allerdings schwenken überlebende Leukämiezellen häufig auf andere Ersatzproteine und Signalwege um. Das Team fand heraus, dass in Zelllinien mit Venetoclax‑Resistenz die STAT3‑Spiegel stark anstiegen, zusammen mit seinem Partner MCL1, einem weiteren starken Schutzfaktor gegen Zelltod. Detaillierte Patientendaten von Hunderten Menschen, die mit Venetoclax‑haltigen Regimen behandelt wurden, zeigten, dass jene mit höheren Mengen aktivierten STAT3 in ihren Leukämiezellen kürzere Remissionen und ein schlechteres Gesamtüberleben hatten — unabhängig von Alter oder Behandlungs‑Kombination. In resistenten Zellen und Patientenproben war besonders eine Form von STAT3 vermehrt, die in den Mitochondrien — den Energiestationen der Zelle — lokalisiert ist; sie war mit aufgeblähten, deformierten Innenfalten der Mitochondrien verbunden, was auf gestörten und umgestellten Energiestoffwechsel hinweist.
STAT3 zerlegen statt nur blockieren
Da traditionelle STAT3‑Inhibitoren klinisch wenig Erfolg hatten, wandten sich die Forschenden einer neueren Strategie zu: dem zielgerichteten Proteinabbau. Anstatt STAT3 lediglich in seiner Aktivität zu hemmen, markieren kleine "Degrader"‑Moleküle STAT3 physisch zur Entsorgung durch die zelluläre Recycling‑Maschinerie. In Venetoclax‑resistenten AML‑Zelllinien entfernten zwei experimentelle Degrader, KTX‑201 und KTX‑105, STAT3 und dessen aktivierte Formen effizient, ohne verwandte Proteine zu beeinflussen. Das löste starken Zelltod aus, verringerte die Abhängigkeit der Leukämiezellen von MCL1 und normalisierte teilweise Mitochondrienstruktur und ‑funktion. In Zellen von AML‑Patientinnen und ‑Patienten mit Venetoclax‑Resistenz beseitigten die Degrader STAT3 und förderten die Reifung unreifer Krebszellen zu eher normalen roten und weißen Blutzellen, während gesunde Spenderzellen kaum beeinträchtigt wurden — ein Hinweis auf Selektivität gegenüber kranken Stamm‑ und Vorläuferzellen.
Beschädigte Mitochondrien reparieren und Tests in lebenden Modellen
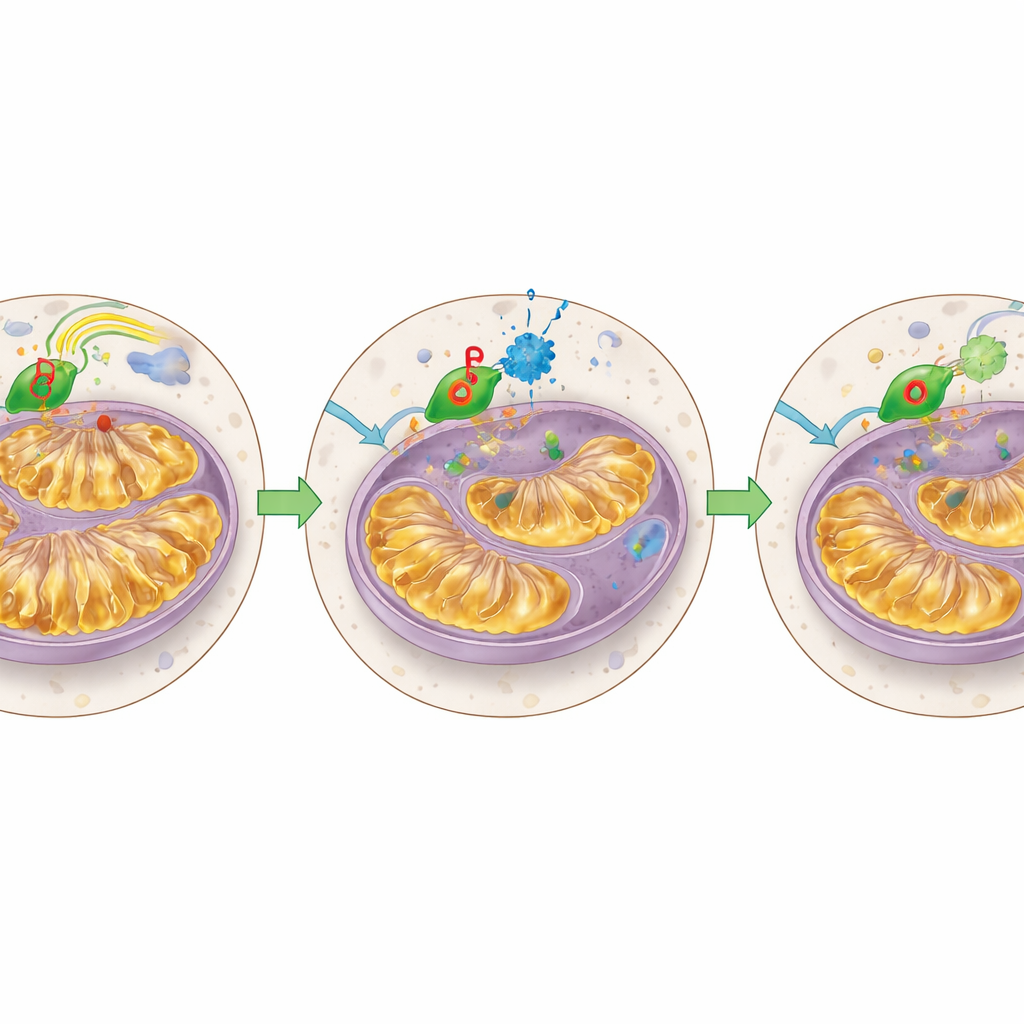
Bei näherer Untersuchung der Mitochondrien zeigten die Forschenden, dass STAT3‑Degrader die Menge an mitochondrialem STAT3 reduzierten, die abnorme Ausweitung der Innenfalten minderten und die Energieproduktion wieder in einen normaleren Zustand verschoben. Venetoclax‑resistente Zellen hatten ihre Mitochondrien „auf Hochtouren“ betrieben — hohe Energieproduktion, aber kaum Reservekapazität für Stress; die Behandlung mit Degradern dämpfte diese Überaktivität. Anschließend testete das Team die Wirkstoffe in Mäusemodellen, die entweder Venetoclax‑resistente Leukämiezelllinien oder patientenabgeleitete resistente AML‑Zellen trugen. In diesen Tieren senkte ein klinisch fortgeschrittener Degrader namens KT‑333 STAT3‑ und MCL1‑Spiegel in den Leukämiezellen deutlich, verkleinerte den Pool unreifer, leukämieinitiierender Zellen im Knochenmark und verlängerte das Überleben im Vergleich zu unbehandelten Mäusen signifikant.
Was das für die zukünftige AML‑Behandlung bedeutet
In der Summe deuten die Ergebnisse darauf hin, dass Venetoclax‑Resistenz bei AML eng mit einem überaktiven STAT3‑Signalweg verbunden ist, der sowohl die Genaktivität als auch das mitochondriale Verhalten umgestaltet, um Leukämiezellen am Leben zu erhalten. Durch selektives Entfernen von STAT3 können Degrader‑Medikamente diesen Fluchtweg abschneiden, die mitochondriale Struktur normalisieren, Krebszellen in Richtung Zelltod oder Reifung treiben und in präklinischen Modellen die Ergebnisse verbessern. Für Patientinnen und Patienten, deren Erkrankung nicht mehr auf aktuelle Therapien anspricht, könnten STAT3‑Degrader wie KT‑333 einen neuen, mutationsunabhängigen Ansatz bieten, die zugrunde liegende Überlebensmaschinerie resistenter Leukämiezellen anzugreifen — und sie gehen bereits in frühe klinische Prüfungen.»}
Zitation: Chakraborty, S., Morganti, C., Zaldana, K. et al. A STAT3 degrader demonstrates efficacy in venetoclax resistant acute myeloid leukemia. Leukemia 40, 717–729 (2026). https://doi.org/10.1038/s41375-026-02883-9
Schlüsselwörter: akute myeloische Leukämie, venetoclax‑Resistenz, STAT3‑Degrader, mitochondriale Dysfunktion, zielgerichteter Proteinabbau