Clear Sky Science · ar
إعادة تشكيل ميكروبيوم الأمعاء بواسطة المضادات الحيوية يقلل الالتهاب العصبي بعد إصابة دماغية رضّية
لماذا الأمعاء مهمة بعد إصابة في الرأس
عندما نفكر في الارتجاجات أو الإصابات الدماغية الرضّية، عادة ما نتصور أضراراً داخل الجمجمة. لكن هذه الدراسة تُظهر أن ما يحدث في الأمعاء يمكن أن يحدد إلى حد كبير طريقة شفاء الدماغ. عبر إعادة تشكيل مؤقتة لتكوين الميكروبات المعوية باستخدام المضادات الحيوية، وجد الباحثون أنهم قادرون فعلياً على تقليل أضرار والتهاب الدماغ بعد إصابة بالرأس في الفئران، مما يكشف عن مسار غير متوقع لحماية الدماغ.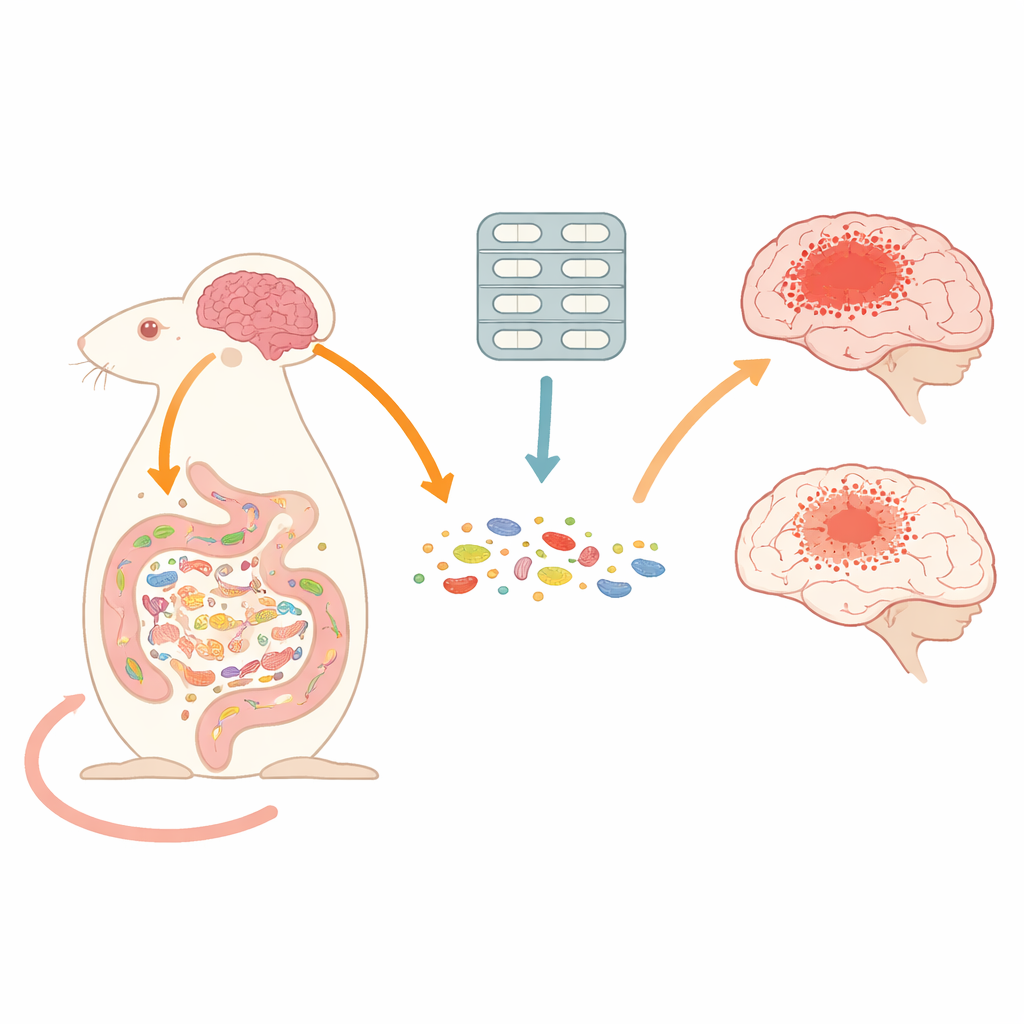
إعادة محاكاة إصابة الرأس واضطراب الأمعاء في الفئران
استخدم الفريق نموذجاً معتمداً للإصابة الدماغية الرضّية في ذكور الفئران، إذ قدّموا إما ضربة محكومة واحدة أو ضربتين تفصل بينهما أكثر من شهر لمحاكاة الإصابات المتكررة. بعض الفئران تلقت ماءً فقط، بينما أعطيت أخرى مزيجاً عن طريق الفم من مضادات حيوية واسعة الطيف لمدة ثلاثة أيام، شبيهاً بالأدوية المستخدمة في وحدات العناية المركزة. ثم قاس العلماء تلف الدماغ، ووظيفة الحركة، ونشاط الخلايا المناعية في الدماغ، والتغيرات المفصّلة في ميكروبات الأمعاء ومنتجاتها الكيميائية. كما درسوا فئراناً خالية من الجراثيم رُبّيت بالكامل بدون ميكروبات للنظر كيف يؤثر الغياب التام للميكروبيوم على تعافي الدماغ.
المضادات الحيوية تقلل تلف الدماغ لكنها تأتي بتكاليف
رغم أنها أضرت بشدة بالميكروبيوم المعوي، فقد جعلت المعالجة قصيرة الأمد بالمضادات الحيوية الإصابات الدماغية أقل حدة. الفئران التي تعرّضت لضربتين في الرأس ولم تتلق مضادات حيوية طورت أكبر آفات دماغية، وموتاً خلوياً أكثر، ونشاطاً قوياً لخلايا مناعية تسمى الميكروغليا والخلايا النجمية والبلعميات المخترقة. بالمقابل، كانت آفات الفئران المصابة التي تلقت مضادات حيوية أصغر حجماً، وعدد الخلايا الميتة أقل في القشرة والمهاد، ونشاط هذه الخلايا المناعية في الدماغ أخف. كما أظهرت غزو أقل للخلايا المناعية المحيطية إلى الدماغ. بقي الأداء الحركي متراجعاً بعد الإصابة المتكررة، لكن تلف نسيج الدماغ وإشارات الالتهاب انخفضت بوضوح بعد دورة المضادات الحيوية.
كيف أعيد تشكيل الميكروبيوم وموادّه الكيميائية
لم تخرج ميكروبات الأمعاء من التجربة سالمة. قللت المضادات الحيوية بشكل حاد من الحمض النووي البكتيري في البراز وأعادت تشكيل تنوّع الميكروبات، خصوصاً بعد الإصابة المتكررة. كل من الإصابة الدماغية الرضّية والمضادات الحيوية على حدة غيّرت مزيج الأنواع، ومعاً أحدثتا أكبر تغيير. انخفضت مستويات الأحماض الدهنية قصيرة السلسلة—جزيئات صغيرة تصنعها ميكروبات الأمعاء وتدعم غالباً الوظائف المضادة للالتهاب والحماية—في مجرى الدم لدى الفئران المعالجة بالمضادات الحيوية، لا سيما الحمض الدهني البيوتيرات. كشف التسلسل طويل القراءة للحمض النووي أن بعض الأنواع، مثل Parasutterella excrementihominis وLactobacillus johnsonii، صمدت أو توسعت رغم المعالجة، مما يوحي بأن ميكروبات مقاومة للمضادات أو مرنة تمتلك خصائص مهدئة للمناعة قد توازن فقدان أنواع أخرى.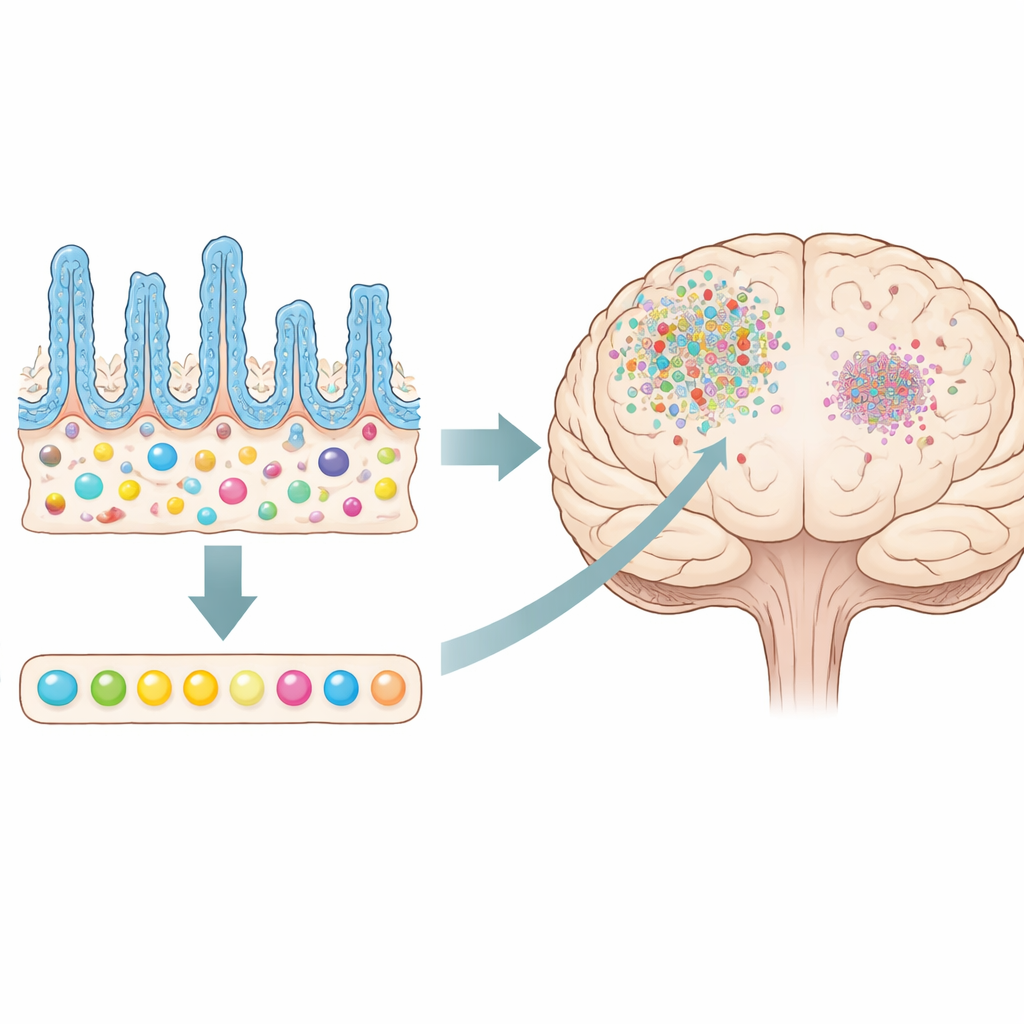
هيكل الأمعاء يتضرر، ومع ذلك يستفيد الدماغ
عند فحص الأمعاء مباشرة، لاحظ الباحثون أن الإصابة الدماغية الأسوأ ارتبطت بالزُغابات المعوية الأقصر وغير المنظمة وفقدان خلايا كوبليت المنتجة للمخاط الواقي. أدت المضادات الحيوية قصيرة الأمد إلى مزيد من التغير في هذا الطلاء المعوي المتعب أصلاً، مما أسفر عن زغابات أقصر، وتجاويف أضيق، وخلايا منتجة للمخاط أقل لدى الحيوانات التي تعرضت لإصابة شديدة وتلقت مضادات حيوية. بعبارة أخرى، بدا حاجز الأمعاء أكثر هشاشة، حتى بينما انخفض الالتهاب في الدماغ. هذا التباين يبرز أن تغييرات الميكروبيوم المدفوعة بالمضادات قد تفيد الدماغ بينما تفرض في الوقت ذاته تكلفة على صحة الأمعاء.
ماذا يحدث عندما لا توجد ميكروبات إطلاقاً؟
لفصل تأثير تعطيل الميكروبيوم عن غيابه التام، فحص الفريق فئراناً خالية من الجراثيم لم تُستوطن أبداً بالميكروبات. بعد إصابة الدماغ، أداء هذه الحيوانات كان أسوأ من الفئران العادية: كانت آفاتها أكبر، وكانت الميكروغليا والخلايا النجمية في الدماغ أكثر نشاطاً. هذا يشير إلى أن غياب الميكروبات مدى الحياة يحرم الجهاز المناعي والدماغ من إشارات "تدريب" مهمة لازمة للصمود. بالمقابل، يبدو أن تعطيل ميكروبيوم راسخ لفترة وجيزة بالمضادات الحيوية يخفّض مسارات التهابية معينة دون مسح كل الوظائف الميكروبية.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بشكل عام، تُظهر الدراسة أن الإصابة الدماغية الرضّية لا تضر الدماغ فحسب، بل تعطل أيضاً الأمعاء وسكانها الميكروبيين، وأن مجتمع الأمعاء بدوره يؤثر على الدماغ المصاب. دورة قصيرة من المضادات الحيوية واسعة الطيف في الفئران أعادت تشكيل الميكروبيوم، وخفتّت استجابات التهابية رئيسية، وحدت من فقدان نسيج الدماغ، رغم أنها خفضت المستقلبات الميكروبية المفيدة وساءت بعض ملامح الأمعاء. ونظراً للمخاطر الجسيمة المرتبطة بالاستخدام المطوّل أو المتكرر للمضادات الحيوية لدى البشر، لا يقترح المؤلفون المضادات الحيوية كعلاج بحد ذاتها. بل يرون أن فهم أي البكتيريا والطرق الميكروبية المرنة تخفف الالتهاب يمكن أن يلهم استراتيجيات قائمة على الميكروبيوم أكثر أماناً ومحددة—مثل بروبيوتيك مخصص أو مضادات ميكروبات دقيقة—لتحسين التعافي بعد صدمات الدماغ.
الاستشهاد: Flinn, H., Marshall, A., Holcomb, M. et al. Antibiotic-induced gut microbiome remodeling reduces neuroinflammation in traumatic brain injury. Commun Biol 9, 481 (2026). https://doi.org/10.1038/s42003-026-09737-1
الكلمات المفتاحية: إصابة دماغية رضّية, ميكروبيوم الأمعاء, المضادات الحيوية, الالتهاب العصبي, الأحماض الدهنية قصيرة السلسلة