Clear Sky Science · ar
البربيرين يعزز فعالية السيسبلاتين في سرطان إيرليش المائي عبر تعديل مسار الاستماتة والالتقماخ الخلوي
مركب نباتي يساعد العلاج الكيميائي على إصابة الأورام لا الأعضاء
يمكن أن تكون أدوية العلاج الكيميائي منقذة للحياة، لكنها غالبًا ما تضر الأعضاء السليمة وتفقد فعاليتها مع تكيف الخلايا السرطانية. تبحث هذه الدراسة فيما إذا كان البربيرين—مركب أصفر طبيعي يوجد في عدة نباتات طبية—يمكن أن يجعل دواء السرطان الشائع، السيسبلاتين، أكثر فعالية مع تخفيف آثاره الضارة. في نموذج فأري لسرطان بطني عدواني، طرح الباحثون سؤالًا بسيطًا له عواقب كبيرة: هل يمكن لجزيء نباتي أن يساعد العلاج القياسي على قتل المزيد من الخلايا السرطانية وحماية أكبر لجزء من الجسم؟
كيف يلتقي علاج تقليدي مع رعاية السرطان الحديثة
استُخدم البربيرين لقرون في الطب التقليدي ومعروف بالفعل بخصائصه المضادة للأكسدة والمضادة للالتهاب. في الآونة الأخيرة اهتم العلماء بكيفية تأثيره على نمو الخلايا وموتها، وهي عمليات مركزية في السرطان. أما السيسبلاتين، فهو دواء قوي يُستخدم في المستشفيات يسبب تلفًا في الحمض النووي للخلايا سريعة الانقسام، لكنه قد يضر أيضًا الكبد والكلى. استخدم الفريق فئرانًا حاملة لسرطان إيرليش المائي—ورم ينمو بسرعة ويملأ البطن بسائل سرطاني—ليرى كيف يؤثر البربيرين بمفرده، أو السيسبلاتين بمفرده، أو الاثنان معًا على نمو الورم والبقاء وصحة الأعضاء.
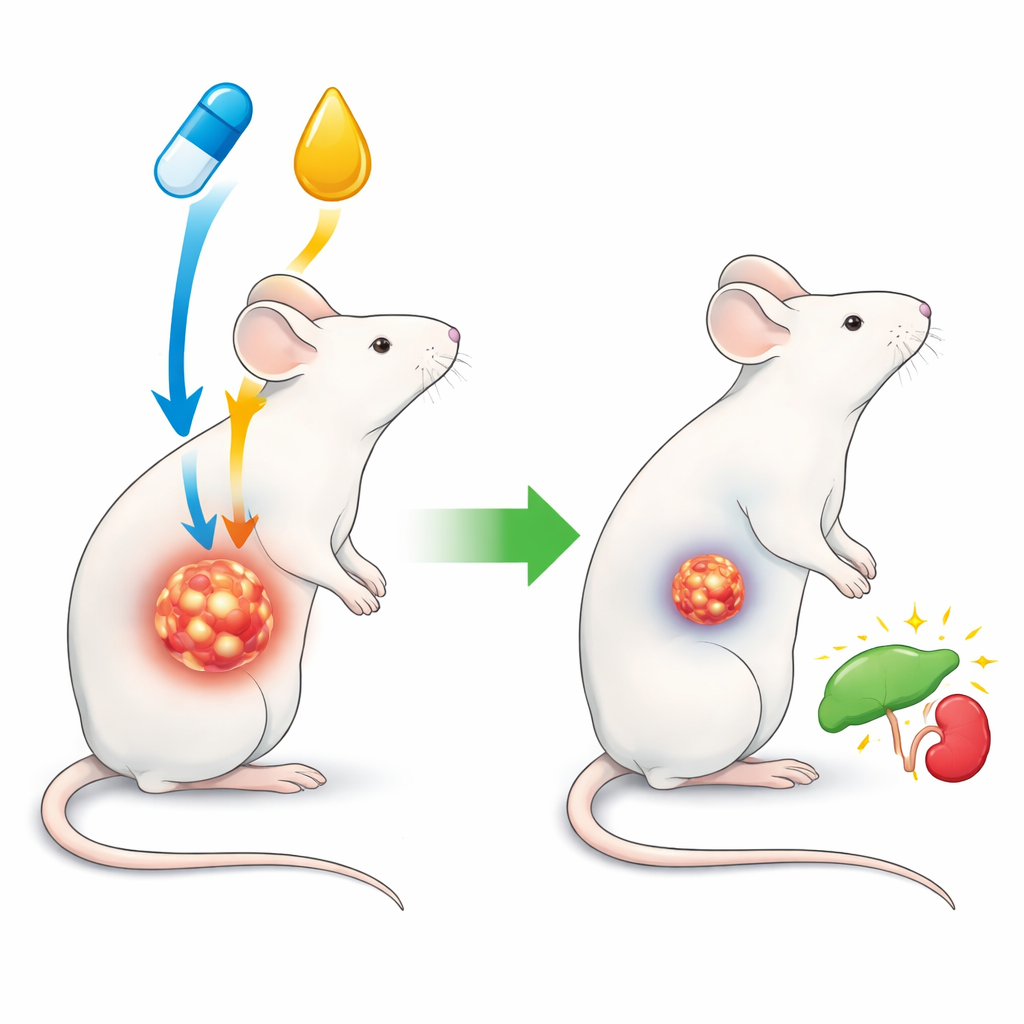
اختبار تراكيب علاجية مختلفة في الفئران
قُسمت ثمانون فأرًا إلى ثماني مجموعات، شملت ضوابط صحية وحيوانات حاملة للورم عولجت بالمالح أو البربيرين أو السيسبلاتين أو التركيبة معًا. على مدار 14 يومًا، راقب الباحثون وزن الجسم، وحجم السائل الورمي في البطن، وعدد خلايا الورم الحية والميتة، ومدة بقاء الفئران على قيد الحياة. كما قاسوا مؤشرات دم قياسية لوظائف الكبد والكلى، ومستويات جزيئات واقية وضارة مرتبطة بالإجهاد التأكسدي، وفحصوا نسيج الكبد مجهريًا. سمح هذا التصميم متعدد المستويات برؤية ليس فقط ما إذا كانت الأورام تنكمش، بل أيضًا كيف استجاب بقية الجسم.
مزيد من موت الورم، حياة أطول، وأذى أقل للأعضاء
أنتجت تركيبة البربيرين مع السيسبلاتين الفوائد الأبرز. كانت الفئران الحاملة للأورام التي تلقت المركبين معًا لديها أصغر أحجام أورام وأدنى عدد من خلايا السرطان الحية، إلى جانب نسبة أكبر من الخلايا الورمية الميتة. واستفادت هذه الفئران أيضًا من أكبر مكاسب في مدة البقاء وتمديد العمر بالمقارنة مع الحيوانات الحاملة للورم غير المعالجة. بينما كان السيسبلاتين وحده يميل إلى تعطيل وظائف الكبد والكلى—رافعًا الإنزيمات ونواتج الفضلات في الدم—أعاد إضافة البربيرين هذه المقاييس إلى حد كبير نحو الطبيعي. أظهرت الاختبارات الجزيئية أن الزوج العلاجي عزز مؤشرات موت الخلايا المبرمج، ووقف الخلايا السرطانية في طور عدم الانقسام، وحسّن الدفاعات المضادة للأكسدة في نسيجَي الكبد والكلى، ما يشير إلى أن البربيرين ساعد في الحد من الأضرار العرضية التي يسببها السيسبلاتين.
مساعدة الجسم على إزاحة الخلايا السرطانية الميتة
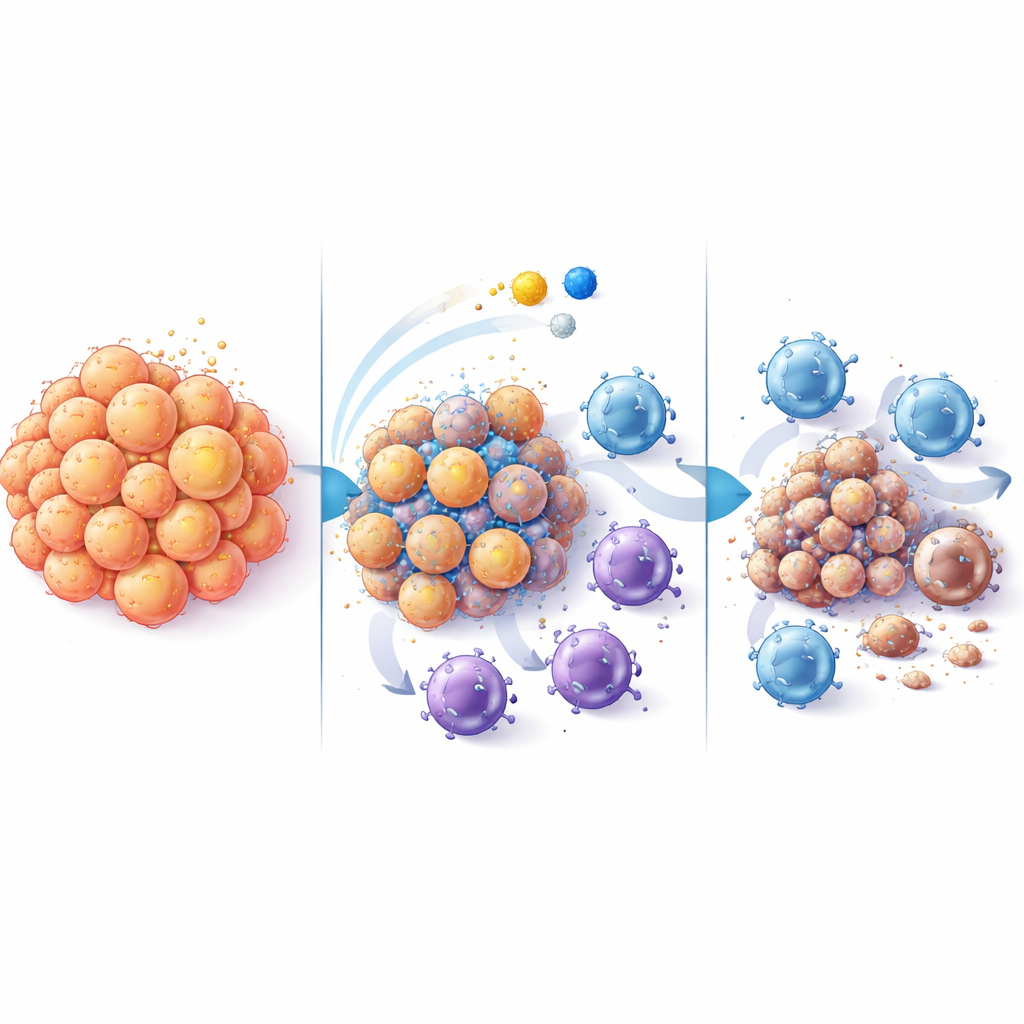
بعيدًا عن مجرد قتل خلايا الورم، نظر الباحثون في مدى كفاءة الجسم في إزالتها، وهي عملية تنظيف تُسمى الالتقماخ الخلوي. ركزوا على إشارتين سطحيتين على خلايا الورم: الكالريتيكولين، الذي يعمل كعلم "كُلْني" للخلايا المناعية، وCD47، الذي يعمل كدرع "لا تأكلْني". في الفئران، زاد البربيرين إشارة الكالريتيكولين المفيدة وعند الجمع مع السيسبلاتين خفّض CD47. جعل هذا التحول الخلايا السرطانية المحتضرة أسهل على الجهاز المناعي للتعرّف عليها وابتلاعها. في الوقت نفسه، قَلَّت أقوى حالة الجينات الرئيسية التي تدفع مسارات النمو والبقاء داخل الخلايا السرطانية (مثل مكوّنات محور الإشارة PI3K/Akt والمستقبلات المرتبطة بها) في مجموعة التركيبة، مما يشير إلى أن البربيرين والسيسبلاتين معًا كانا يزعزعان التوصيلات الداخلية للورم وكذلك ستاره الخارجي.
ما الذي قد يعنيه هذا لعلاجات السرطان المستقبلية
بعبارات مبسطة، توحي هذه الدراسة أن البربيرين يمكن أن يساعد السيسبلاتين على أداء مهمته بشكل أفضل: فمعًا قلّصا الأورام أكثر، وقتلا مزيدًا من الخلايا السرطانية، ومدّا فترة البقاء، وقللا تلف الكبد والكلى في الفئران. من خلال إضعاف الإشارات المشجعة للسرطان وجعل الخلايا الورمية المحتضرة أكثر "وضوحًا" للجهاز المناعي، يبدو أن البربيرين يحول السيسبلاتين إلى أداة أكثر حدة ونظافة. وبينما هذه النتائج أولية وتستند إلى نموذج حيواني، فإنها تشير إلى إمكانية استخدام مركب نباتي معروف كمكمل للعلاج الكيميائي القياسي، بهدف ليس فقط تحكم أقوى في السرطان بل أيضًا علاج ألطف لبقية الجسم.
الاستشهاد: Salem, M.M., Dawod, S.M., Mohamed, T.M. et al. Berberine enhances cisplatin efficacy in ehrlich ascites carcinoma via modulation of apoptotic pathway and efferocytosis. Sci Rep 16, 13637 (2026). https://doi.org/10.1038/s41598-026-49296-3
الكلمات المفتاحية: البربيرين, السيسبلاتين, الالتقماخ الخلوي, إشارة PI3K Akt, سُمّية العلاج الكيميائي