Clear Sky Science · ar
الاستخلاص الانتقائي لليثيوم من محاليل النشاوية الحامضية لبطاريات منتهية الصلاحية
لماذا لا تزال البطاريات القديمة مهمة
تغذي بطاريات أيون الليثيوم هواتفنا وأجهزتنا الحاسوبية وسياراتنا الكهربائية، لكن الليثيوم بداخلها يصعب استعادته بمجرد انتهاء عمر البطاريات. اليوم، يُفقد جزء كبير من ذلك الليثيوم أو يُستعاد فقط بعد العديد من الخطوات المكلفة. تستكشف هذه الدراسة طريقة أبسط لسحب الليثيوم مبكراً من السائل الحامضي الناتج عند إذابة البطاريات المُفرَّقة كيميائياً، بهدف توفير الطاقة والمواد الكيميائية والمعادن القيمة.
تحويل الخلايا المفرَّقة إلى سائل مفيد
غالباً ما يبدأ إعادة تدوير البطاريات الحديثة بـ «الكتلة السوداء»، وهي مسحوق داكن ينتج عن تمزيق الخلايا المستهلكة. هذا المسحوق غني بالليثيوم لكنه غني أيضاً بالنيكل والكوبالت والمنغنيز ومعادن أخرى. إحدى الطرق الشائعة هي إذابة الكتلة السوداء في حمض كلور الماء (HCl)، مكوِّنة سائلاً مالحاً يحمل تقريباً جميع المعادن معاً. التحدي أن طرق الاسترداد الحالية عادةً تركز على المعادن الأغلى ثمناً أولاً، تارِكة الليثيوم إلى النهاية، حين يكون مُخففاً ومفقوداً جزئياً ومختلطاً بالعديد من الشوائب. إن استخلاص الليثيوم في وقت أبكر من نفس السائل الحامضي سيكون أكثر كفاءة، لكنه يتطلب مادة تستطيع التقاط الليثيوم بشكل انتقائي دون اصطحاب المعادن الأخرى.
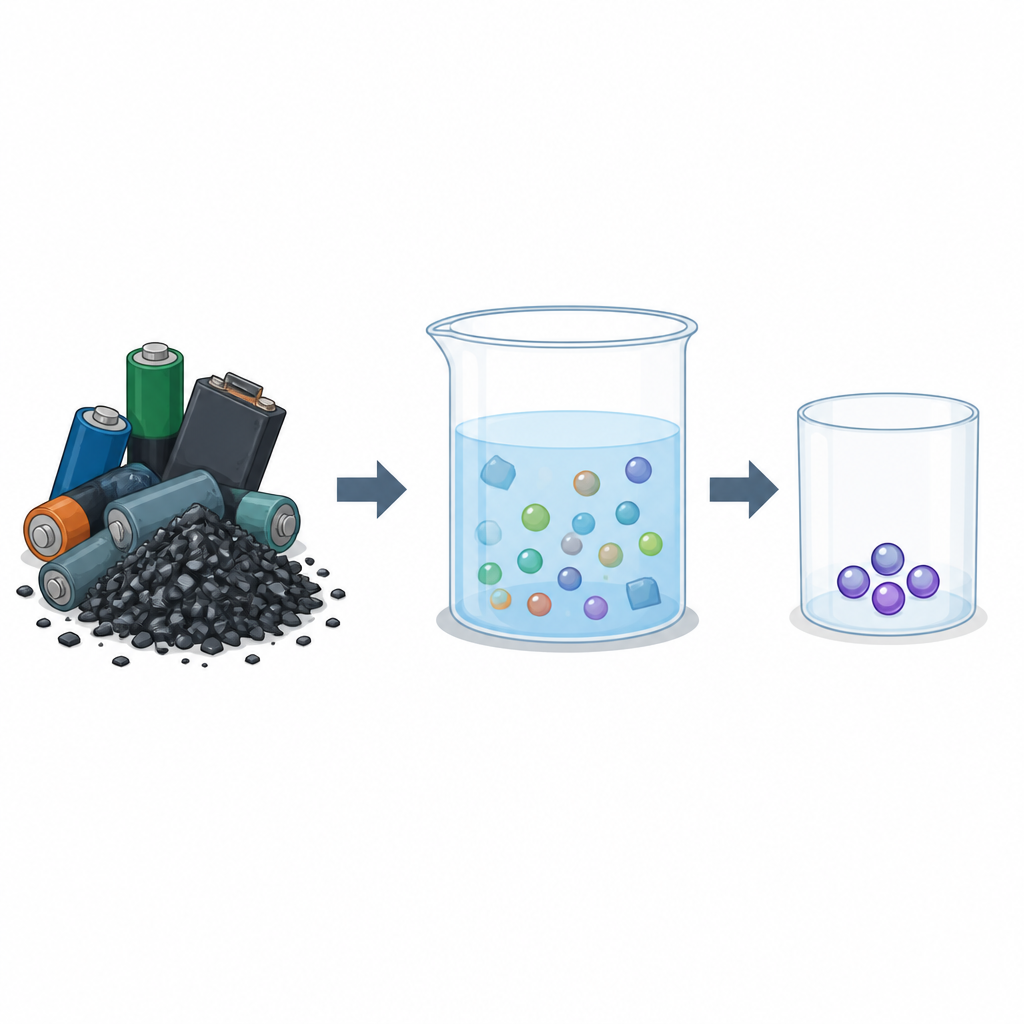
سائل مُصمم يفضّل الليثيوم
صمم الباحثون سائلًا عضويًا خاصًا يعمل كمرشح على المستوى الجزيئي. يجمع بين ثلاثة مكونات: أيونات الحديد، ومذيب صناعي شائع يُسمى ثلاثي بيوتيل فوسفات، وجزيء مساعد حمضي معروف باسم P507. عند مزج الطور العضوي هذا مع محلول نشارة البطاريات الحمضي، تنتقل أيونات الليثيوم إلى السائل العضوي بسهولة أكبر بكثير من النيكل أو الكوبالت أو المنغنيز. ضبط الفريق بعناية النسبة بين P507 والحديد بحيث يتمكن السائل من التقاط الليثيوم من المحلول الحامضي ثم إطلاقه لاحقاً في ماء نقي، مع إبقاء الحديد محتبساً داخل الطور العضوي لإعادة الاستخدام.
خطوة بخطوة: من حساء مختلط إلى ليثيوم نقي
اختُبرت مخططان عمليان مختلفان قليلاً. في الأول، تم تحميل السائل العضوي بالليثيوم مباشرةً من نَشْر البطارية، وأضيف P507 بعد ذلك لتثبيت النظام. في الثاني، حُمِّل الحديد أولاً في الطور العضوي باستخدام محلول مخزوني بسيط، ثم جُلب هذا السائل إلى اتصال مع النَشْر الفعلي. اتبعت كلتا الطريقتين ثلاث مراحل رئيسية: الغسل لإزالة الشوائب الأثرية، والاقتلاع لنقل الليثيوم من السائل العضوي إلى الماء، والتجديد لتحضير الطور العضوي لدورة جديدة. مع نسبة خلط مناسبة بين الطور العضوي والمائي ونسبة P507 إلى الحديد حوالي 1.5 إلى 1.7، استخرجت العملية أكثر من 90 في المئة من الليثيوم عبر مراحل تلامس متعددة بينما تُرك النيكل والكوبالت تقريباً بالكامل في المحلول الأصلي.
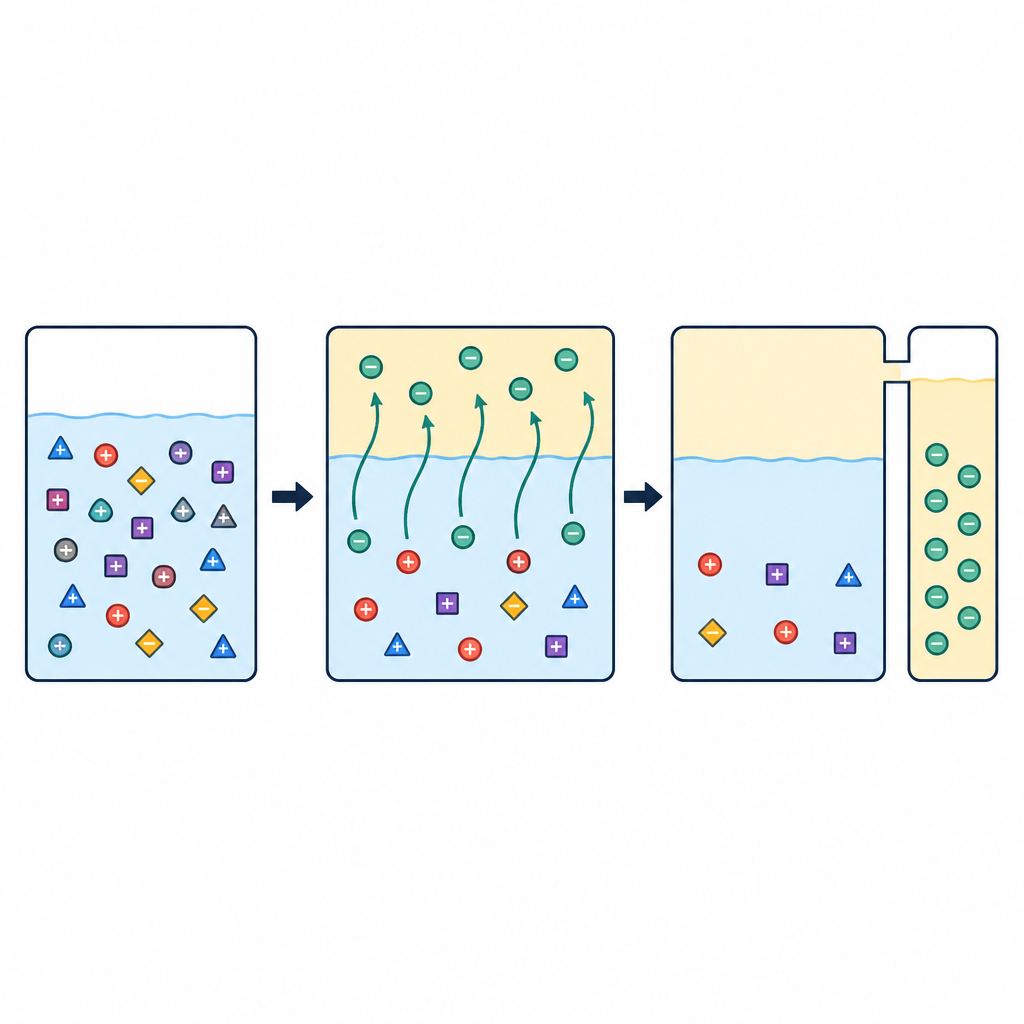
الحفاظ على استقرار النظام وقابليته لإعادة الاستخدام
استخدم الفريق قياسات الأشعة تحت الحمراء والأشعة فوق البنفسجية المرئية لتأكيد كيفية تفاعل الحديد والجزيئات العضوية داخل مرشح السائل. أظهرت هذه الاختبارات أن الحديد يبقى مرتبطاً في شكل يبقى في الطور العضوي حتى عندما ينخفض مستوى الكلوريد أثناء اقتلاع الماء. نتيجةً لذلك، يمكن إعادة استخدام نفس المذيب لعدة دورات دون فقدان كبير في الحديد أو أداء الاستخلاص. على مدى ست تجارب متكررة، ظل الاستخلاص في مرحلة واحدة لليثيوم بالقرب من 65 في المئة، واحتوى التيار المائي النهائي الغني بالليثيوم على 11 إلى 14 غراماً من الليثيوم لكل لتر بينما كانت مستويات النيكل والكوبالت تحت حد الكشف وكان المنغنيز شبه غائب.
ما يعنيه هذا لإعادة تدوير البطاريات أنظف
بالنسبة لغير المتخصص، النتيجة الأساسية هي أنه يمكن سحب الليثيوم مبكراً من محلول نشارة بطارية قاسٍ وملحي باستخدام مرشح سائل قابل لإعادة التدوير والماء فقط كخطوة نهائية لاسترداده. هذا يتجنب تسخين الكتلة السوداء لدرجات حرارة عالية، ويقلل المواد الحمضية والقاعدية المضافة، ويمنع إدخال معادن شوائب إضافية. في مصنع إعادة تدوير صناعي، يمكن بعد ذلك معالجة المحلول المنقّى باستخدام طرق موجودة لاسترداد النيكل والكوبالت والمنغنيز، بينما يمكن تحويل التيار المائي الغني بالليثيوم إلى أملاح ليثيوم بدرجة بطارية. معاً، تقدم هذه الخطوات طريقة أكثر كفاءة وربما أكثر استدامة لإغلاق دورة الليثيوم في البطاريات القابلة لإعادة الشحن.
الاستشهاد: Saleem, U., Buvik, V., Bandyopadhyay, S. et al. Selective extraction of lithium from acidic chloride leachates of spent batteries. Sci Rep 16, 14984 (2026). https://doi.org/10.1038/s41598-026-43332-y
الكلمات المفتاحية: إعادة تدوير الليثيوم, مُرشّح البطارية, استخلاص بالمذيبات, الكتلة السوداء, الهايدروميتالورجيا