Clear Sky Science · ar
بروبوفول ينظّم تعديل m6A لِـ PARP-1 بواسطة METTL3 لتحفيز بارثاناتوس وتحسين مقاومة العلاج الكيميائي في سرطان الرئة غير صغير الخلايا
لماذا تهم هذه الدراسة الأشخاص المصابين بسرطان الرئة
يتلقى العديد من الأشخاص المصابين بسرطان الرئة غير صغير الخلايا، وهو أكثر أنواع سرطان الرئة شيوعًا، علاجًا كيمياويًا يعتمد على دواء السيزبلاتين. وللأسف، غالبًا ما تُصبِح الأورام مقاومة لذلك يتراجع فعاليته. تستكشف هذه الدراسة مساعدًا غير متوقع موجودًا بالفعل في غرف العمليات يوميًا: المخدّر بروبوفول. يسأل الباحثون ما إذا كان بإمكان بروبوفول أن يجعل الأورام العنيدة في الرئة حساسة للعلاج الكيميائي مرة أخرى ويكشفون كيف يحدث ذلك داخل خلايا السرطان.
مخدّر مألوف مع وظيفة خفية
يشتهر بروبوفول بكونه الدواء الذي ينعِم المريض للنوم بسرعة قبل الجراحة. في السنوات الأخيرة، لاحظ العلماء أنه قد يؤثر أيضًا في كيفية نمو وخضوع خلايا السرطان للموت. أشارت أعمال سابقة إلى أن بروبوفول قد يبطئ نمو خلايا سرطان الرئة ويعزز تأثيرات السيزبلاتين، لكن الشرح التفصيلي بقي غامضًا. ركز المؤلفون هنا على سلالة خلايا سرطان رئة مقاومة للسيزبلاتين ونماذج فئران لمعرفة ما إذا كان بروبوفول يمكن أن يستعيد استجابة العلاج الكيميائي وإذا كان الأمر كذلك، ما هي مفاتيح الخلية التي يغيّرها لتحقيق ذلك.
إجبار الخلايا المقاومة على الانتحار الذاتي
في أطباق تحتوي خلايا سرطان الرئة، كان بروبوفول وحده يكاد لا يضر الخلايا العادية، لكنه خفّض بقوة بقاء الخلايا المقاومة للسيزبلاتين عندما استُخدم مع الدواء. أظهرت طرق الصبغ التي تبرز الخلايا الميتة أن العلاج المزدوج تسبب في درجة أكبر بكثير من موت الخلايا مقارنة بالسيزبلاتين وحده. في الفئران المزروعة بأورام رئوية مقاومة، أدى إضافة بروبوفول إلى السيزبلاتين إلى أورام أصغر ووزن أورام أخف ومناطق تحلل نسيجي أكثر مقارنة بالعلاج الكيميائي وحده. تشير هذه النتائج إلى أن بروبوفول لا يكتفي بتخدير المرضى؛ بل يدفع أيضًا خلايا الأورام المقاومة للعقاقير نحو الدمار عند استخدامه جنبًا إلى جنب مع السيزبلاتين. 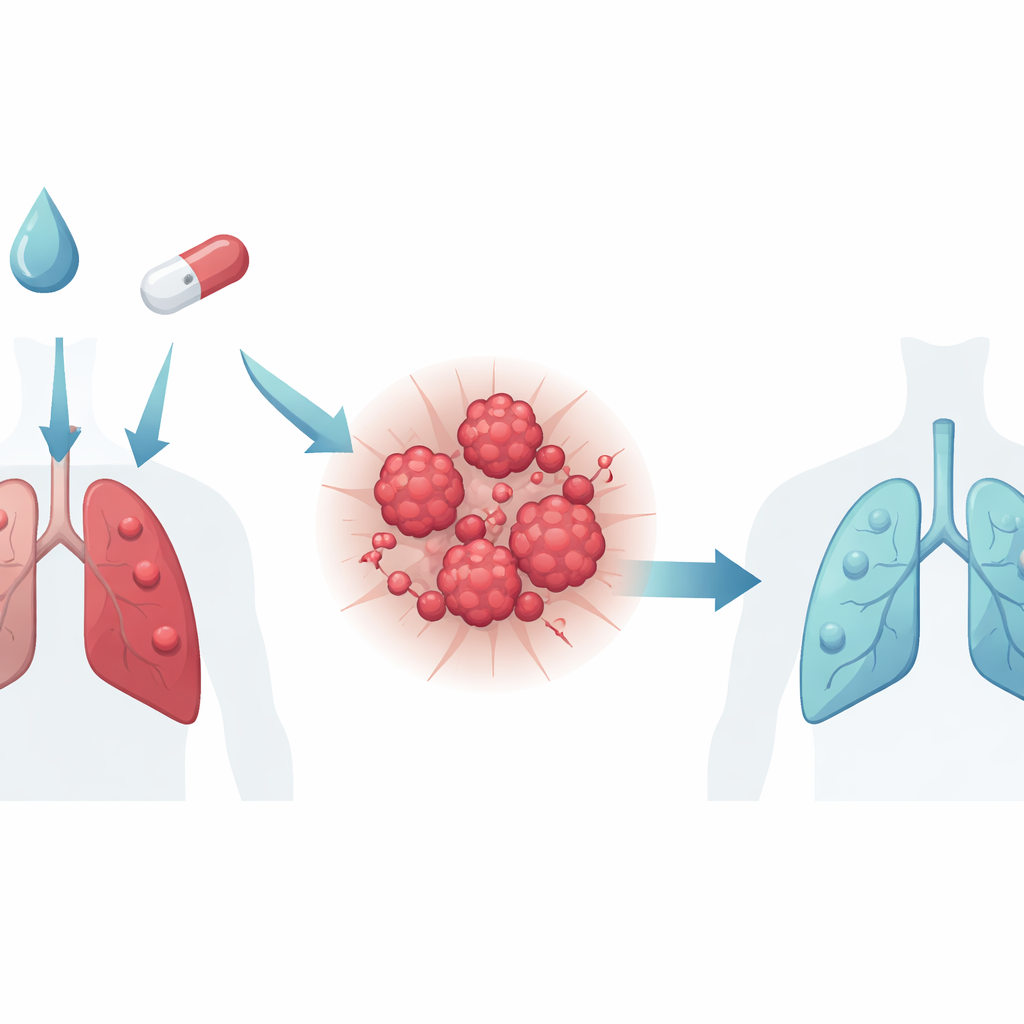
نوع خاص من موت الخلايا مفعّل
سأل الفريق بعد ذلك عن نوع موت الخلايا الذي يتم تحفيزه. بدلًا من مسار الانتحار الخلوي «المرتب» الكلاسيكي الذي يُناقَش كثيرًا في أبحاث السرطان، وجدوا أدلة على مسار أقل شهرة يُسمى بارثاناتوس. في هذه العملية، يصبح إنزيم إصلاح الحمض النووي PARP-1 مفرط النشاط، مستهلكًا جزيء طاقة أساسيًا (NAD+)، ومتسببًا في تلف الميتوكوندريا، ودافعًا ثنائي بروتين قوي إلى نواة الخلية ليتسبب في تمزيق الحمض النووي. راقب الباحثون كل هذه العلامات المميزة: زيادة ارتباط وحركة نووية للبروتينين AIF وMIF، فقدان سلامة غشاء الميتوكوندريا، استنزاف NAD+، تراكم مركب مرتبط بـ PARP-1 (PAR)، وإشارات قوية لتلف الحمض النووي. أدت استعمال مثبط محدد لـ PARP-1 إلى عكس هذه التغيرات، مما يوضح أن هذا التسلسل المدمّر يعتمد على دفع PARP-1 إلى حالة فرط نشاط بواسطة العلاج.
إنزيم وسم الرنا في قلب المفتاح
لفهم سبب فرط نشاط PARP-1، توجّه الباحثون إلى طبقة تحكم جيني تعمل ليس بتغيير الحمض النووي بل بوضع علامات خفيفة على رسائل الرنا. إنزيم مركزي في هذه العملية يُسمى METTL3 يضع وسمًا كيميائيًا صغيرًا (المعروف m6A) على الرنا ويمكن أن يؤثر على مدة بقاء هذه الرسائل ومقدار البروتين المنتج منها. تُظهر الدراسة أن بروبوفول يزيد مستويات METTL3 في خلايا سرطان الرئة المقاومة المعالجة بالسيزبلاتين. عندما تم تقليل METTL3 اصطناعياً، انخفض الوسم الخاص على رنا PARP-1، وتراجعت مستويات PARP-1، وقلّت خسارة الطاقة، وتراجعت علامات بارثاناتوس. وعند زيادة METTL3، حدث العكس: مزيد من الوسم على رنا PARP-1، وزيادة نشاط PARP-1، ومزيد من الإجهاد الميتوكوندري، وإشارات أقوى لهذا المسار القاتل. في أورام الفئران، زاد بروبوفول مع السيزبلاتين من البروتينات المرتبطة ببارثاناتوس، لكن هذا التأثير خَفّ عندما تم خفض METTL3 في خلايا السرطان. 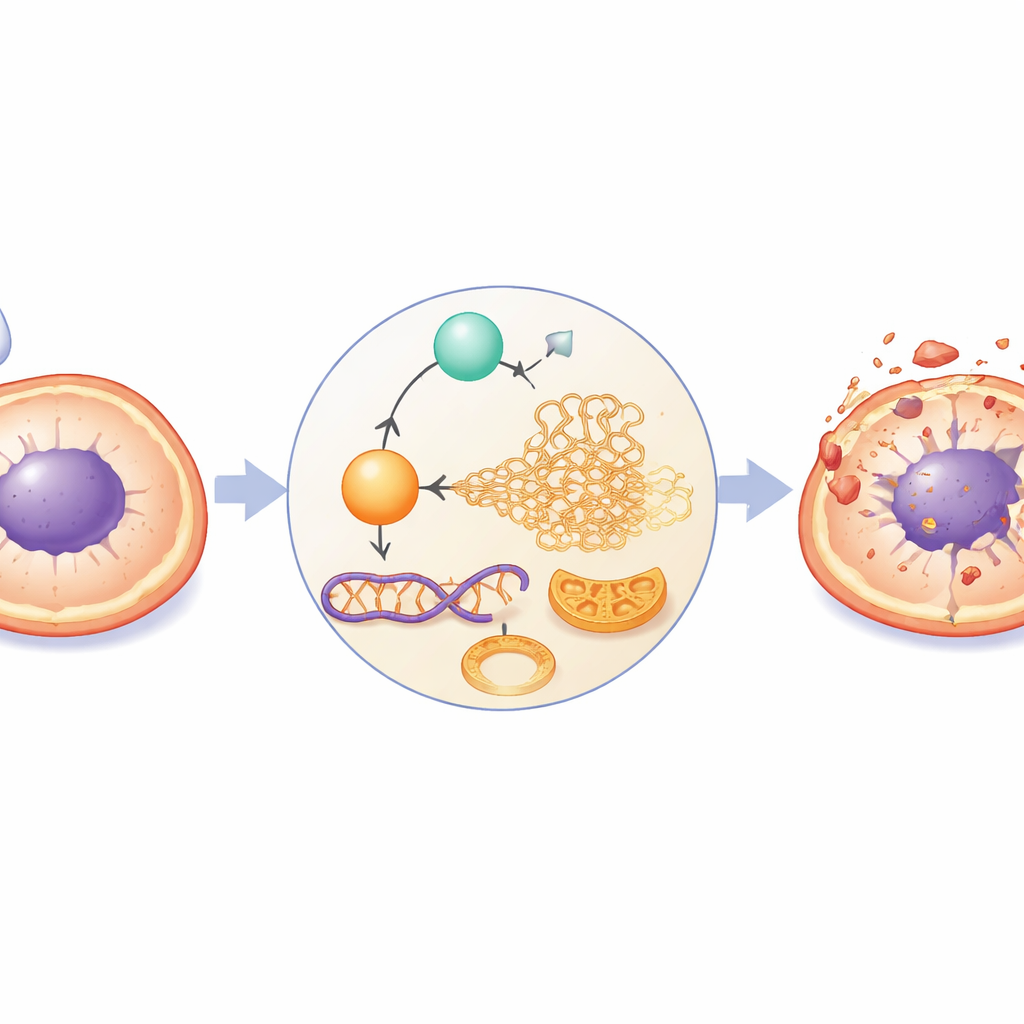
ماذا قد يعني هذا للعلاجات المستقبلية
بشكل إجمالي، تكشف الدراسة أن بروبوفول يمكن أن يجعل خلايا سرطان الرئة غير صغيرة الخلايا المقاومة حساسة للسيزبلاتين مرة أخرى عبر رفع METTL3، الذي بدوره يثبت PARP-1 ويدفع الخلايا نحو بارثاناتوس. بعبارة مبسطة، يساعد بروبوفول على «إغراق» نظام إصلاح في خلايا السرطان إلى حد يدفعها إلى شكل كارثي من الموت، متغلبًا على مقاومتها للعلاج الكيميائي. ورغم أن هذه النتائج ما تزال في مرحلتي المختبر والحيوانات، فإنها توحي بأن أدوية تؤثر على سلسلة METTL3–PARP-1–Parthanatos، بما في ذلك مخدّرات شائعة الاستخدام، قد تُستغل مستقبلاً لتحسين نجاح العلاج الكيميائي في سرطانات الرئة صعبة العلاج.
الاستشهاد: Ling, Q., Liu, K., Wen, J. et al. Propofol regulates METTL3-mediated PARP-1 m6A modification to promote Parthanatos to improve NSCLC chemotherapy resistance. Sci Rep 16, 12110 (2026). https://doi.org/10.1038/s41598-026-42665-y
الكلمات المفتاحية: سرطان الرئة غير صغير الخلايا, مقاومة السيزبلاتين, بروبوفول, PARP-1, ميثلة الحمض النووي الريبي