Clear Sky Science · ar
كلودين18.2 يعزز تكاثر سرطان المعدة عبر تنشيط MCM2/5
لماذا هذا مهم لسرطان المعدة
يبقى سرطان المعدة من بين أكثر السرطانات فتكًا عالميًا، جزئياً لأن العديد من المرضى يُشخَّصون في مراحل متأخرة ولا تعمل العلاجات الحالية مع الجميع. تركز هذه الدراسة على جزيء بوّاب قليل المعرفة على خلايا المعدة يُسمى كلودين18.2، وتطرح سؤالين كبيرين: هل يمكن أن تساعد الأدوية التي تتعرف على هذا الجزيء المرضى على العيش لفترة أطول، وماذا يفعل كلودين18.2 داخل الخلايا الورمية تحديدًا ليساعدها على النمو؟ قد تُحسّن الإجابات طريقة اختيار الأطباء للمرضى المناسبين للأدوية المستهدفة الجديدة وتلهم تراكيب علاجية مبتكرة.
علامة سطحية بوعد علاجي
راجع الباحثون أولاً تجربتين سريريتين دوليتين كبيرتين، تسميان SPOTLIGHT وGLOW، اختبَرتا دواءً مضادًا بالأجسام المضادة يُدعى زولبيتوكسيماب لدى مرضى بسرطان المعدة أو تقاطع المريء والمعدة المتقدم الذين كانت أورامهم تحمل كلودين18.2 لكنها تفتقر إلى علامة شائعة أخرى، HER2. بجمع بيانات 1,072 مريضًا، وجدوا أن إضافة الزولبيتوكسيماب إلى العلاج الكيميائي القياسي أخر بوضوح تدهور السرطان مقارنة بالعلاج الكيميائي وحده. وكانت الفائدة ملحوظة خصوصًا لدى المرضى الآسيويين، وفي السرطانات التي بدأت في جسم المعدة الأساسي بدلًا من التقاطع مع المريء، وفي الأورام من النوع المعوي المزعوم. هذه النتائج تقوي الحجة بأن كلودين18.2 ليس مجرد علامة على سطح الورم، بل هدف مفيد للعلاج الخطي الأول لدى مرضى محددين.
علامة ترتبط بمرض أكثر عدوانية
لفهم ما يعنيه وجود كلودين18.2 بالنسبة للمرضى الأفراد، فحص الفريق عينات نسيجية من 92 شخصًا خضعوا لعملية جراحية لسرطان المعدة. باستخدام جسم مضاد عالي التخصيص يتعرف فقط على نمط كلودين18.2 الفرعي، قيّموا شدة تلطيخ أغشية الخلايا الورمية. حوالي 46 بالمئة من الأورام كانت إيجابية. الأورام الإيجابية كانت أكثر احتمالًا أن تكون انتشرت إلى العقد اللمفاوية المجاورة، وكان المزيد من المرضى الذين لديهم سرطانات إيجابية لكلودين18.2 في مراحل متقدمة (III أو IV) عند التشخيص. عند متابعة نتائج المرضى، وجد الباحثون أن الأشخاص الذين أعربت أورامهم عن كلودين18.2 كان لديهم بقاء عام أقصر: حوالي 31 بالمئة فقط كانوا على قيد الحياة بعد خمس سنوات، مقارنة بـ52 بالمئة بين أولئك الذين افتقرت أورامهم إلى هذه العلامة. هذا يشير إلى أن كلودين18.2 قد يشير إلى شكل أكثر عدوانية من المرض.
كيف يدفع كلودين18.2 نمو الخلايا الورمية
بعد ذلك، تحول المحققون إلى نماذج خلوية وحيوانية لكشف ما يفعله كلودين18.2 داخل الخلايا السرطانية. ركزوا على خط خلوي لسرطان المعدة يُنتج مستويات عالية بطبيعته من كلودين18.2 واستخدموا أدوات جينية لإيقاف هذا البروتين. عند تقليل كلودين18.2، انقسمت الخلايا ببطء أكبر وعلق كثير منها عند نقطة تفتيش مهمة قبل الانقسام الخلوي تُعرف بمرحلة G2/M. في الفئران، بقيت الأورام المنبثقة من خلايا ناقصة كلودين18.2 أصغر بكثير وأخف وزنًا من الأورام المنبثقة من خلايا غير معدلة، على الرغم من أن الصحة العامة ووزن الجسم لدى الحيوانات لم تتغير. أظهرت عينات الأورام من هذه الفئران أيضًا خلايا أقل نشاطًا في الدورة ومستويات منخفضة من البروتينات المرتبطة بالتكرار الخلوي.
الصلة بآلات النسخ داخل الخلية
لاستقصاء الآلية، حلل الفريق أي الجينات تغيرت عند خفض كلودين18.2. وجدوا تحولات واسعة في المسارات المرتبطة بدورة الخلية ونسخ الحمض النووي. برزت عائلة بروتينات تُدعى بروتينات صيانة النسخة الصغيرة، أو MCMs. تعمل هذه البروتينات كقوابض تنزلق على الحمض النووي لمساعدته على التفكيك والنسخ. في الخلايا التي انخفض فيها كلودين18.2، انخفضت مستويات عدة أعضاء من عائلة MCM، لا سيما MCM2 وMCM5، اللذان يشكلان معًا بوابة دخول حاسمة للحمض النووي إلى آلية النسخ. إعادة كلودين18.2 أعادت مستويات MCM2 وMCM5 وأنقذت قدرة الخلايا على التكاثر. في أورام الفئران، أدى خفض كلودين18.2 أيضًا إلى خفض MCM2 وMCM5. تشير هذه العلاقة الوثيقة إلى أن بروتينات MCM هذه هي وسطاء رئيسيون يعمل عبرهم كلودين18.2 لتعزيز نمو الورم.
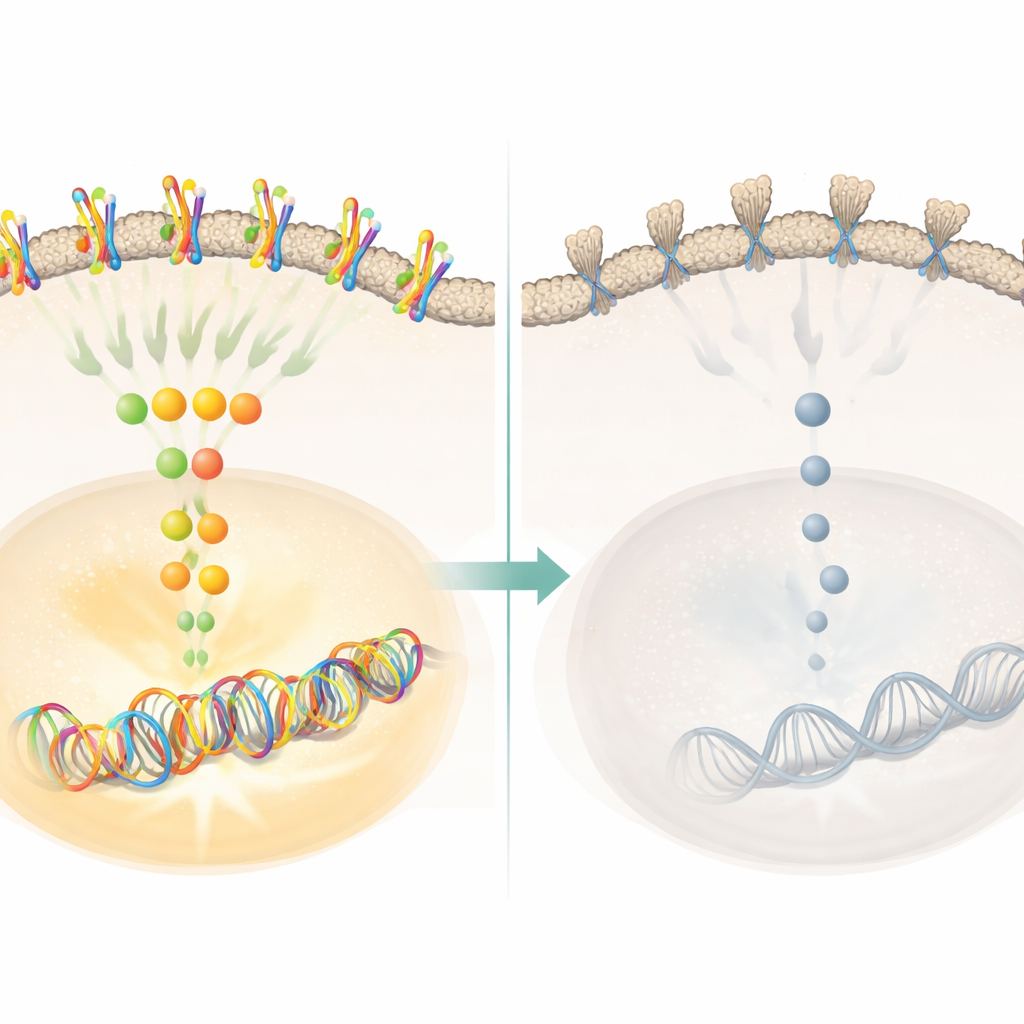
مفاتيح إشارية تتحكم في النمو
أظهرت الدراسة أيضًا أن كلودين18.2 يؤثر في مسارات تحكم رئيسية بالنمو داخل الخلية. عندما تم إسكات كلودين18.2، تراجعت نشاطات مستقبلات التيروسين كيناز على سطح الخلية والجزيئات المتعاقبة مثل ERK وCDK1، التي تعمل كمفاتيح لتقدم دورة الخلية. انخفضت الفسفرة، وهي علامة كيميائية تُشغّل هذه المفاتيح، على ERK وCDK1 وMCM2، ما يوحي بأن سلسلة الإشارة الكاملة الدافعة لنسخ الحمض النووي قد تخفت. عند إعادة مستويات كلودين18.2 تعافت الإشارات. أشارت تحليلات قواعد البيانات أيضًا إلى أن الأورام ذات كلودين18.2 العالي قد تكون حساسة بشكل خاص للأدوية التي تثبط إنزيمات دورة الخلية، مما يلمح إلى أن ربط علاجات مستهدفة لكلودين18.2 بمثبطات دورة الخلية قد يكون مثمرًا.
ما الذي يعنيه هذا للمرضى
بعبارات بسيطة، تُظهر هذه الدراسة أن كلودين18.2 أكثر من مجرد علامة على بعض سرطانات المعدة: إنه يعمل كمفتاح رئيسي يساعد خلايا الورم على مواصلة نسخ حمضها النووي والانقسام، جزئيًا عبر تنشيط آلات النسخ MCM والمسارات الرئيسية للنمو. يحُدّ منع كلودين18.2، سواء بدواء مثل الزولبيتوكسيماب أو بخفض نشاطه، من نمو الأورام في الخلايا والفئران والمرضى، وتبدو الأورام الحاملة لهذه العلامة أكثر عدوانية في الغالب. تدعم هذه النتائج استخدام اختبارات دقيقة لكلودين18.2 لاختيار المرضى المرجح أن يستفيدوا من العلاج المستهدف وتصميم تراكيب ذكية تُطفئ محرك نمو الورم عند نقاط متعددة.
الاستشهاد: Zheng, B., Fu, M., Lou, F. et al. Claudin18.2 promote gastric cancer proliferation by activating MCM2/5. Sci Rep 16, 10263 (2026). https://doi.org/10.1038/s41598-026-39540-1
الكلمات المفتاحية: سرطان المعدة, كلودين18.2, العلاج المستهدف, دورة الخلية, تكرار الحمض النووي