Clear Sky Science · ar
تحليل التطور العُرْفي يكشف أنماط التحول الخبيث للأورام الغدية المخاطية الحليمية داخل القنوات في البنكرياس
لماذا تهم الأكياس الصغيرة في البنكرياس
يُعد سرطان البنكرياس من أخطر أنواع السرطان، ويرجع ذلك بشكل كبير إلى أنه يُكتشف عادة في مراحل متأخرة. ومع ذلك، يُكتشف لدى كثير من المرضى أكياس صغيرة مملوءة بالسوائل في البنكرياس تُسمى الأورام الغدية المخاطية الحليمية داخل القنوات (IPMNs). يمكن رؤية هذه الأكياس على الفحوصات قبل سنوات من ظهور السرطان، مما يوفر نافذة نادرة للوقاية. والتحدي هو التمييز بين الأكياس التي ستظل خاملة وتلك التي ستتطور إلى سرطان قنوي ليفي البنكرياس المهدد للحياة (PDAC). تسأل هذه الدراسة سؤالاً بسيطاً لكنه حاسم: كيف تتحول هذه الأكياس إلى سرطان على مستوى الحمض النووي والنسج؟
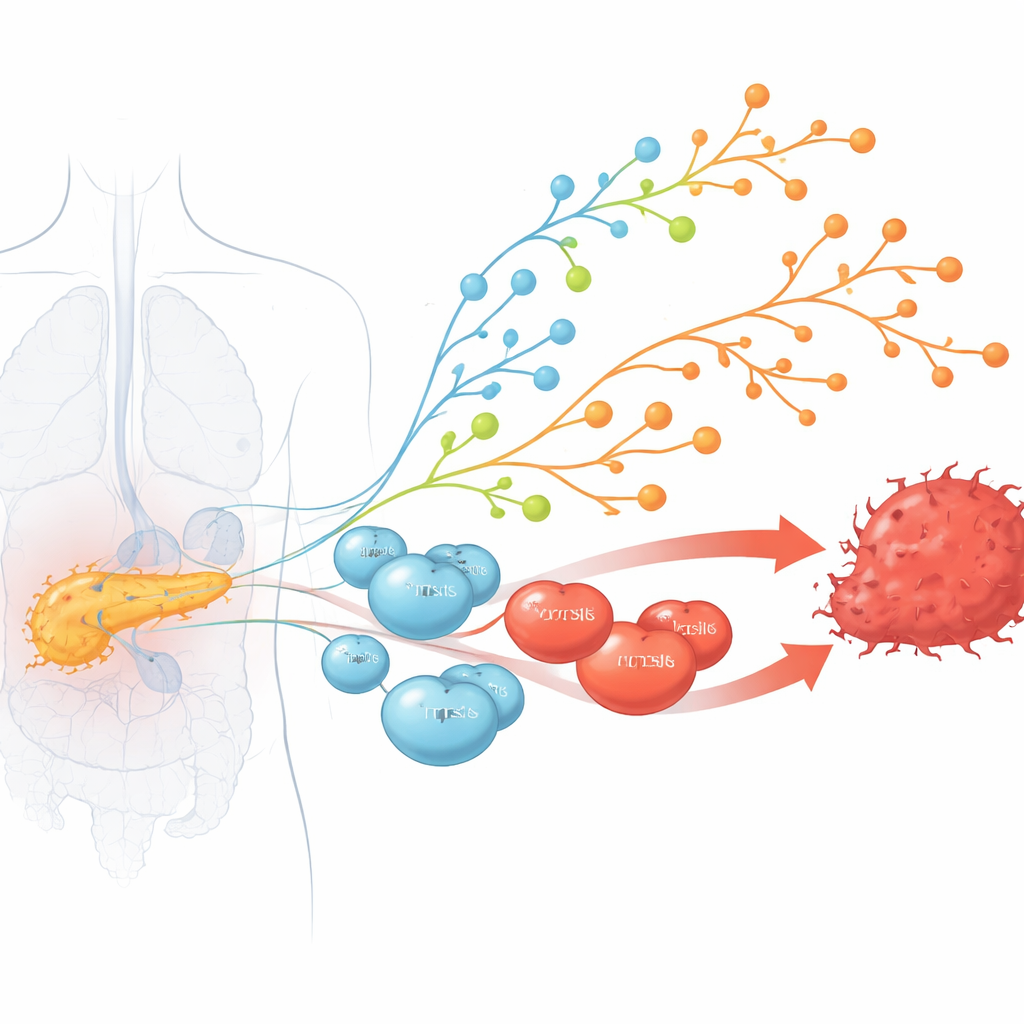
تتبع قصة حياة الأكياس السابقة للسرطان
درس الباحثون عينات IPMNs استُأصلت من بنكرياس 12 مريضاً أثناء الجراحة. وبدلاً من التعامل مع كل ورم كوحدة واحدة، أخذوا عينات من عدة مناطق في كل آفة — مناطق منخفضة الدرجة، ومناطق عالية الدرجة، ومناطق غازية قريبة عندما وُجدت. ثم قاموا بتسلسل الجينوم الكامل ونشاط آلاف الجينات (النسخة الجينية) من 47 عينة ورمية ونسيج طبيعي مطابق. أتاح لهم ذلك إعادة بناء "أشجار عائلية" لخلايا السرطان، وتتبع تراكم تلف الحمض النووي عبر الزمن، وربط التغيرات الجينية بتحولات في سلوك الخلايا والبيئة المناعية المحيطة.
مساران رئيسيان من الكيسة إلى السرطان
كشفت أشجار العائلة الجينية عن نمطَين تطوريين عامّين. في معظم المرضى، عادت كل أجزاء الآفة إلى سلف مؤسس واحد، مثل شجرة ذات جذع واحد يتفرع لاحقاً. في حالات أخرى، أجزاء مختلفة مما بدا ككيسة واحدة نشأت فعلياً من مؤسسين مستقلين نما كلٌ منها جانباً إلى جانب، أشبه بأحراج من الشجيرات. أظهر كلا النمطين تراكمًا تدريجياً للضرر الجيني: طفرات مبكرة ومشتركة في جينات مثل KRAS وGNAS ظهرت في الجذع، بينما ارتبطت تغييرات لاحقة — بما في ذلك تعدلات في TP53 وLRP1B وفقدان جينات مثل RNF43 وU2AF1 — بالمرحلة السابقة للسرطان عالية الدرجة والسرطان الغازي. والأهم أن عدد وتعقيد عمليات إعادة ترتيب الحمض النووي على نطاق واسع، المعروفة بالمتغيرات التركيبية وتغييرات عدد النسخ، كان أعلى بكثير في السرطان المتطور منه في IPMNs، وبشكل خاص غنى بهذه التغيرات في الآفات ذات التطور المتفرع والمعقد.
قوى طفُرية خفية وعدم استقرار الحمض النووي
من خلال فحص "بصمات" أنواع الطفرات المختلفة، تمكن الفريق من استنتاج العمليات التي شكلت هذه الجينومات عبر الزمن. كان تآكل التلف المرتبط بالعمر حاضراً طوال الوقت، مما ساهم في بدء تكوين IPMNs ودفع توسعها البطيء. في بعض الحالات، أُنشِطت عمليات طفُرية أخرى لاحقاً، بما في ذلك تلك المرتبطة بإنزيمات قد تُسبب مَعدَّلات طفُر عالية، ونماذج تشير إلى عدم استقرار على مستوى الكروموسوم. ومن المثير للاهتمام أن نماذج إدخال-حذف عادةً ما تُربط بعيوب في تصحيح عدم التطابق ظهرت مبكراً، على الرغم من أن الاختبارات القياسية أظهرت أن هذه الأورام لم تتصف بفشل تقليدي في آليات تصحيح عدم التطابق. يقترح ذلك وجود انهيارات بديلة وأكثر دقّة في صيانة الحمض النووي قد تدفع بعض IPMNs بهدوء نحو جينومات أكثر فوضى وخطورة أعلى.
أنماط نشاط الجينات والخلايا المناعية المحيطة
أظهرت بيانات الحمض النووي الريبي أن IPMNs ليست كلها على مسار بيولوجي واحد. حدَّد الباحثون مجموعتين رئيسيتين من التعابير الجينية. كانت إحدى المجموعات تتميز بحمولة طفُرية إجمالية أعلى، وزيادة في نشاط جينات مرتبطة بنوع فرعي أكثر عدوانية "شبيه الحرشفي" من سرطان البنكرياس، وتغيرات متكررة في جين LRP1B؛ كما أنها مالَت إلى وجود المزيد من الخلايا القاتلة (T CD8+) الحاضرة. أما المجموعة الأخرى فبدت أقرب إلى النوع الفرعي "الكلاسيكي" للبنكرياس، المرتبط غالبًا بتوقع أفضل بعض الشيء، وأظهرت تعبيرًا أعلى لجينات مثل GATA6 وHNF4A وKRAS وGNAS. وبمقارنة العينات السابقة للسرطان والغازية، وجدوا أنه مع تقدم الآفات إلى PDAC، أصبحت النسج أكثر سيطرةً من قِبل الليفيويات المرتبطة بالسرطان (خلايا داعمة تشكل نسيجًا ليفيًا كثيفًا يشبه الندبة) وفقدت بعض خصائصها الظهارية الطبيعية، بينما انخفضت الخلايا T عمومًا. ترافق هذا التحول في البيئة الدقيقة للورم مع ميزات جزيئية أكثر عدوانية.
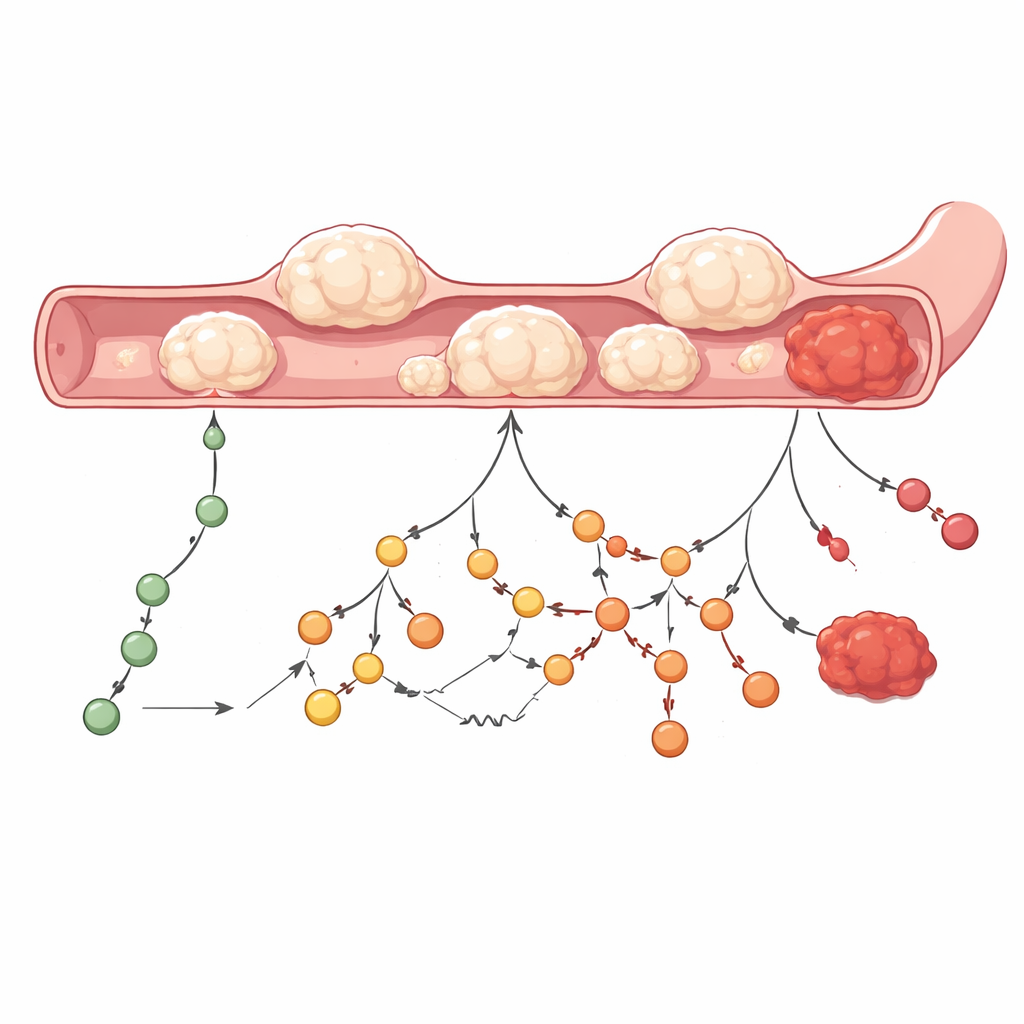
ماذا يعني هذا للمرضى والكشف المبكر
بشكل عام، تُظهر الدراسة أن IPMNs غالبًا ما تتكوّن من مجموعات خلوية متعددة متميزة جينيًا يمكن أن تتبع مسارات مختلفة نحو — أو أحيانًا بعيدًا عن — السرطان. تنمو بعض الآفات من أصل متساوي واحد يكتسب تدريجيًا تغييرات خطيرة، بينما تحتوي أخرى على عدة مؤسسين مستقلين يتطور كل منهم بالتوازي، لكلٍ منهما عيوبه الجينية وبصمته المناعية. تُشير التغيرات التركيبية الكبيرة في الحمض النووي وأنماط التعبير الجيني المعينة إلى النقلة من كيسة حميدة إلى ورم غازي. وللمرضى، تؤكد هذه النتائج سبب صعوبة التنبؤ بالمخاطر اعتمادًا على التصوير وحده، ولماذا قد تفشل اختبارات طفرية بسيطة في سائل الكيسة في كشف الصورة الكاملة. على المدى الطويل، قد يساعد الجمع بين قراءات الجينوم الكامل والحمض النووي الريبي — مع إمكانية تكييفها لأخذ عينات أقل توغلاً — الأطباء على تمييز الأكياس منخفضة المخاطر التي يمكن مراقبتها بأمان عن تلك عالية المخاطر التي تستدعي جراحة في الوقت المناسب، مما يقدّم مسارًا نحو منع حقيقي لسرطان البنكرياس.
الاستشهاد: Pea, A., He, X., Upstill-Goddard, R. et al. Clonal evolutionary analysis reveals patterns of malignant transformation of Intraductal Papillary Mucinous Neoplasms of the pancreas. Nat Commun 17, 3427 (2026). https://doi.org/10.1038/s41467-026-69762-w
الكلمات المفتاحية: سرطان البنكرياس, الأكياس قبل السرطانية, تطور الورم, عدم استقرار جيني, البيئة الدقيقة للورم