Clear Sky Science · ar
أيوجلينا غراكيلس كمنصة فحص عالي الإنتاجية للنشاط المضاد للبكتيريا، السمية الخلوية ونفاذية الغشاء في اختبار خطوة واحدة وفعّال من حيث التكلفة
لماذا تهم خلية خضراء صغيرة
تصبح العدوى البكتيرية المميتة أصعب في المعالجة مع تطوّر الجراثيم لمقاومة مضاداتنا الحيوية الحالية. ومع ذلك، فإن العثور على أدوية جديدة عملية بطيئة ومكلفة وغالباً ما تكون محبطة. تقدم هذه الدراسة مساعداً بسيطاً وغير متوقع: أيوجلينا غراكيلس، ميكروب شائع يعيش في البرك. من خلال مراقبة كيفية تغيّر لون هذه الخلية الخضراء الصغيرة، بنى الباحثون اختباراً من خطوة واحدة يمكنه بسرعة تمييز مرشحات مضادة للبكتيريا واستخلاص المركبات السامة والتحقق مما إذا كانت تستطيع اجتياز حواجز بيولوجية متعددة — وكل ذلك في اختبار اقتصادي واحد.
تغير لوني بسيط ذو تبعات كبيرة
تبدو الأيوجلينا كحذاء أخضر صغير تحت المجهر. لونها ينتج عن البلاستيدات الخضراء، نفس الهياكل المسؤولة عن حصاد الضوء الموجودة في خلايا النباتات. في الماضي البعيد، نشأت تلك البلاستيدات من بكتيريا، وما زالت تحتفظ ببعض الصفات البكتيرية. تجعل هذه الخصوصية البلاستيدات عرضة لعدة مضادات حيوية، التي يمكن أن تضر بالبلاستيدات أو تزيلها وتحول الأيوجلينا من الأخضر إلى الأبيض — عملية تُعرف بالتبييض. في الوقت نفسه، فالأيوجلينا كائن غذائي مرن: يمكنه العيش على مغذيات مذابة حتى عند فقدانه للبلاستيدات. هذا يعني أن المركب الذي يسبب تبييض الأيوجلينا بينما تظل الخلايا حية وتستمر في الانقسام يحتمل أن يستهدف آلية مضادة للبكتيريا من دون أن يكون ساماً على نطاق واسع للخلايا المعقدة مثل خلايانا.
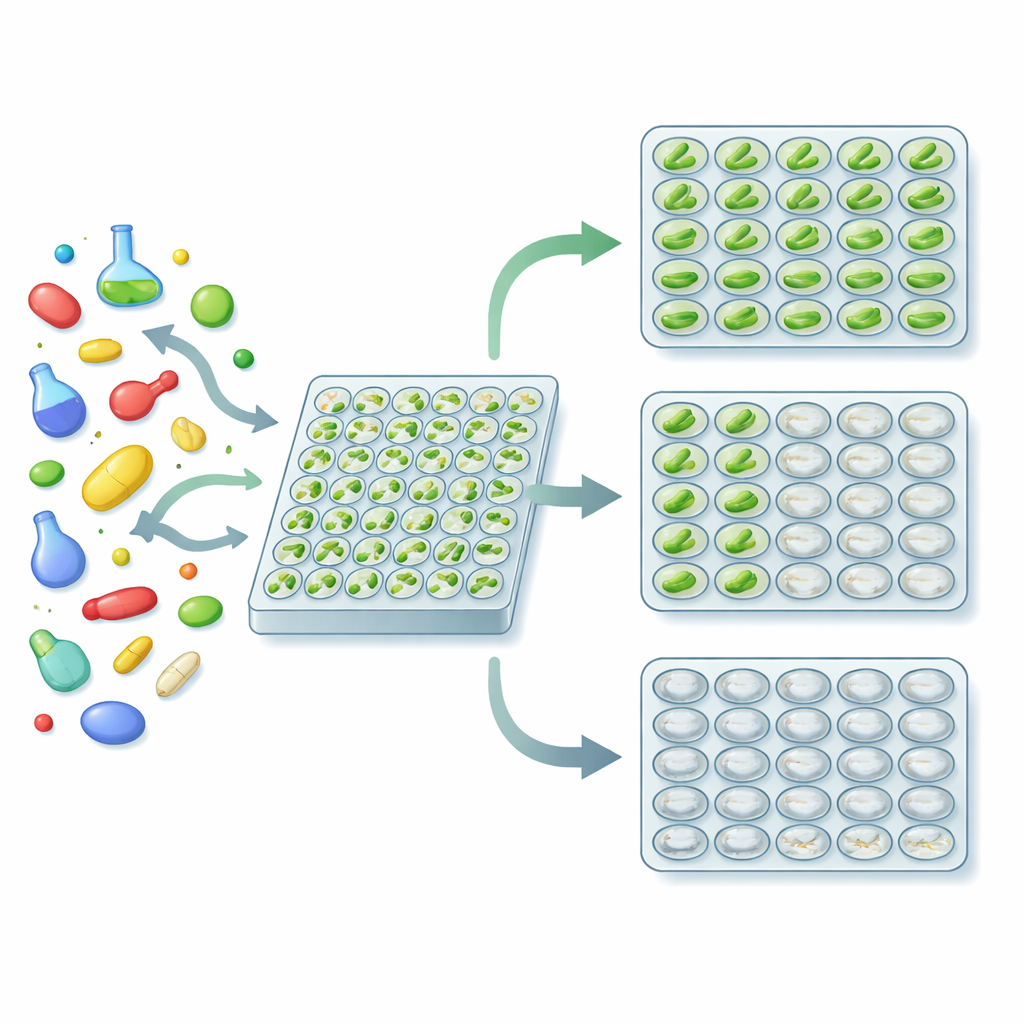
ثلاثة نتائج في اختبار واحد سهل
حوّل المؤلفون هذه البيولوجيا إلى فحص عالي الإنتاجية عملي. قاموا بزراعة الأيوجلينا في أطباق معيارية ذات 96 بئراً، وأضافوا مركباً مختلفاً لكل بئر، وانتظروا بضعة أيام. في النهاية، دخلت كل بئر بشكل موثوق في إحدى الحالات المرئية الثلاث: أخضر (المركب لم يفعل شيئاً مهماً)، أبيض لكن معتم (الخلايا نجت لكنها فقدت البلاستيدات، ما يشير إلى نشاط مضاد للبكتيريا)، أو شفاف (الخلايا قُتلت، مما يوحي بسُمية عامة). باستخدام قارئ أطباق يقيس مقدار الضوء الممتص في أطوال موجية مختلفة، حدّد الفريق حدوداً عددية تفرّق تلقائياً بين هذه الحالات. نسبة معينة بين الضوء الممتص في نطاقي الأحمر والأخضر من الطيف تشير إلى التبييض، بينما تقيس قوة الإشارة الكلية ما إذا كانت الثقافة قد نمت أصلاً.
اختبار الشاشة عملياً
لاختبار ما إذا كانت هذه المقاربة تعمل عملياً، تحدّى الباحثون الأيوجلينا أولاً بمكتبة تجارية مكوّنة من 79 مركباً موصوفاً جيداً. فرّق نظامهم القائم على اللون بوضوح بين الأدوية المعروفة بقدرتها على قتل الخلايا وتلك التي تتداخل بشكل محدد مع عمليّات من النوع البكتيري. أسبّع مركبات تسببت بالتبييض من دون القضاء على الثقافات. كانت معظم هذه مضادات حيوية كلاسيكية تعيق إنتاج البروتين أو الحمض النووي في البكتيريا، وتمثّل أسرًا كيميائية متميزة متعددة. ومن المهم أن ليس كل الأدوية من فئة واحدة تبيّض الأيوجلينا، ممّا يوضح أن الإرث البكتيري للبلاستيدة يتقاطع جزئياً فقط مع البكتيريا الحديثة. أعطت بعض المركبات أنماط امتصاص ضوئي غير عادية لأنها نفسها كانت ملونة، ما يذكّر المستخدمين أن الجزيئات ذات الصبغة القوية قد تتطلب فحصاً يدوياً للنتائج.
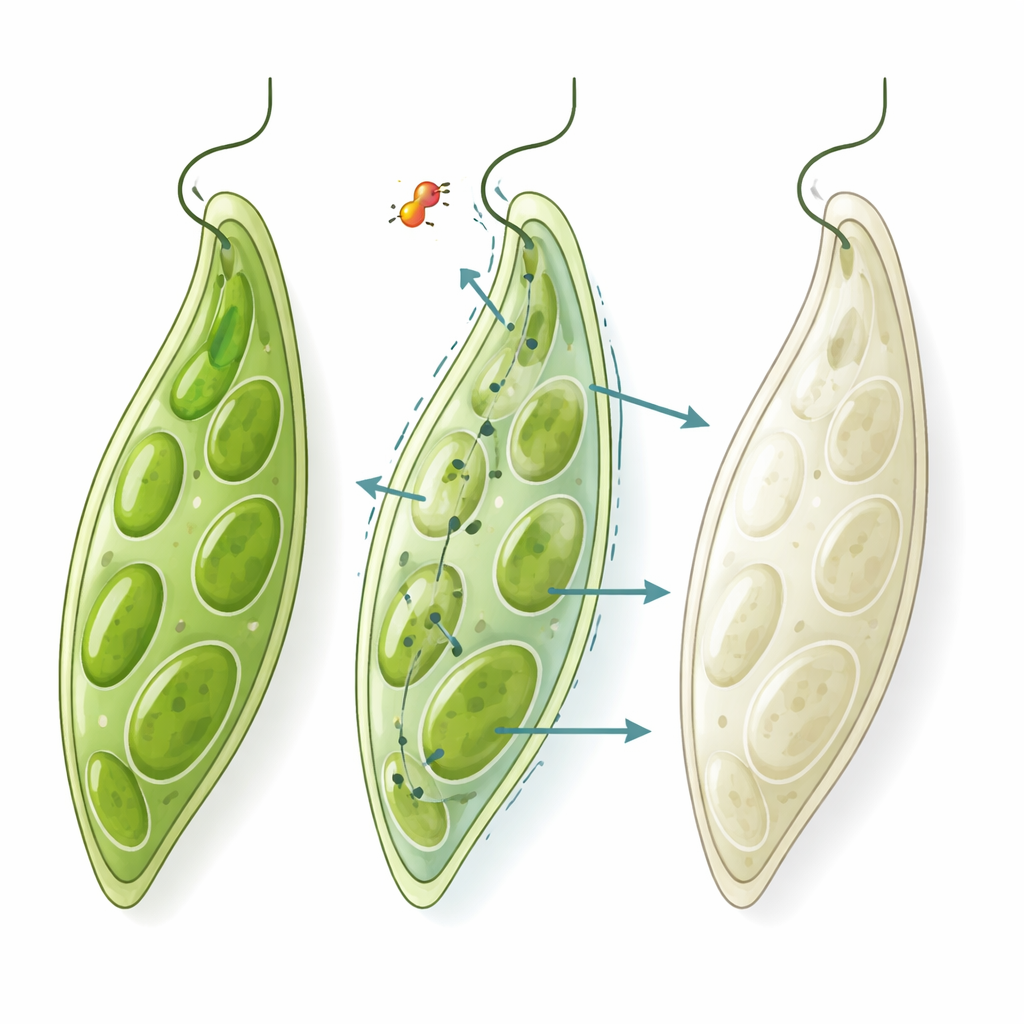
اكتشاف إشارات في المستقلبات الطبيعية
طبّق الفريق بعد ذلك الاختبار على 88 مركباً طبيعياً نادراً معزولاً من الميكسوبيكتيريا والفطريات، وهي كائنات معروفة بإنتاج جزيئات كيميائية غريبة. أوقف 18 مركباً نمو الأيوجلينا، متوافقاً مع آليات معروفة تؤثر في إنتاج الطاقة أو الهيكل الخلوي أو آليات إعادة التدوير الخلوية. اللافت أن مركباً واحداً — أرجيرين C، ببتيد حلقي من الميكسوبيكتيريا — تسبب في تبييض قوي بدلاً من القتل الصريح. يُعرف أن أرجيرين C يعيق عامل استطالة بروتيني يشارك في تخليق البروتين داخل الميتوكوندريا، وهي محطات طاقة الخلية التي تعود أيضاً أصولها إلى البكتيريا. أثبت تأثيره المُبيّض في الأيوجلينا أن الاختبار قادر على رصد آليات شبيهة بالمضادات البكتيرية تتجاوز الأدوية التقليدية المستهدفة للريبوسوم أو الحمض النووي.
وعود وحدود المقاربة
سيغفل هذا الفحص القائم على اللون بعض أنواع المضادات الحيوية المهمة. على سبيل المثال، الأدوية التي تهاجم جدران الخلايا البكتيرية لا تجد هدفاً في البلاستيدات وبالتالي تترك الأيوجلينا خضراء. حتى بين المركبات التي تعطل إنتاج البروتين، تسبب حوالي 40% فقط التبييض، ما يبرز المسافة التطورية بين البلاستيدات والممرضات الحديثة. من ناحية أخرى، تميّزت الطريقة بكونها رخيصة للغاية، متينة وسهلة القياس على نطاق واسع. تنمو الأيوجلينا في وسط بسيط من الملح والإيثانول بدون مصل حيواني، يمكن الحفاظ عليها لأسابيع مع رعاية بسيطة، ولا تتطلب سوى معدات مختبرية أساسية. وبما أن بلاستيدها مشتق من سلف غرام-سالب، فإن هذا الاختبار مناسب بشكل خاص لاكتشاف أدوية قادرة على اختراق الأغشية المتعددة النموذجية لبعض البكتيريا المقاومة المثيرة للقلق اليوم.
ما الذي يعنيه هذا للمضادات الحيوية المستقبلية
للمراقب العادي، تُظهر هذه الدراسة كيف أن مراقبة كائن أحادي الخلية يتحول من الأخضر إلى الأبيض يمكن أن توجه البحث عن مضادات حيوية الغد. اختبار الأيوجلينا ليس حلاً شاملاً لمشكلة مقاومة الأدوية، لكنه مرشح مبكر قوي: في خطوة واحدة يبرز جزيئات تبدو مضادة للبكتيريا، تبدو آمنة نسبياً للخلايا المعقدة، ويمكنها عبور حواجز غشائية متعددة. يمكن بعد ذلك نقل هذه النتائج الواعدة لاختبارات أعمق مباشرةً في البكتيريا الممرضة وخلايا الحيوانات. ومع استمرار ارتفاع حالات العدوى متعددة المقاومة عالمياً، قد تسرّع أدوات الفحص الذكية وغير المكلفة هذه الاكتشاف من خلال تمكين العلماء من تركيز الموارد النادرة على أبرز المرشحين.
الاستشهاد: Pereira, L., Löffler, LS., H. Kirsch, S. et al. Euglena gracilis as a high-throughput screening platform for antibacterial activity, cytotoxicity and membrane permeability in a one-step and cost-effective assay. J Antibiot 79, 376–385 (2026). https://doi.org/10.1038/s41429-026-00911-5
الكلمات المفتاحية: اكتشاف المضادات الحيوية, الفحص عالي الإنتاجية, أيوجلينا غراكيلس, مقاومة الأدوية, المستقلبات الطبيعية