Clear Sky Science · zh
小鼠卵巢炎性老化的多细胞起源
为什么卵巢的老化重要
人们比以往任何时候都更晚生育,但我们的卵巢并未随这种社会变化同步。随着女性年龄增长,生育力下降,流产和并发症的风险上升。科学家们知道卵巢会变得更纤维化、更发炎,支持健康卵子的能力也下降,但具体的微观机制一直难以确定。本研究利用强大的新型基因图谱工具,构建了小鼠老化卵巢的细胞级图谱,揭示免疫细胞如何进入、细胞间通信如何改变,以及这种缓慢、持续的炎症——称为“炎性老化”——如何出现。
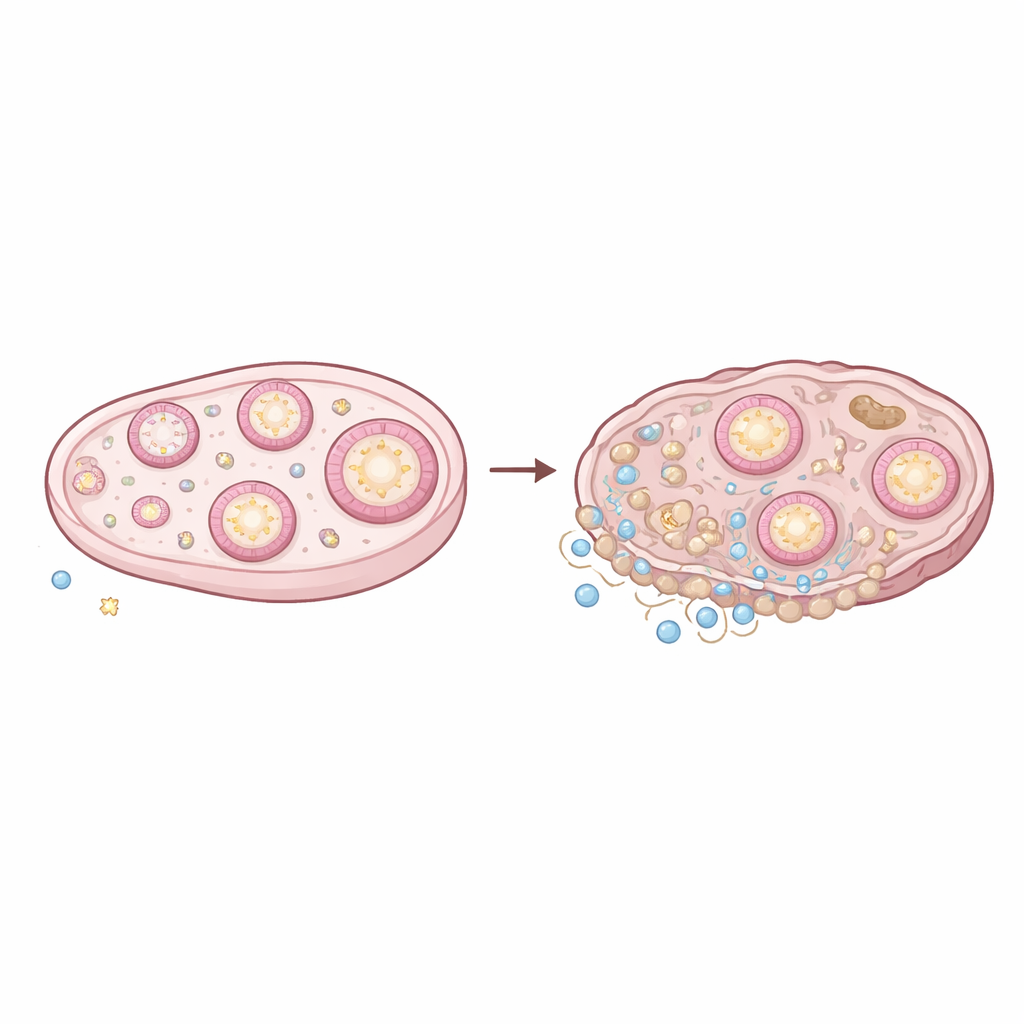
仔细审视老化的卵巢
卵巢是一个不断重塑的器官:滤泡生长与消亡,排卵造成每月一次的“创伤”,暂时性结构黄体出现后又退化。为了观察这一动态组织随年龄的变化,研究人员使用单细胞RNA测序分析了来自年轻(3个月)和年老(14个月)小鼠卵巢的数千个单细胞,读取每个细胞中哪些基因被激活。随后他们将这些信息与空间转录组学叠加,后者可将基因活动映射回组织的物理位置。两种方法结合,生成了年轻与老化卵巢中细胞类型、位置及相互交流的详细图景。
免疫细胞进入并加剧炎症
最明显的年龄相关变化之一是免疫细胞激增。虽然巨噬细胞(组织常驻的清道夫细胞)的总体数量并未猛增,但其构成发生了改变,向更具促炎和促进纤维化的类型转变。研究组辨识出与老化相关的瘢痕相关巨噬细胞以及一类标记有激活受体(Cd300e)的巨噬细胞,这两类在其他器官中已知会驱动慢性炎症和疤痕形成。淋巴细胞——T细胞和B细胞——的扩增更为显著。与慢性炎症性疾病相关的T细胞亚群,以及在失调时可触发纤维化的先天淋巴样细胞,变得更为常见。这些免疫细胞通过众所周知的炎症通路发出更强的信号,包括肿瘤坏死因子(TNF)和招募、激活更多免疫细胞的趋化因子网络,从而建立起自我强化的循环。
卵巢支持细胞的变化
卵子并非孤立地老化;它们依赖周围的颗粒细胞,这些细胞构成滤泡的主体。通过将颗粒细胞分成对应不同滤泡阶段的亚型,并映射它们在组织中的位置,研究人员显示出老化改变了这些细胞的组成和行为。年老卵巢中早期阶段的颗粒细胞相对减少,而晚期和退化(闭经性)颗粒细胞增多,反映出滤泡库的减少。重要的是,与健康滤泡生长相关的基因活动——例如参与激素生成、脂质代谢和早期发育的信号——随年龄下降。与此同时,靠近卵巢间质边界的外层颗粒细胞增强了吸引并激活免疫细胞(尤其是巨噬细胞)的信号。

有利于纤维化的互作网络
通过追踪哪些细胞类型发送和接收特定分子信号,作者揭示出一个密集的、依赖年龄的通信网络。间质成纤维细胞和颗粒细胞发送更多招募巨噬细胞并引导其朝促纤维、成瘢痕状态转变的信号。反过来,老化相关的巨噬细胞增加了刺激成纤维细胞沉积胶原和其他基质蛋白的因子,使卵巢更僵硬、更纤维化。淋巴细胞与巨噬细胞也交换促进其存活、运动和炎性活性的信号,暗示存在正反馈环。例如,B细胞和T细胞强化了增强抗原呈递和免疫激活的通路。总体而言,这一网络分析显示曾经为卵子提供良好支持的微环境如何逐渐被慢性炎症和瘢痕组织主导。
这对生殖健康意味着什么
通俗地说,这项工作表明老化卵巢慢慢从一个滋养卵子的器官转变为一个以免疫为中心的、发炎的组织。曾经专注于养护和协调卵子的颗粒细胞开始更像是吸引免疫细胞的灯塔。专门化的巨噬细胞和T细胞反过来维持炎症和纤维化,使滤泡更难以正常发育和排卵,并可能降低卵子质量。尽管该研究在小鼠中进行,但许多相同的细胞类型和通路在人类中也存在,这提示通过针对这些炎症和纤维化回路——而不仅仅是卵子本身——可能开辟延缓生殖健康衰退并减轻更广泛绝经相关健康影响的新策略。
引用: Galligos, A., Varberg, J.M., Yueh, WT. et al. Multicellular origins of murine ovarian inflammaging. Commun Biol 9, 593 (2026). https://doi.org/10.1038/s42003-026-09826-1
关键词: 卵巢衰老, 炎性老化, 免疫细胞, 颗粒细胞, 生育力下降