Clear Sky Science · zh
使用临床获取的核心活检进行胃肠肿瘤的个性化信号通路分析以实现患者分层和药物靶点评估
这项研究对患者的重要性
癌症医生越来越努力根据每位患者肿瘤的独特生物学特征来匹配治疗。对于消化系统癌症——例如胰腺、结肠、肝脏或胆管的癌症——这点尤为紧迫,因为这些癌症常见、常常被晚期诊断且难以治疗。本研究探索了一种新的实验室方法,能够从微小的活检样本中读取大量与癌症相关蛋白的活性,目标是帮助医生为个体患者选择更精确的治疗方案。
从 DNA 列表到活体信号
目前,大多数“个性化”癌症治疗都依赖于读取肿瘤中的 DNA 变化。尽管这种方法很强大,但单靠 DNA 并不能显示细胞内哪些信号实际上被开启并推动肿瘤生长。这些信号由蛋白质承载,其中许多可被药物直接作用。研究人员使用了一种名为 DigiWest 的高通量技术,这是经典免疫印迹(Western blot)的现代变体,可一次测量约 130–200 种蛋白及其活化形式。重要的是,该方法所需的样本量仅相当于一次针刺活检,使其适用于真实临床环境。
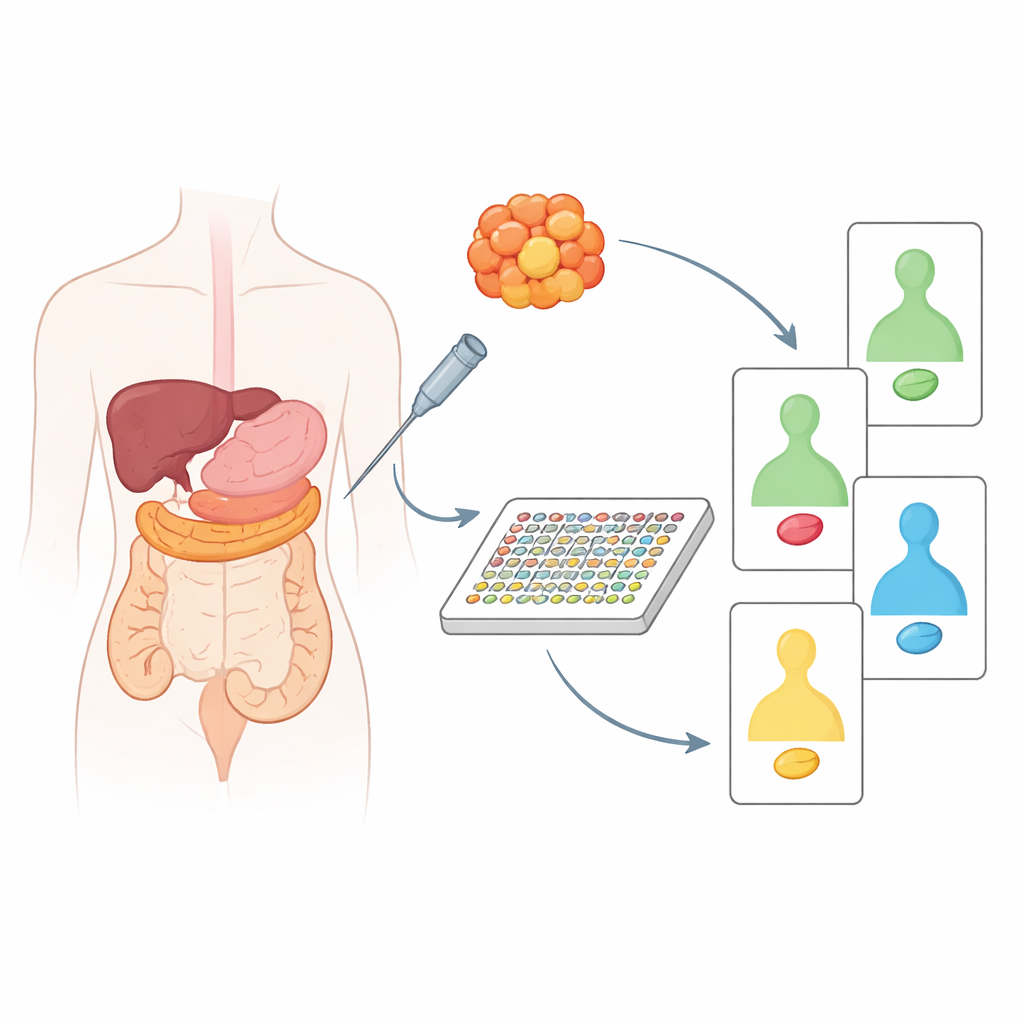
将肿瘤组织与其健康邻近组织进行比较
研究团队首先分析了 20 名胰腺或结直肠癌患者的保存组织样本,并始终将肿瘤样本与同一患者的邻近非癌组织配对。通过将肿瘤与其自身健康对照进行比较,他们能够识别出真正被癌症改变的蛋白,而不是仅反映器官间的正常差异。这揭示了许多知名癌症守护基因和驱动因子(如 p53、Ras、PTEN 等)在行为上的明显对比。例如,胰腺肿瘤往往表现出增强的促生长信号和保护性蛋白的丧失,而结肠肿瘤则呈现出其自身特有的通路紊乱模式。当研究人员根据这些蛋白变化对样本进行聚类时,可以将胰腺癌分为两个生物学上不同的组,并在结肠癌中检测到与患者年龄和肿瘤在肠道内位置相关的有意义差异。
个体肿瘤的“信号条码”
超越群体平均值,科学家为每个肿瘤构建了详细的蛋白质档案。这些档案突出了哪些信号通路(例如涉及 mTOR、MAPK/Erk、Wnt 或免疫相关因子的通路)特别活跃或被关闭。许多被测蛋白是现有药物的直接靶点,或位于这些靶点的下游,使研究团队能够推断出哪些药物可能干扰肿瘤的主要生长引擎。在回顾性病例中,四分之三的样本中他们能够指出一个或多个可能推动肿瘤进展的通路。他们还识别出富含免疫细胞标志物的肿瘤,提示可能对免疫治疗有反应的“热”肿瘤,以及一些具有显著独特签名的罕见病例。
将该方法应用于真实患者
为了测试其在临床床边的实用性,研究人员随后将 DigiWest 应用于 14 名正在由分子肿瘤委员会评估的不同胃肠道癌症患者的新鲜针刺活检样本。这些患者病史复杂,并且常有既往治疗。由于无法获得配对的健康组织,每个肿瘤的蛋白水平被与组内中位水平比较,以定义何为异常偏高或偏低。即使在这种更严格的设置下,14 个肿瘤中有 12 个显示出清晰且与治疗相关的通路活性模式。在两个详细示例中,蛋白质数据证实了结肠癌中 FGFR2 基因的 DNA 水平扩增以及肝癌中 mTOR 抑制机制的丧失,强烈支持委员会考虑使用抑制 FGFR 或抑制 mTOR 的药物。总体而言,DigiWest 的发现与关键遗传驱动因素一致,并在大多数可评估病例中提示了潜在的药物靶点。
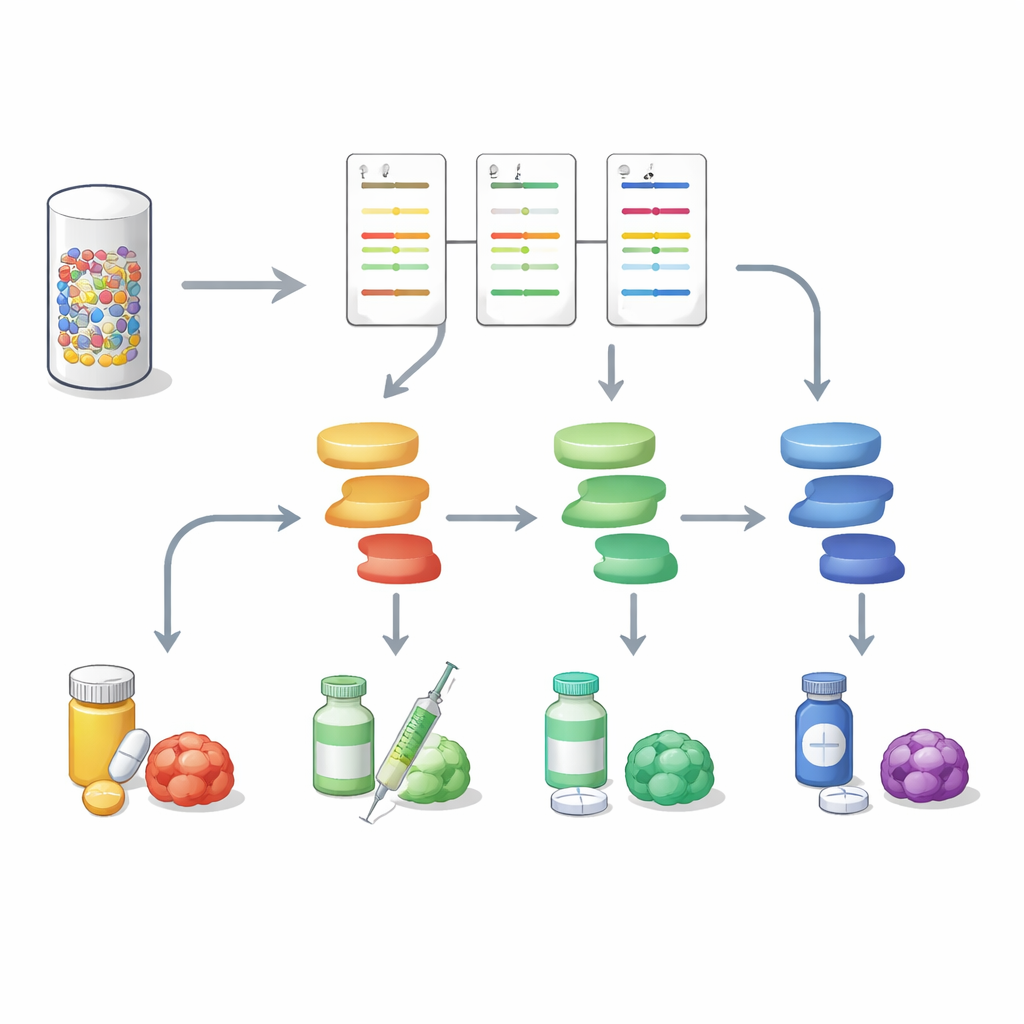
迈向更完整的肿瘤画像
这项工作表明,将蛋白质信号分析与 DNA 测序并行进行,可以提供对胃肠道肿瘤更丰富且更具可操作性的图像。通过将微小活检转化为多通路活性地图,DigiWest 有助于区分在特定肿瘤中哪些分子开关确实被打开,以及哪些药物可能最佳地干预它们,同时也可能标出新出现的耐药路径。尽管仍需更大规模的研究,该方法为将高内涵蛋白质谱分析引入日常精准肿瘤学提供了一条务实之路,并推动实现基于每位患者“活体”肿瘤而不仅仅是其遗传蓝图的个体化治疗方案。
引用: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
关键词: 精准肿瘤学, 胃肠道癌症, 蛋白质组学, 活检分析, 靶向治疗