Clear Sky Science · zh
在胶质母细胞瘤标本中,不同标记的微小胶质细胞特异性被覆盖
这对脑癌为何重要
医生和研究者正试图利用大脑自身的免疫细胞去对抗像胶质母细胞瘤这样致命的肿瘤。但在肿瘤内部,两类密切相关的细胞会混在一起:驻留的大脑防御细胞称为小胶质细胞,而游走的免疫细胞称为巨噬细胞。许多新疗法依赖于分辨这两类细胞。本研究显示,在胶质母细胞瘤中,用来标记小胶质细胞的几种最常用的“识别标签”不再可靠,这一警示可能重新塑造科学家解读脑肿瘤数据和设计治疗策略的方式。
大脑的守护者
在健康的大脑中,小胶质细胞静静巡逻组织,清理碎片并应对损伤。相比之下,巨噬细胞来自骨髓,通常驻留于身体其他部位,但在发生损伤或疾病时会涌入大脑。在胶质母细胞瘤中,这两类细胞可占肿瘤质量的半数左右。有些细胞可能帮助肿瘤生长并规避免疫疗法,而另一些则可能抑制肿瘤。要理解它们的作用,研究者需要在真实组织中(而不仅是基因列表上)有清晰、可操作的方法来区分小胶质细胞和巨噬细胞。
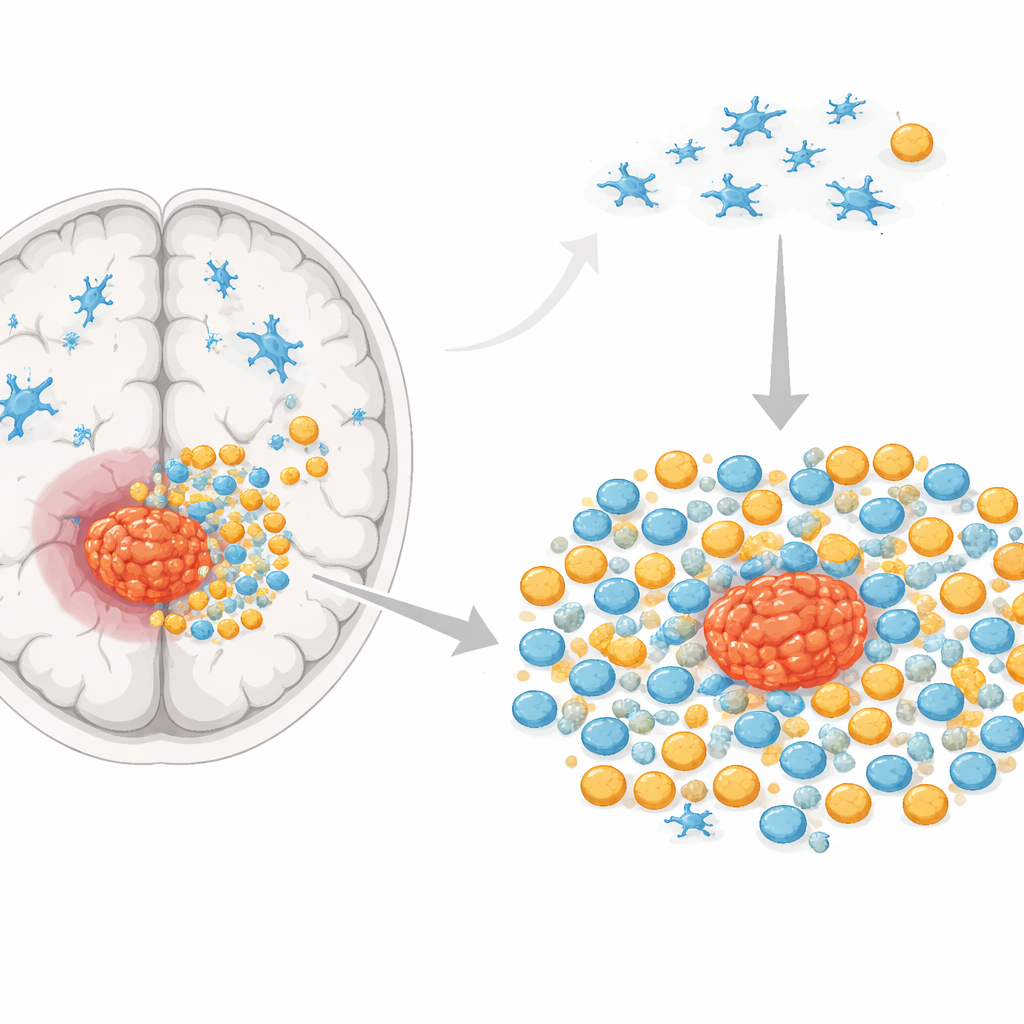
在健康大脑中有效的标记
过去十年,强大的单细胞方法表明某些分子几乎只由小胶质细胞产生。尤其有四个——SALL1、TMEM119、P2RY12 和 HEXB——已成为研究中广泛使用的“仅限小胶质细胞”标记。作者检验了这些标记在人体和小鼠脑切片中在蛋白水平上的表现,使用荧光染色。在癫痫患者组织和健康小鼠组织中,四个标记中有三个(SALL1、TMEM119 和 P2RY12)确实出现在大多数小胶质样细胞上,而 HEXB 的一致性较差。这支持了在近乎正常条件下,这些标签可以较好地区分小胶质细胞的观点。
肿瘤如何模糊细胞身份
在胶质母细胞瘤的小鼠模型中,情况发生了显著变化。当肿瘤细胞植入大脑后,研究团队绘制了这些标记的表达位置:远离肿瘤的组织、肿瘤边缘以及肿瘤核心内部。四个标记在肿瘤周围和内部都能检测到,但其分布发生了变化。SALL1、TMEM119 和 P2RY12 在肿瘤边界附近表达强烈,而在肿瘤内部则急剧下降,使许多免疫细胞失去了这些本应定义小胶质细胞的标签。HEXB 在各区域均表现弱且不连续。染色还出现在没有通用髓系标记的细胞上,提示某些肿瘤细胞自身也可能表达这些分子。
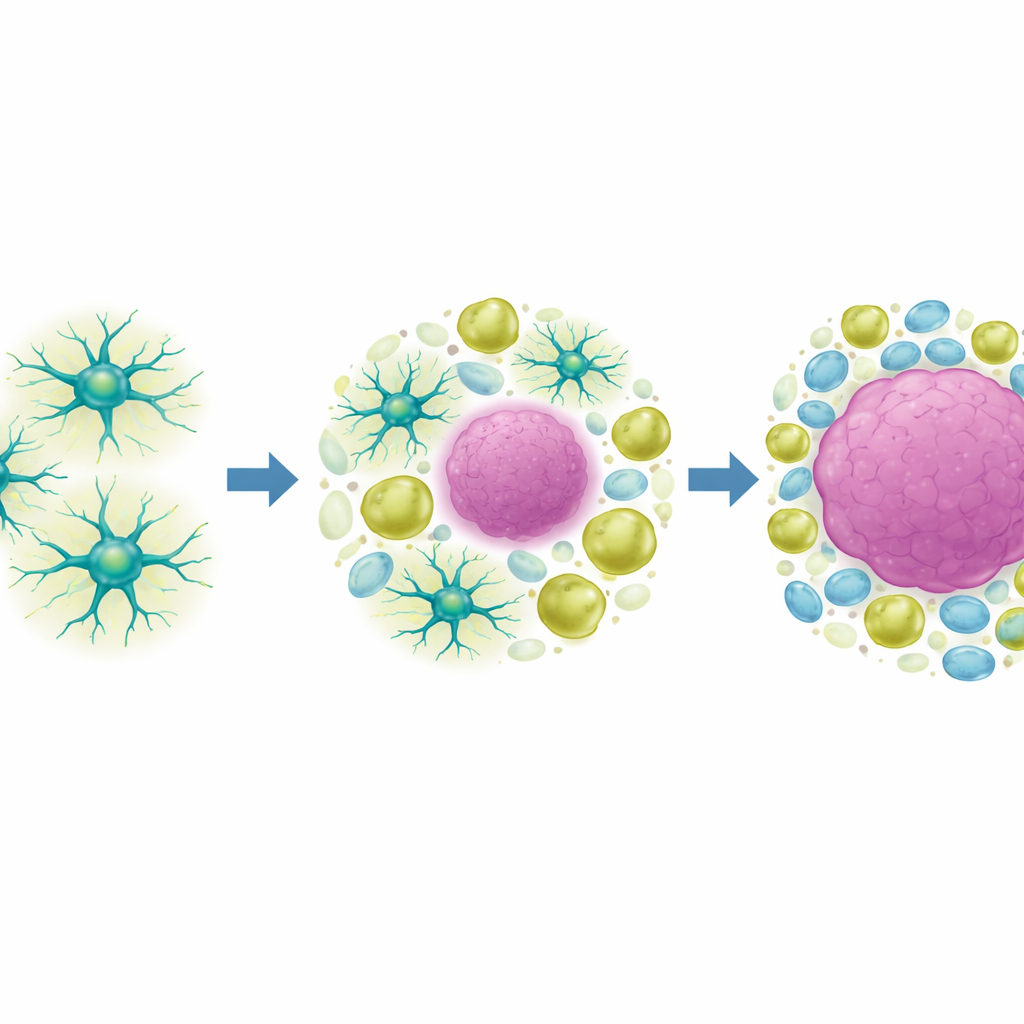
巨噬细胞也获取“仅小胶质细胞”标签
为明确哪些细胞是哪类,研究者构建了骨髓嵌合小鼠,这种技术用荧光信号标记所有进入的巨噬细胞,同时保留驻留小胶质细胞不被标记。在这些动物中,他们可以在同一肿瘤中并排直接观察到小胶质细胞和巨噬细胞。与预期相反,两类细胞在相似的区域表达了 SALL1、TMEM119 和 P2RY12,尤其是在肿瘤核心外部。在肿瘤内部,携带这些标记的无论哪类细胞都只占少数。在体外培养中,原代小胶质细胞和骨髓来源的巨噬细胞都产生这四种标记,且将小胶质细胞系暴露于肿瘤条件培养液后,其 SALL1、TMEM119 和 P2RY12 水平下降——这与在肿瘤中观察到的标记信号丧失相呼应。
在癌症中重新思考小胶质细胞的识别
综合来看,这些发现表明在胶质母细胞瘤的背景下,这四种分子不能被视为小胶质细胞的专属识别标志。肿瘤环境导致小胶质细胞丧失这些标记,而巨噬细胞甚至肿瘤细胞也可能获得它们,有效抹去了早期基因表达研究所暗示的清晰界限。对于非专业读者来说,信息是:在脑癌中,免疫细胞高度可塑,会根据肿瘤环境改变它们的“表面徽章”。研究者在开发和测试新的胶质母细胞瘤疗法时,需要采用更复杂、考虑情境的策略——例如命运追踪模型或标记组合——而不是依赖任何单一标签来区分小胶质细胞和巨噬细胞。
引用: Bungert, A.D., Sanchin, A., Blank, A. et al. Microglia-specificity of different markers is overridden in glioblastoma specimens. Sci Rep 16, 14687 (2026). https://doi.org/10.1038/s41598-026-52315-y
关键词: 胶质母细胞瘤, 小胶质细胞, 巨噬细胞, 脑肿瘤免疫, 细胞标记