Clear Sky Science · zh
运动与限时和/或饮食联合改善饮食致肥小鼠的肝脂质稳态
日常习惯为何对肝脏至关重要
肥胖常以腰围和体重秤上的数字来讨论,但它也在悄然重塑我们最重要的器官之一:肝脏。当肝脏内脂肪积聚过多时,人可以发展为一种现在称为代谢功能相关性脂肪肝病(MASLD)的疾病,这会增加糖尿病、心脏病和肝衰竭的风险。这项小鼠研究提出了一个与日常生活直接相关的实用问题:如果你已经因饮食而肥胖,通过改变饮食内容、进食时间和活动量,能在多大程度上逆转肝脏损伤并恢复肝细胞内更健康的脂肪处理?
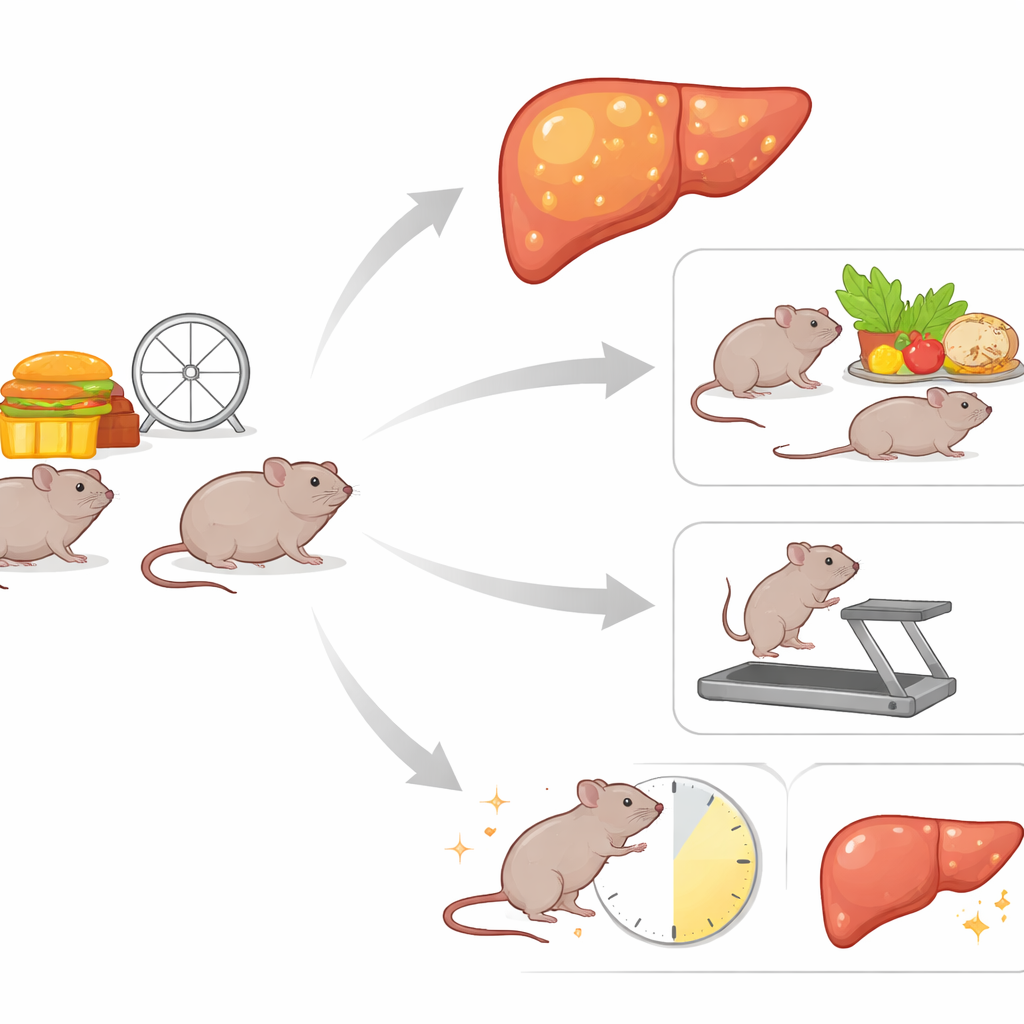
研究如何设计
研究者先让幼年雌性小鼠食用极高脂肪饮食六个月,足以使其肥胖并给肝脏造成压力。经过这一“诱导”期后,动物被分为六组,继续观察另一个六个月。一组保持高脂饮食不变。其他组则在持续高脂饮食的同时加入跑步机运动,或同时加入跑步机运动与限时进食(仅在夜间活动期提供食物),或者改为低脂饮食并分别有无相同的附加干预。这样的设计使团队能够比较仅改变饮食、运动和进食时间窗口以及它们组合对体重、血液中肝损伤标志物、详细的肝脏脂质组成以及控制肝脏合成和燃烧脂肪的关键基因活性的影响。
体重下降、肝脏损伤与简单血检
从高脂改为低脂饮食对体重的影响最大:改变饮食的小鼠在研究结束时体重约为持续高脂组的一半。单独的运动或限时进食在持续高脂饮食时并未引起显著减重,但二者结合则产生适度下降,暗示将进食时间与动物的自然昼夜节律对齐有助于代谢,即便食物类型未变。相同的模式也出现在常规肝功能血检中。持续高脂饮食的小鼠血液中AST和ALT水平较高——这些酶在肝细胞受损时会渗入血中。加入跑步机运动,尤其是加入限时进食,使这些水平向正常方向回落,而改为低脂饮食的降幅最大。由肝脏合成的白蛋白维持在典型范围内,表明器官的基本合成功能在损伤标志改善的同时仍然保持完好。
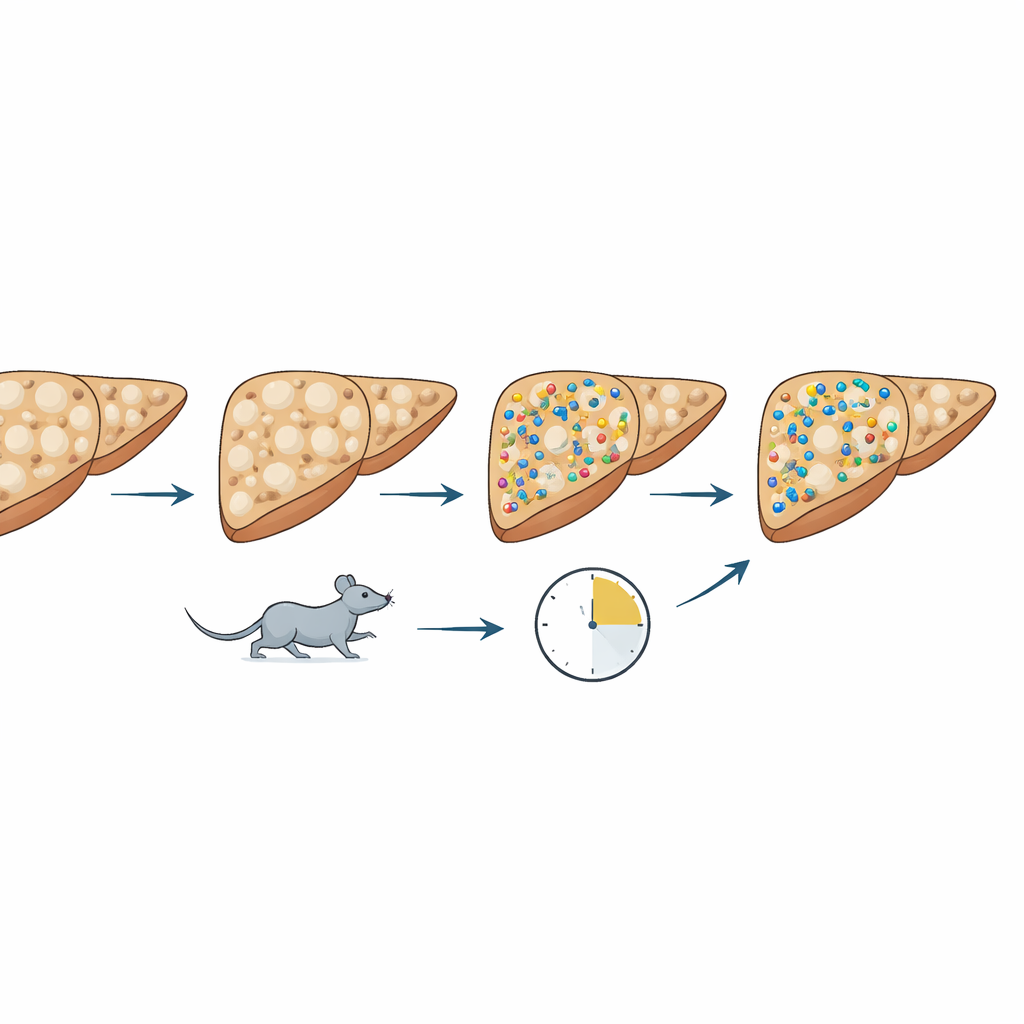
肝脏脂质格局内部发生了什么变化
除了总脂质量外,研究团队使用脂质组学——一种可以同时列出多种单独脂类化合物的化学工具包——来观察肝脏“脂质景观”如何转变。高脂饮食扭曲了这一景观,促使某些种类的脂质增加,例如已与胰岛素抵抗和肝功能障碍相关的特定鞘脂类和磷脂类。当小鼠改为低脂饮食——尤其是与跑步机运动结合时——脂质的平衡再次发生变化。鞘磷脂及其密切相关的二氢鞘磷脂以及溶血磷脂酰胆碱和磷脂酰胆碱的水平上升,显示出细胞膜在肝脏恢复过程中可能的重塑。重要的是,许多这些脂质种类与AST和ALT呈负相关:当它们增加时,肝损伤的迹象减少,提示其中至少一些变化属于愈合反应的一部分,而非新的损害形式。
肝脏“控制开关”如何响应
研究者还测量了作为脂肪处理控制开关的基因活性——有些基因促进新脂肪和胆固醇的合成,另一些则促进将脂肪燃烧以供能。在饮食改变加上运动与限时进食的条件下,驱动脂肪合成的基因(例如由固醇调节因子和肝X受体调控的基因)趋向下调。与此同时,与线粒体和过氧化物酶体中脂肪氧化相关的基因显示出更为复杂的反应:在某些仍然高脂且有运动的组中,它们的活性相对较高,可能反映肝脏试图应对持续的脂肪过载,而在低脂组中,随着总体脂肪压力的缓解,这些基因的活性则可放松。总体模式表明,并非单一开关被切换,而是肝脏在脂肪储存、分解和输出之间进行广泛的再调节。
对人类和未来研究的意义
对普通读者而言,主要信息很直接:改变你吃什么仍然是逆转与肥胖相关的肝脏压力的最有力方式,但运动和一致的日常进食时间窗口也能带来有意义的益处——即使不健康的饮食尚未完全纠正。在这些小鼠中,将低脂饮食与规律的跑步机运动和夜间限时进食相结合,改善了体重、降低了血液中肝损伤的指标,并使肝细胞内的脂质组成和调控基因朝向更健康的状态调整。此项工作为探索性且在动物身上进行,因此并不为人类规定具体方案。不过,它强调了一个令人鼓舞的原则:肝脏具有显著的可塑性,协调的饮食、运动和进食时间改变可以帮助在多年超负荷后将其重新推回平衡。
引用: Guerra, N.P., Bräuer, A.U., Gräler, M.H. et al. Exercise and time-restricted and/or dietary feeding jointly improve hepatic lipid homeostasis in diet-induced obese mice. Sci Rep 16, 10508 (2026). https://doi.org/10.1038/s41598-026-45394-4
关键词: 脂肪肝, 限时进食, 运动, 高脂饮食, 脂质代谢