Clear Sky Science · zh
果蝇酪胺β-羟化酶基因对酒精耐受性必不可少
为什么小小的果蝇和酒精能讲出大故事
人类并不是唯一会对酒精产生反应或随着时间对其效应产生耐受性的生物。该研究转向谦卑的果蝇,旨在揭示单一脑内化学通路如何帮助动物应对反复的酒精暴露。通过剖析这一过程背后的遗传学和神经回路,工作阐明了大脑如何将既往经验转化为行为改变,以及单个基因的细微变化如何同时影响应激反应和运动的驱动力。
多面性的脑内信使
研究的核心是酪胺β-羟化酶,或称 Tbh,这一基因使果蝇能够生成壳碱(octopamine),这种信号分子与脊椎动物的类肾上腺素信使相关。早期工作显示,完全缺乏壳碱的果蝇在生育能力上存在困难,运动启动不良,并对乙醇表现出异常反应。在本研究中,作者首先探问 Tbh 基因本身的结构。他们发现该基因至少产生四种不同的RNA转录本,进而编码三种略有差异的Tbh蛋白。这些不同版本主要在可能受磷酸“开关”调控的区域有所差异,提示细胞可在发育过程中或在应激下对该酶的活性进行精细调整。
构建更强的失功能突变体
一种广泛使用的Tbh突变体,称为 TbhnM18,检测不到壳碱,但新的分析显示其DNA变化并未移除某些Tbh蛋白的起始点,且仍保留有减少量的转录本。为创造更干净的失功能等位基因,研究团队通过重组技术删除关键起始外显子,构建了新的等位基因 TbhDel3。这个较大的缺失显著降低了Tbh转录本水平并去除了大部分蛋白编码能力,同时保留了一个起始更下游的异常转录本。比较原始与新突变体使研究者能够分辨哪些行为是真正依赖于Tbh功能的。
酒精耐受、应激与运动
作者使用一种“醉态计”(inebriometer)柱来测量果蝇在乙醇蒸气中保持平衡的时长,并测试不同基因型对酒精的适应能力。正常果蝇在首次暴露后会变得更具抵抗力,这一现象称为功能性乙醇耐受。TbhDel3 和 TbhnM18 的雄性在初始敏感性上表现正常,但在第二次暴露后耐受性明显降低,表明行为适应方面存在特异性缺陷,而非基本运动控制问题。然而在多次重复或慢性给药后,即便是突变体最终也会与对照趋同,说明依赖于Tbh和非依赖Tbh的耐受形式并存。两种突变体在热应激下表现不同:在乙醇处理前短暂热冲击使对照与 TbhnM18 果蝇更具抵抗力,但却降低了 TbhDel3 果蝇的抵抗力,这暗示某些Tbh转录本或蛋白形式对应激诱导的保护尤为重要。对行走和爬行的平行测试显示,在被强烈驱动下——比如以盐作为不愉快的刺激或为了离开食物寻找蛹化地点——突变体的移动距离可与或超过正常果蝇。它们的问题不在于运动本身,而在于何时以及以多大强度去做出反应的决策。
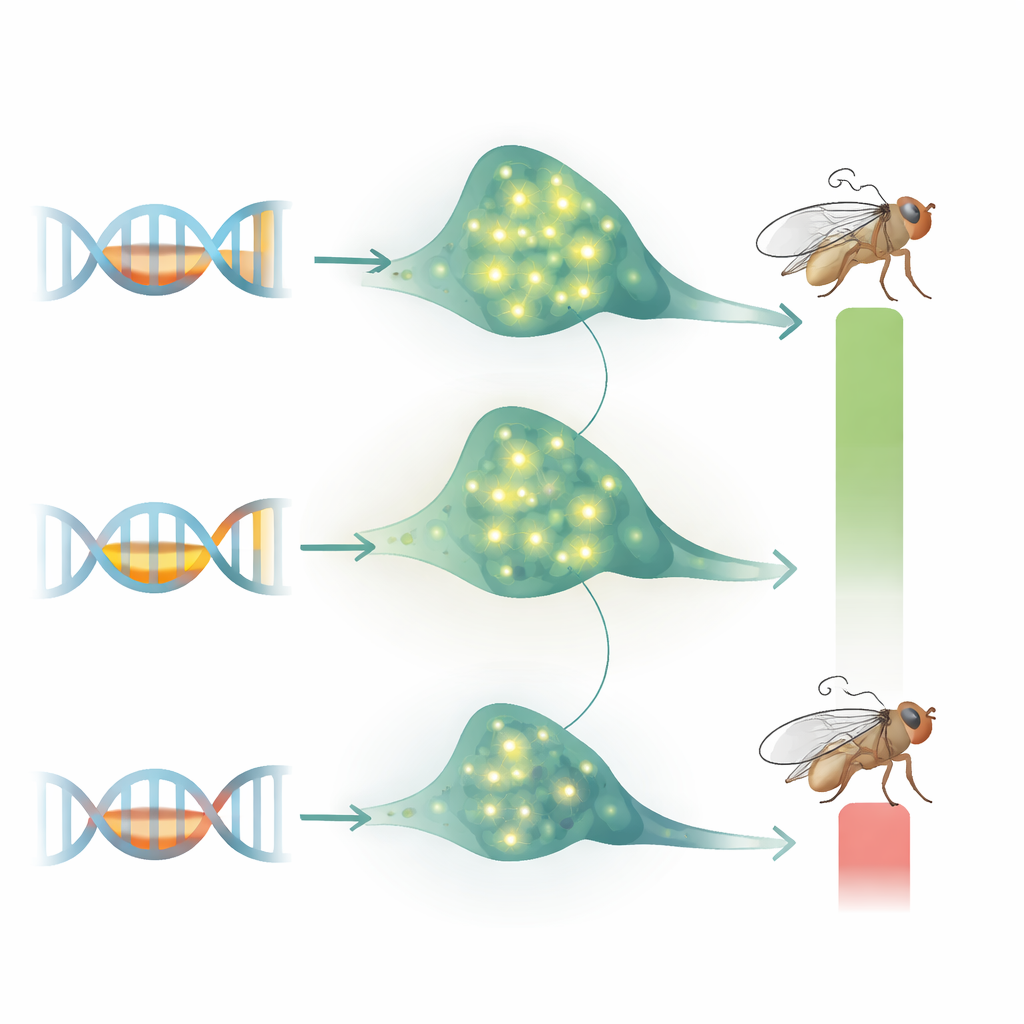
定位关键神经元
下一个问题是 Tbh 在神经系统的何处必须发挥作用以实现乙醇耐受。通过仅在成虫中打开一个热诱导的 Tbh 基因,研究者在 TbhnM18 突变体中恢复了正常的耐受性,证明成虫期而非发育期的表达至关重要。随后他们使用一系列遗传驱动系在选定的神经元群中重新开启 Tbh。令人惊讶的是,标记许多已知壳碱细胞(包括先前被证明控制对乙醇先天吸引的那些细胞)的驱动器未能挽救耐受性,这表明嗜好与耐受依赖于不同的回路。新构建的 4.6-Tbh-Gal4 驱动器标记了一组受限的大脑和腹侧神经索神经元,当用它在突变体中表达 Tbh 时确实恢复了耐受。然而在野生型中用同一驱动器过表达 Tbh 会降低耐受,显示出酶的过多或过少均有害,壳碱水平必须被严格平衡以实现恰当的适应。
这对大脑与酒精意味着什么
综合来看,研究结果表明,负责合成一种脑内信使的单一酶可被多种基因版本及蛋白水平的开关所控制,并且该酶在一小部分成虫神经元中的活性对于学会抵抗酒精的效应至关重要。Tbh 的缺失并非削弱了基本运动能力,而是破坏了果蝇利用既往经验和不断变化的内部状态来调整行为的能力,包括其对酒精和应激的反应。鉴于昆虫中的壳碱与脊椎动物的去甲肾上腺素相似,这项工作提示,在更复杂的大脑中,对相关通路的类似精细调控可能会影响其如何处理反复暴露于药物、应激及其他强烈经历的能力。
引用: Ruppert, M., Hampel, S., Claßen, G. et al. The Drosophila tyramine beta-hydroxylase gene is required for ethanol tolerance. Sci Rep 16, 12180 (2026). https://doi.org/10.1038/s41598-026-45082-3
关键词: 果蝇 酒精 耐受性, 壳碱能(octopamine)信号传导, 神经递质 基因, 应激 与 酒精, Drosophila 行为