Clear Sky Science · zh
整合机器学习与多组学分析识别 ALOX5 作为糖尿病肾病肾小管间质炎症的潜在治疗靶点
这对糖尿病患者为何重要
很多糖尿病患者会担心自己的肾脏状况,但多数解释集中在血糖和血压上。本研究更深入地探查随着损伤发展,肾组织内部到底发生了什么。通过结合大数据、单细胞分析和实验室成像,研究者锁定了免疫细胞内的一个特定炎性开关,该开关可能可被一种天然化合物关闭,从而有望为糖尿病肾脏保护开辟新途径。
更细致地看糖尿病引起的肾损伤
医生长期以来知道糖尿病肾病可导致肾功能衰竭,但注意力常集中在称为肾小球的微小滤过结构上。然而,最近的证据表明,滤过结构之间的间质和处理尿液的小管区域在预测肾功能下降速度方面可能更为重要。在这些区域,免疫细胞大量浸润、驱动炎症并遗留瘢痕。作者旨在识别在这些炎性组织中,哪些基因可能充当有害免疫反应的主控开关。
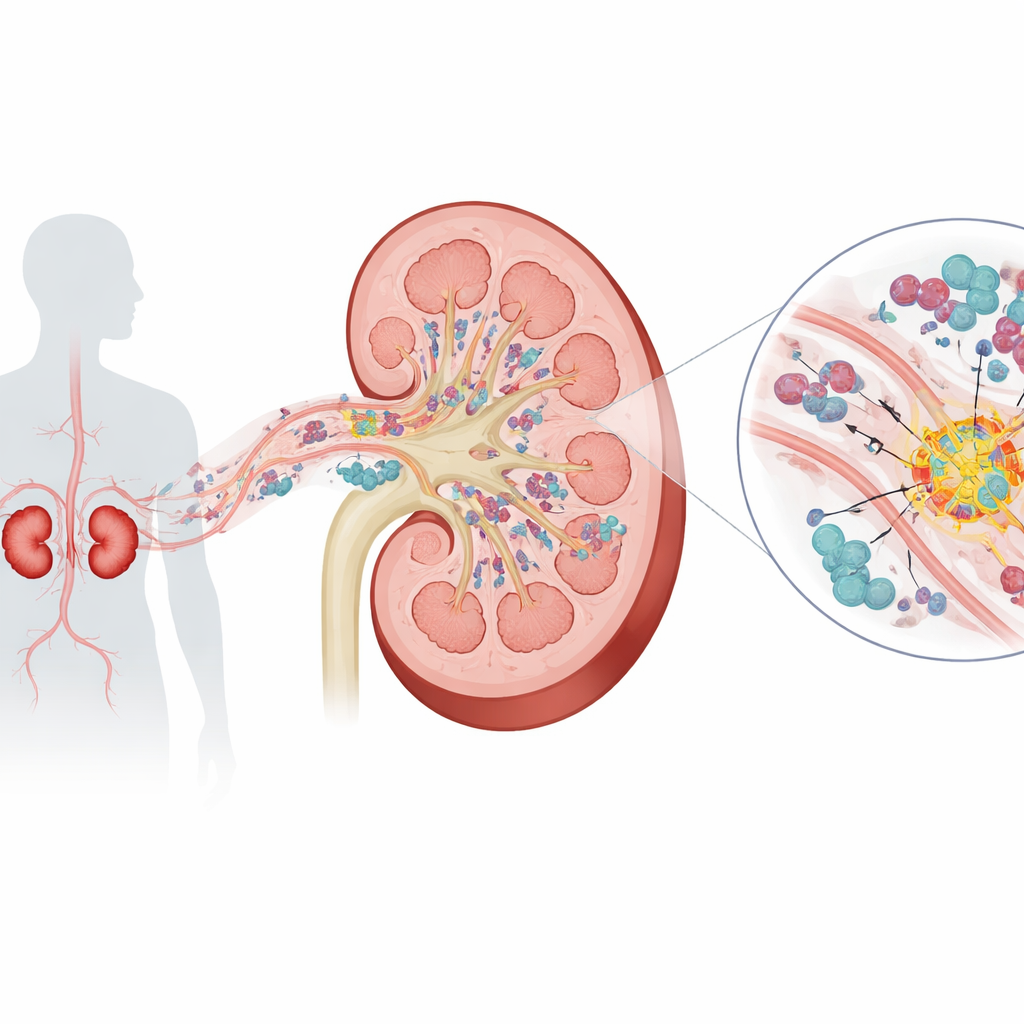
在肾脏免疫细胞中发现一个炎性开关
为寻找这些开关,团队汇总了若干公开的来自有无糖尿病肾病患者肾小管样本的基因表达数据集。利用按基因共表达模式分组的方法,并应用两种独立的机器学习策略,他们将数千个基因缩减到一个突出候选:ALOX5。该基因编码一种将脂类分子转化为白三烯的酶,白三烯是强效的化学信使,能够吸引并激活免疫细胞。在多个患者群体中,病变肾脏中 ALOX5 始终表达升高,其水平与较差的肾功能和更为活跃的炎性免疫环境高度相关。
一条通路如何助长肾脏炎症
研究者接着探问该通路在肾脏中最活跃于何处,以及它如何促进损伤。单细胞测序数据使他们可以观察单个细胞而非整体组织。他们发现 ALOX5 及其助蛋白 ALOX5AP 在某些巨噬细胞中表达最强——这些是一线免疫细胞,可在平息或激发组织炎症之间转换。当这些细胞转向促炎状态时,助蛋白的表达上调,表明白三烯合成机制被激活。多重免疫组织化学(一种在组织切片上同时标记多种蛋白的技术)证实,ALOX5、其伴侣以及“愤怒”型巨噬细胞的标志物在受损小管周围聚集,同时白三烯受体出现在免疫细胞和邻近肾细胞上。该模式支持一个自我增强的循环:巨噬细胞产生白三烯,这些信号通过受体激活邻近细胞,而细胞内的核心控制系统(常称为 NF-kappa B)则进一步推动它们进入炎性状态。
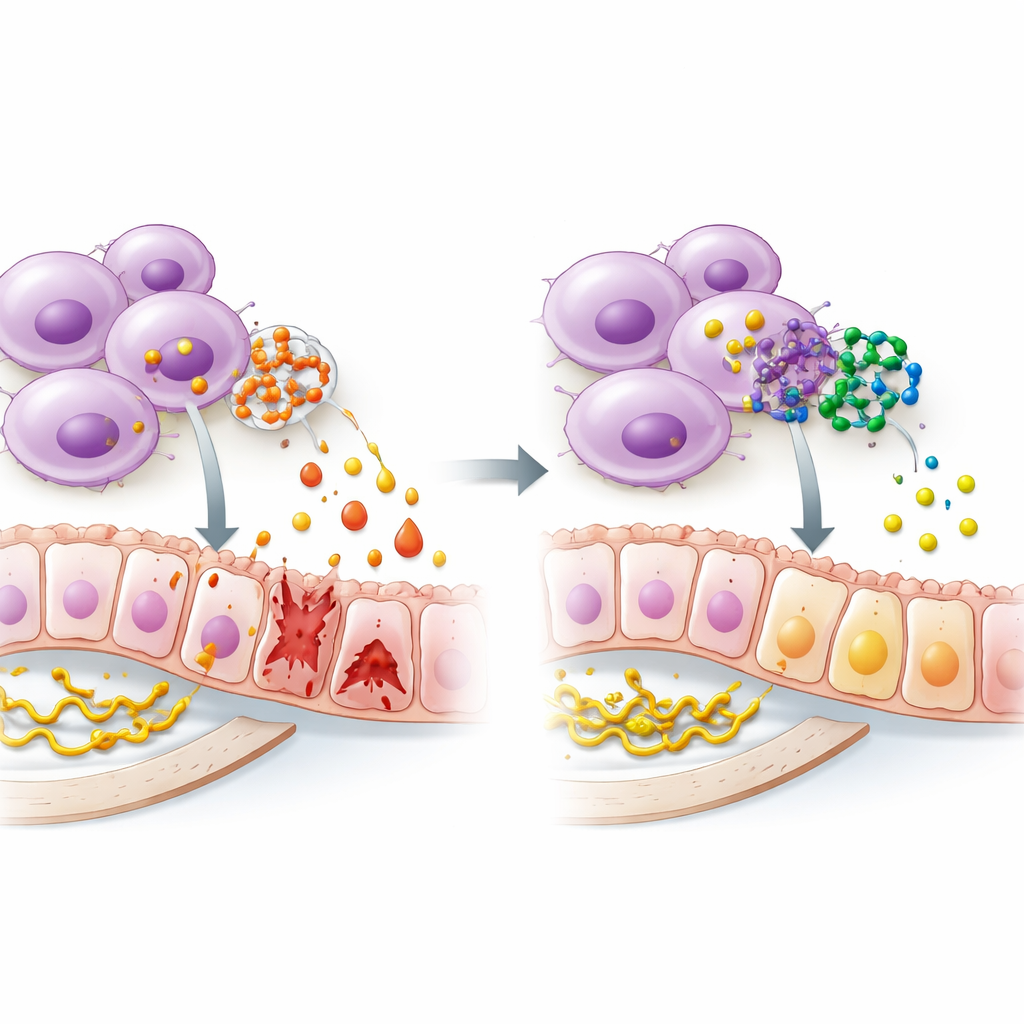
寻找能够平息火焰的药物
识别出一条通路只是第一步;下一个问题是是否可以安全地阻断它。研究团队使用药物指纹数据库筛选出可能影响 ALOX5 的小分子,然后用计算对接评估每个候选与酶三维结构的结合紧密度。四种化合物脱颖而出,其中包括已知的 ALOX5 抑制剂和厚朴酚(一种来源于厚朴树皮的天然物质)。随后的吸收性与类药性质分析显示,尤其是厚朴酚可能适合作为口服制剂,具有良好的摄取性、合理的化学稳定性,以及较低的因非特异性效应而干扰实验结果的可能性。尽管这些预测仍需在现实世界中验证,但它们指向了从分子发现到潜在治疗的可行路径。
这对未来治疗可能意味着什么
通俗地说,研究提出肾脏浸润免疫细胞中的一个特定酶系统像是炎症的音量旋钮。当 ALOX5 及其伴侣蛋白被调高时,巨噬细胞产生更多促炎信使,转入有害状态,推动瘢痕形成和肾功能丧失。通过调低该通路——可能使用诸如厚朴酚的化合物——有望恢复肾脏免疫环境的更健康平衡,从而减缓或预防损伤。尽管临床试验尚远,该研究提供了明确的生物学靶点和有前景的候选分子,使针对糖尿病肾病的精准抗炎治疗更进一步。
引用: Lu, W., Deng, Y., Zhai, L. et al. Integrated machine learning and multi-omics analysis identifies ALOX5 as a potential therapeutic target for tubulointerstitial inflammation in diabetic kidney disease. Sci Rep 16, 14194 (2026). https://doi.org/10.1038/s41598-026-44445-0
关键词: 糖尿病肾病, 肾脏炎症, 巨噬细胞, ALOX5 通路, 厚朴酚