Clear Sky Science · zh
载喜树橙皮苷的脂质-壳聚糖纳米颗粒的开发:理化表征、分子对接与体外(离体)研究
为何一种柑橘化合物需要高科技“升级”
许多食物中的有益成分,例如柑橘类化合物喜树橙皮苷(hesperidin),在理论上看起来很有潜力,但在体内往往表现不佳。喜树橙皮苷与心血管、免疫和抗癌益处有关联,然而它在水中溶解性差,难以穿过肠壁,因此很大一部分被浪费。本研究探讨了一种将喜树橙皮苷“重新包装”为由脂质和天然高分子构成的微小混合颗粒的方法,以期改善其溶解性、在肠道中停留时间并更有效地发挥抗氧化和抗炎作用。
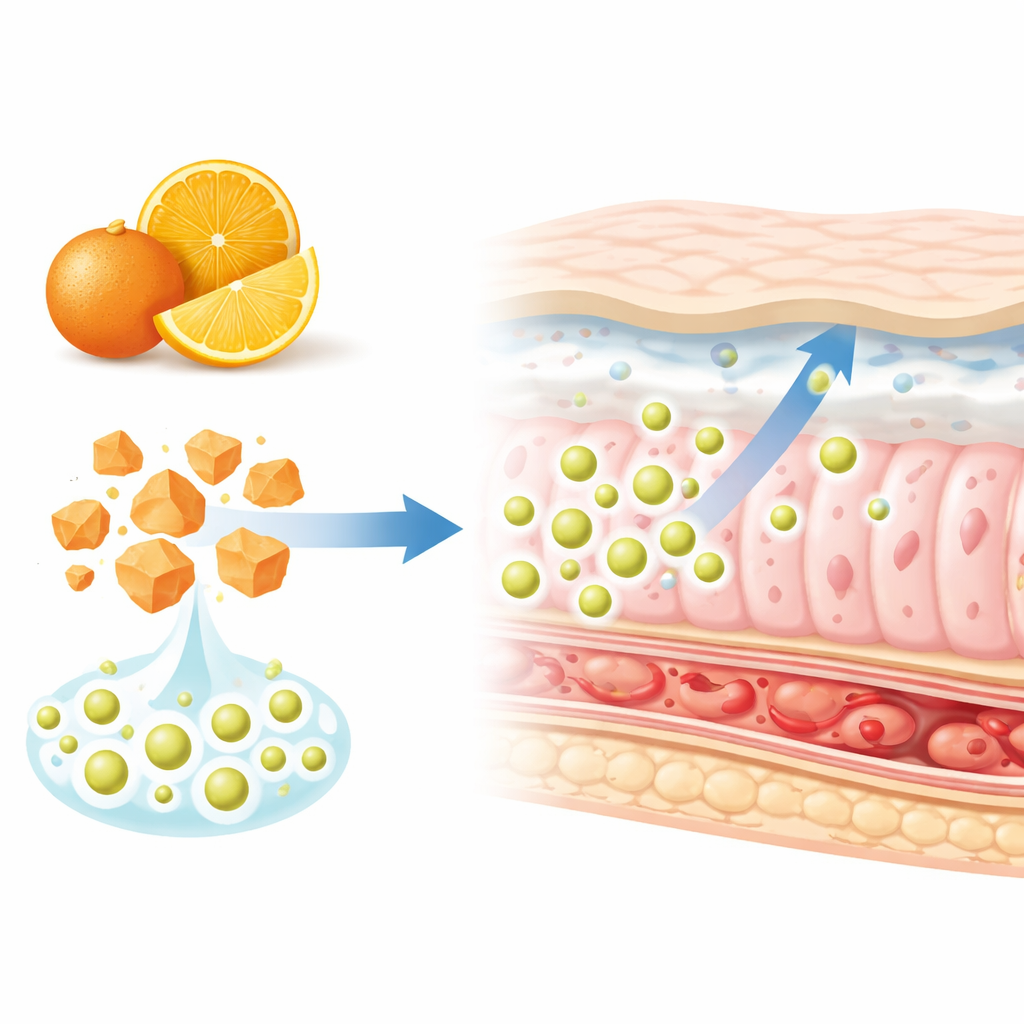
从橘子到微型递送载体
喜树橙皮苷是一种主要存在于橙子、柠檬等柑橘类水果中的植物类黄酮。体外与动物研究将其与抗病毒、抗癌、降压、抗氧化和抗炎等作用联系起来。然而,当以常规补充剂形式口服时,只有一小部分被吸收。它在水中溶解性差,会被肠道酶分解并被肠细胞泵出。为克服这些障碍,研究者设计了由固体脂(单硬脂酸甘油酯)与壳聚糖混合构成的“混合”纳米颗粒,并加入稳定颗粒的助剂。目标是将喜树橙皮苷包封在这种纳米级载体内,以改善其溶解性并优化其在消化道中的转运。
构建与检测纳米载体
团队通过加热、磁力搅拌和高能声波将熔融脂质、壳聚糖和喜树橙皮苷分散到水相中,形成均匀的纳米颗粒,随后冷冻干燥成稳定粉末。他们制备了不同脂质与壳聚糖配比的若干配方,并测定了颗粒粒径、表面电荷以及实际包封率等性质。表现最优的配方颗粒直径约为200纳米——比人类头发宽度小数千倍——呈正电荷并具有高的喜树橙皮苷负载量。进一步的表征显示,在这些颗粒内部,喜树橙皮苷从有序的晶体形态转变为更无序的非晶态;这种转变已知可促使溶解性差的化合物更快溶出。
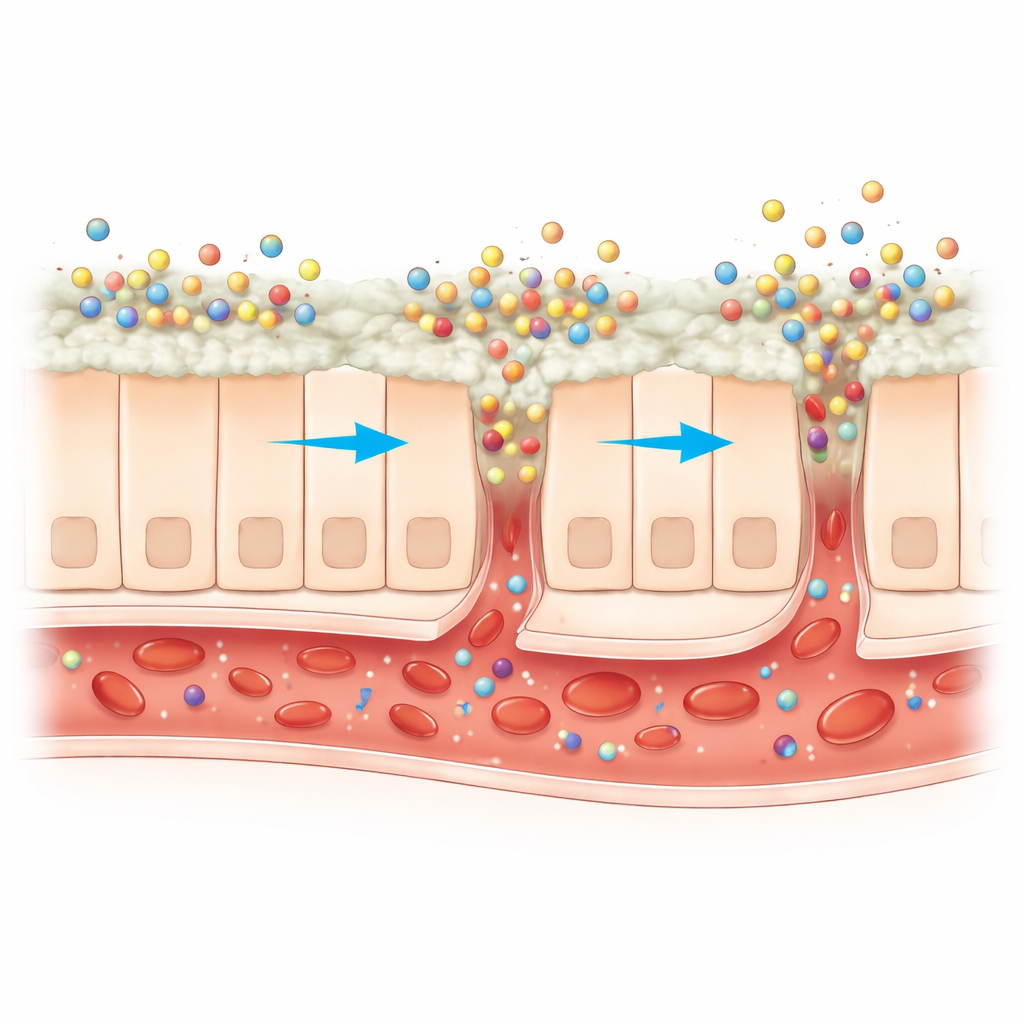
帮助药物穿过肠壁
接下来,科学家们考察了这些纳米颗粒在模拟人体肠道条件下是否能改善喜树橙皮苷的行为。在体外释放实验中,纳米制剂在24小时内稳定释放出超过70%的喜树橙皮苷——约为游离化合物的三倍半左右。在以山羊肠道作为人体肠道替代的离体穿透实验中,纳米颗粒穿过组织输送的喜树橙皮苷量约为游离喜树橙皮苷的3.5倍。壳聚糖包膜带正电,可与肠道表面的带负电黏液良好结合,并似乎温和地松弛细胞之间的紧密连接,使更多微小颗粒得以穿过。更好的溶出、对肠道的更强粘附以及更易的细胞间通行三者结合在一起,表明在生物体内,口服剂量中更大比例可能进入血液循环。
增强抗氧化与抗炎活性
由于喜树橙皮苷以其清除有害自由基与抑制炎症的能力而为人重视,研究者还将纳米制剂的生物活性与游离化合物进行了比较。在标准化学抗氧化能力测定中,纳米颗粒在多个剂量下表现出较游离喜树橙皮苷更强且与浓度相关的自由基清除作用。在作为炎症简化模型的蛋白质抑制测定中,纳米形式在较高浓度下同样表现更佳,接近一种常用抗炎药的效应。为探讨喜树橙皮苷及其载体材料在分子层面上如何与生物靶点相互作用,团队进行了计算机对接模拟。结果表明,喜树橙皮苷与载体分子均可与关键的抗氧化和炎症相关酶形成有利的相互作用,这与实验室观察结果相符。
这对未来补充剂意味着什么
简单来说,该研究表明经精心设计的脂质–壳聚糖纳米颗粒可以帮助一种难溶的植物化合物更容易溶解、在肠道黏膜上更好地停留并更有效地穿过肠壁,同时保持甚至增强其抗氧化和抗炎活性。如果在动物与人体研究中能证实类似益处,这一策略可能使喜树橙皮苷成为更可靠的口服补充剂或药物,进而有望用更低剂量获得更强的效果。更广泛地看,这一方法为升级其他在实验室中看起来有前景但在人体内达不到预期效果的植物来源化合物提供了通用思路。
引用: Gilani, S.J., Altwaijry, N., Sultan, A.M. et al. Development of hesperidin loaded lipid-chitosan nanoparticles: physicochemical characterization, molecular docking and ex vivo study. Sci Rep 16, 13530 (2026). https://doi.org/10.1038/s41598-026-43743-x
关键词: 喜树橙皮苷, 纳米颗粒, 药物传递, 抗氧化剂, 壳聚糖