Clear Sky Science · zh
维生素C在体外缺血再灌注条件下保护少突胶质细胞谱系并调节小胶质细胞炎症反应
一种常见维生素如何可能保护大脑连线
提到维生素C,我们常想到它对抗感冒的作用。但在大脑内部,这种熟悉的营养素或许在做更微妙也更重要的事情:帮助保护包裹神经纤维并维持信号快速平稳传导的细胞。该研究在一种模拟血流和氧气减少的体外模型中探讨了维生素C的作用,这种条件类似于中风或慢性血液灌注不良时的情况,并检验这种维生素是否能保护易受损的大脑细胞。
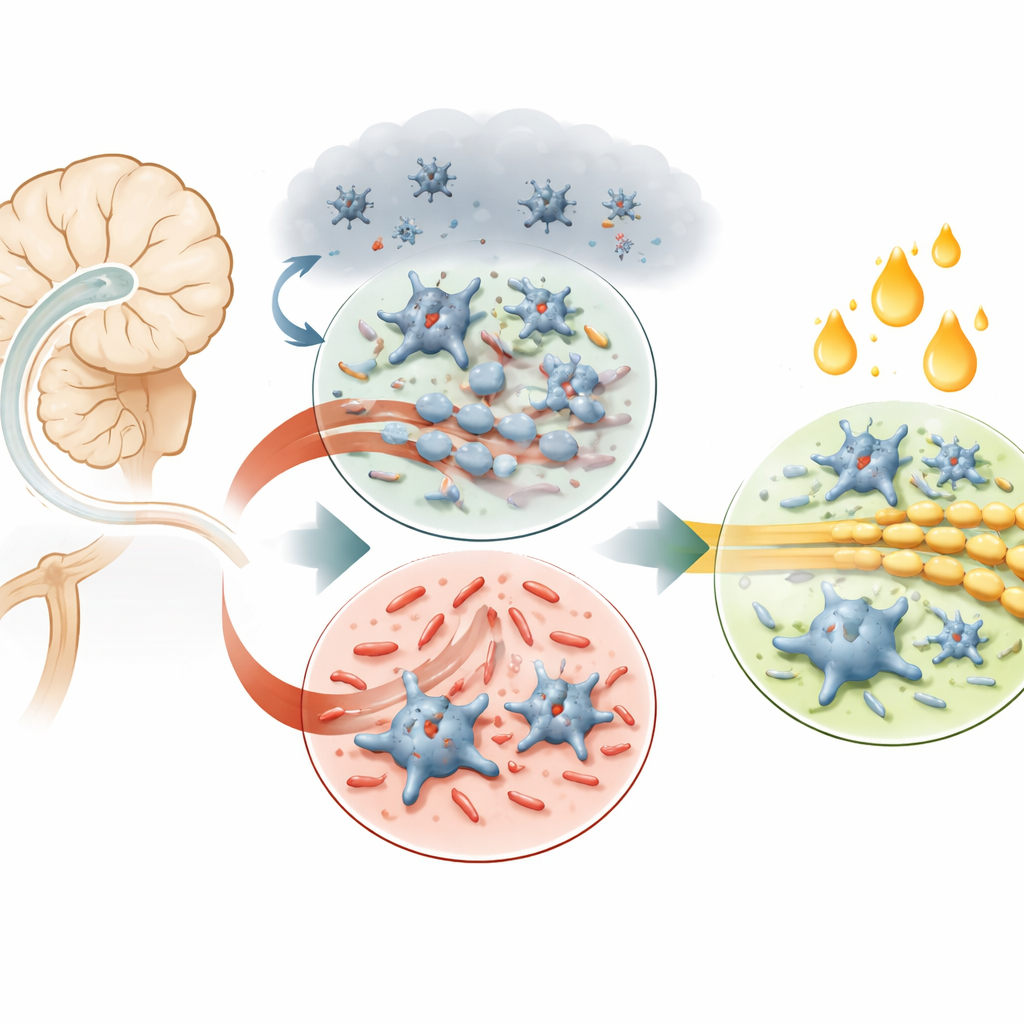
大脑的隐形支援团队
我们的思维、运动和记忆能力不仅依赖于神经元,还依赖于一张由支持细胞组成的网络。其中最重要的细胞之一是少突胶质细胞,它们将神经纤维包裹在一种称为髓鞘的脂质外套中,使电信号能迅速传播。其幼稚形态称为前体细胞,这些细胞必须生长并成熟后才能形成髓鞘。另一个关键角色是小胶质细胞——大脑固有的免疫细胞,它们既能参与修复,也能驱动炎症。由于少突胶质细胞的能量需求极高,当血流受阻导致氧气和养分不足时,它们尤为脆弱。
在实验室重现小型中风
为了在可控条件下研究这些相互作用,研究者使用了在培养皿中生长的大鼠脑细胞。他们将少突胶质前体细胞、成熟少突胶质细胞和小胶质细胞暴露于无氧与无糖的阶段,随后恢复至正常条件。这一程序模拟了中风或短暂灌注不良中突然的缺血和随后恢复。团队测量了细胞死亡数量、前体细胞的成熟情况以及小胶质细胞释放有害炎性分子的程度。随后他们在相同实验中加入了适度剂量的维生素C,其浓度与人类在常规补充后脑脊液中可达到的水平相近。
维生素C平息损伤与炎症
在没有维生素C的条件下,模拟的血流丧失引发了一波损伤。更多的少突胶质前体细胞和成熟细胞进入程序性细胞死亡,成功成熟为形成髓鞘细胞的前体显著减少。细胞内的氧化应激化学标志显著上升,表明活性分子正在攻击脂质及其他成分。小胶质细胞则转向炎症模式,释放出可能进一步伤害邻近细胞的因子。当存在维生素C时,这一景象发生了变化:少突胶质谱系细胞的死亡约减少了一半,它们的成熟有所恢复,损害性活性分子和脂质分解产物的积累明显降低。
支持细胞与免疫细胞之间的对话
因为大脑细胞并非孤立运作,研究者还将少突胶质细胞与小胶质细胞共同培养在一个双层系统中,使它们能交换可溶性信号但不直接接触。在模拟血流丧失时,小胶质细胞被激活,导致更多前体细胞死亡和成熟受损。再次加入维生素C显示出益处:它抑制了小胶质细胞产生侵袭性炎性因子,同时提升了与更平和、修复导向状态相关的标志。有趣的是,在这些混合培养中,成熟少突胶质细胞比单独培养时不那么易受损,提示在某些条件下,邻近的小胶质细胞既可能带来风险也可能提供保护。
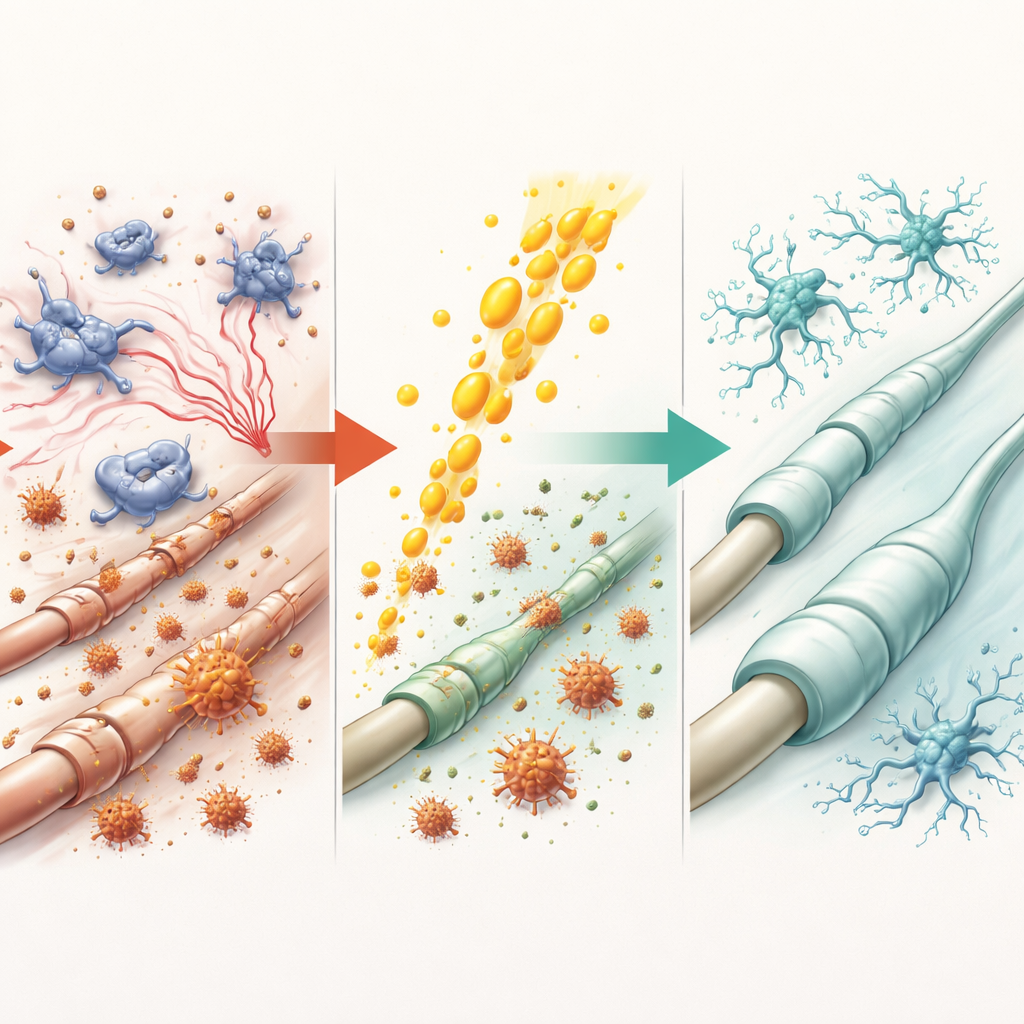
这些发现对大脑健康可能意味着什么
从宏观角度看,这项工作表明在该体外模型中,维生素C可以同时在两个方面发挥作用:它直接保护形成髓鞘的细胞免受氧化损伤,并将大脑免疫细胞从破坏性反应引导向更平和、更支持修复的状态。尽管这些实验是在培养皿中完成,而非活体动物或人体,但它们有助于解释为何在威胁大脑白质的情况下(如中风、慢性灌注不足或某些神经退行性疾病)充足的维生素C可能尤其重要。结果尚不足以支持改变临床实践,但它们将这类安全且广泛可得的营养素作为未来旨在保护大脑连线的治疗策略中的一个有前景的候选者。
引用: Guo, J., Cheng, Y. & Yi, M. Vitamin C protects oligodendrocyte lineage cells and modulates microglial inflammation during OGD/R in vitro. Sci Rep 16, 11048 (2026). https://doi.org/10.1038/s41598-026-41308-6
关键词: 维生素C, 白质, 少突胶质细胞, 小胶质细胞, 氧化应激