Clear Sky Science · zh
具有抗炎活性的鞣花酸苷通过影响Brd4介导的染色质重塑来减轻炎性骨溶解
为什么一种水果化合物可能对关节疼痛重要
许多人因关节炎或其他炎性骨病而长期忍受关节疼痛,这类疾病中机体会缓慢侵蚀自身骨组织。现有药物常能缓解疼痛,但伴随副作用且对长期病损阻止有限。该研究探讨了鞣花酸苷(一种存在于石榴中的天然分子)是否能平息有害炎症、保护骨骼不被侵蚀,并温和地调整免疫细胞内基因的开启和关闭机制。
当防御细胞过度反应时的骨丧失
炎性骨溶解是在骨关节炎、类风湿性关节炎、骨感染以及牙种植体或关节置换周围炎症等情况下出现的一种骨质流失。在这些情形中,被称为巨噬细胞的免疫细胞持续激活并释放大量炎性信号分子。这些信号诱导前体细胞分化为破骨细胞——专门溶解骨组织的细胞。当破骨细胞的活性超过成骨细胞时,就会导致骨变薄、脆弱以及关节或植入物周围的结构性损伤与疼痛。
为何基因控制与“细胞生锈”很重要
当巨噬细胞向吞噬骨质的破骨细胞转变时,其能量代谢上调并产生大量活性氧(reactive oxygen species),可视为细胞内的化学“生锈”。这些活性分子不仅会损伤DNA,还会改变DNA的包装方式——即表观遗传层面的调控。一个关键的表观遗传参与者是名为Brd4的蛋白,它能识别染色质蛋白上的化学修饰并促进许多炎症基因的开启。由于这些表观遗传改变是可逆的,研究者对可将这一基因控制系统引导回更健康、低炎性状态的药物很感兴趣。
一种温和的石榴分子
鞣花酸苷是一种植物来源的多酚,已知具有抗氧化和抗炎特性。研究者首先在体外培养的骨与免疫细胞中评估其安全性。结果显示,巨噬细胞与成骨前体细胞在相对较高剂量下仍能耐受且存活率无显著下降,而约80微摩尔或以下的浓度即使长期暴露也特别安全。在这一安全区间内,鞣花酸苷强烈抑制了破骨细胞的形成与融合,破坏了它们啃噬骨质所需的肌动蛋白环结构,并显著降低了参与破骨细胞分化与骨吸收的基因活性。
从内部改写炎症反应
为了解鞣花酸苷的作用机制,团队分析了炎性巨噬细胞的全基因表达。当细胞用细菌成分刺激以模拟感染时,成千上万与炎症、细胞分裂、染色质组织和DNA损伤通路相关的基因发生了变化。加入鞣花酸苷能将许多这些变化逆转:促炎基因下调,而支持抗氧化防御与细胞保护的基因上调。分析强烈指向会重塑细胞核内DNA三维结构的过程,尤其与组蛋白乙酰化和染色质重塑相关。研究显示鞣花酸苷降低了包括Brd4在内的BET蛋白家族的表达,且计算对接提示鞣花酸苷可直接与这些蛋白结合。同时,鞣花酸苷增强了细胞自身的抗氧化系统,并在免疫细胞与骨前体细胞中明显降低了全局与线粒体来源的活性氧水平。
在活体动物中保护骨骼
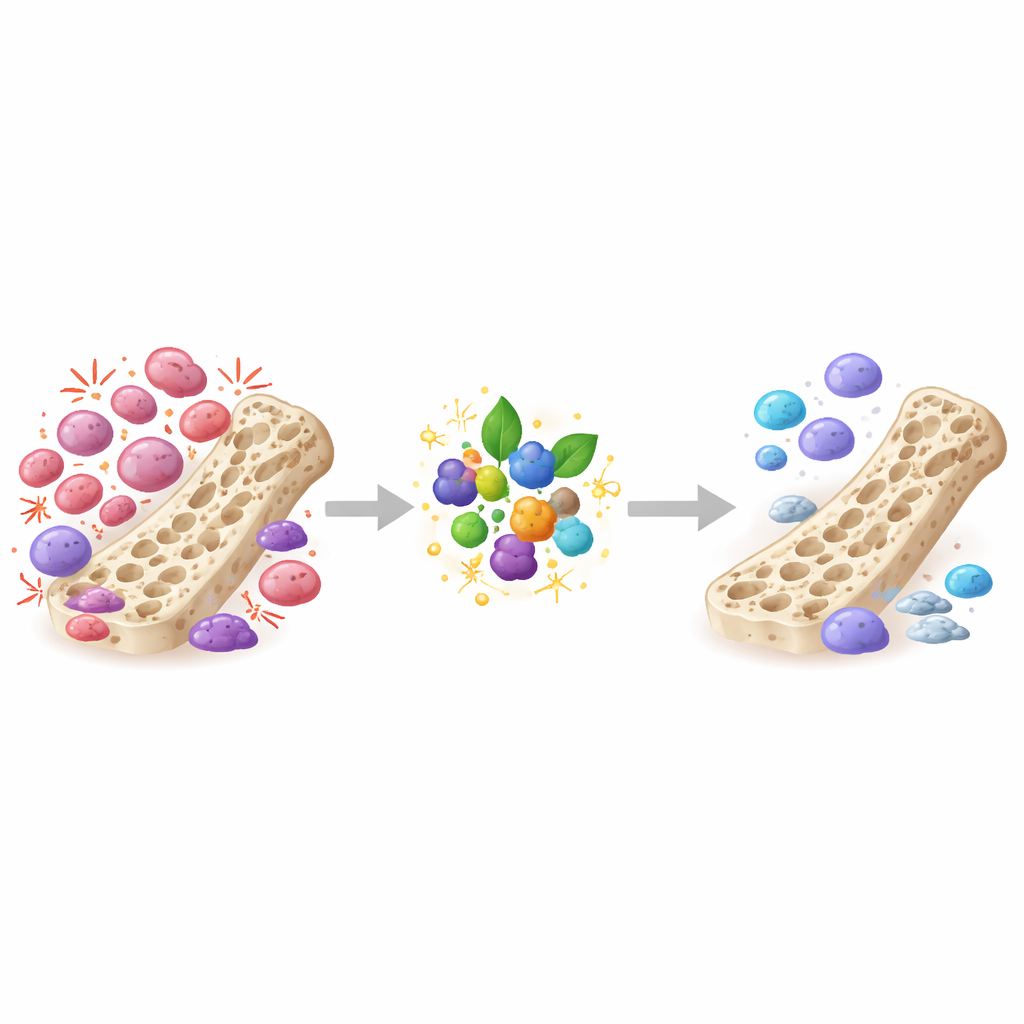
随后研究者使用一种小鼠模型:细菌毒素诱发颅骨的快速骨丧失。仅接受毒素刺激的动物出现广泛的骨坑与侵蚀,并伴有大量炎性细胞浸润。与毒素同时给予鞣花酸苷的鼠类在高分辨率微CT扫描中显示出明显更平滑的骨面,骨体积与结构指标更好。组织染色证实破骨细胞减少且炎症迹象减轻。这些体内结果与细胞培养结果一致,表明鞣花酸苷通过抑制破骨细胞、支持抗氧化体系与表观遗传调控的组合,能够转化为对骨组织的实际结构性保护。
这对未来治疗意味着什么
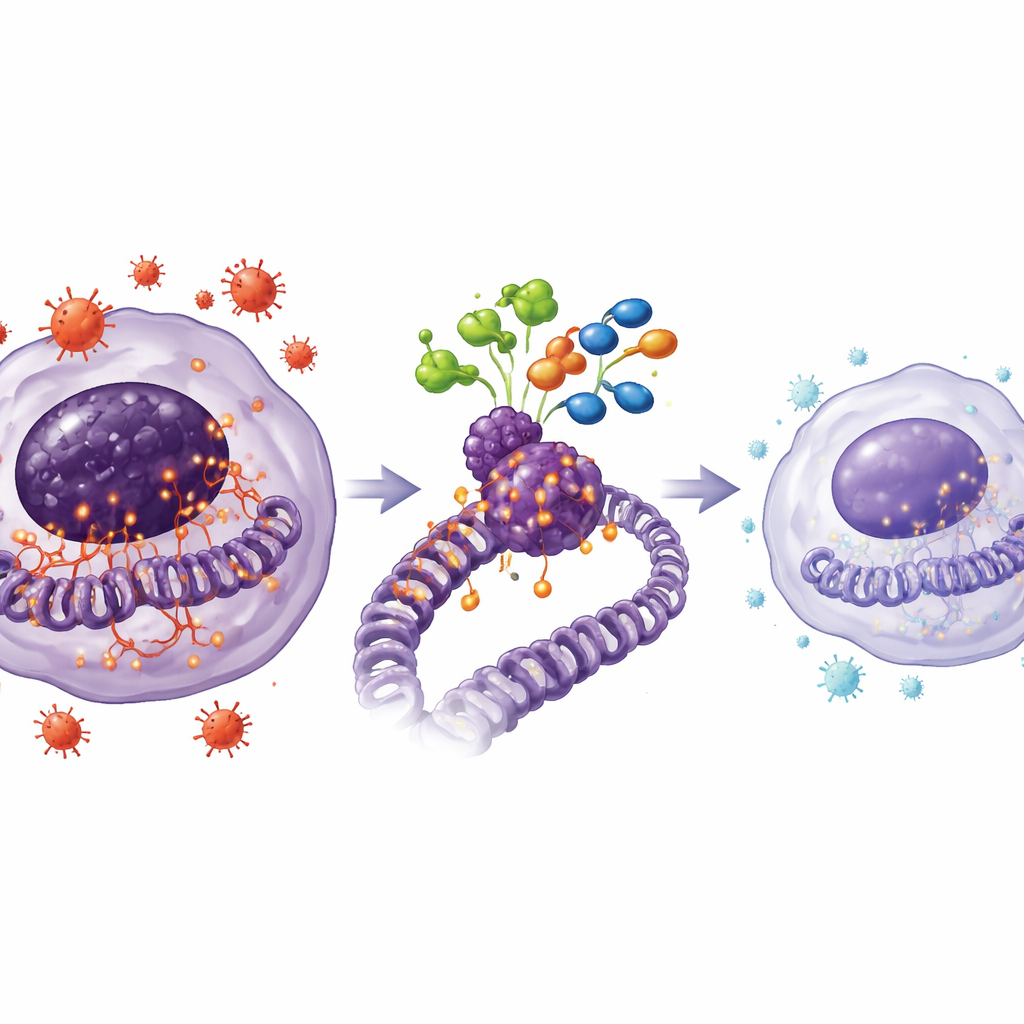
通俗地说,这项工作表明一种来自石榴的天然化合物能够帮助平息过度活跃的免疫细胞,减少有害的细胞“生锈”,并微妙地重置这些细胞内炎症基因的读取方式。通过这些作用,鞣花酸苷减缓了破骨细胞的形成与活性,并在小鼠中保护骨骼免受炎性破坏。尽管仍面临若干挑战——例如提高口服时的吸收性并在更大动物或人类中进行验证——该研究指出了未来治疗关节炎及相关骨病的方向:不仅缓解疼痛,还通过同时靶向炎症与驱动炎症的表观遗传开关来保护骨骼。
引用: Li, H., Li, Q., Wan, T. et al. Punicalagin with anti-inflammatory activities affects Brd-4 mediated chromatin remodeling for attenuating inflammatory osteolysis. Sci Rep 16, 12948 (2026). https://doi.org/10.1038/s41598-026-41262-3
关键词: 鞣花酸苷, 炎性骨溶解, 破骨细胞, 表观遗传调控, 骨骼炎症