Clear Sky Science · zh
可生物降解的低铈镁-镝合金通过调节巨噬细胞介导的免疫微环境促进老年骨质疏松性骨折的骨修复
来自“聪明”金属的更强骨骼
老年骨质疏松患者的骨折愈合通常缓慢且困难。该研究探索了一种由镁及一种名为镝的稀土元素制成的新型临时金属植入物。与传统的钢或钛械不同,这种金属在体内会缓慢溶解,并且似乎能抑制有害炎症,同时促进机体自身的成骨细胞更积极地工作,为老年骨折后的更好恢复提供了潜在新途径。
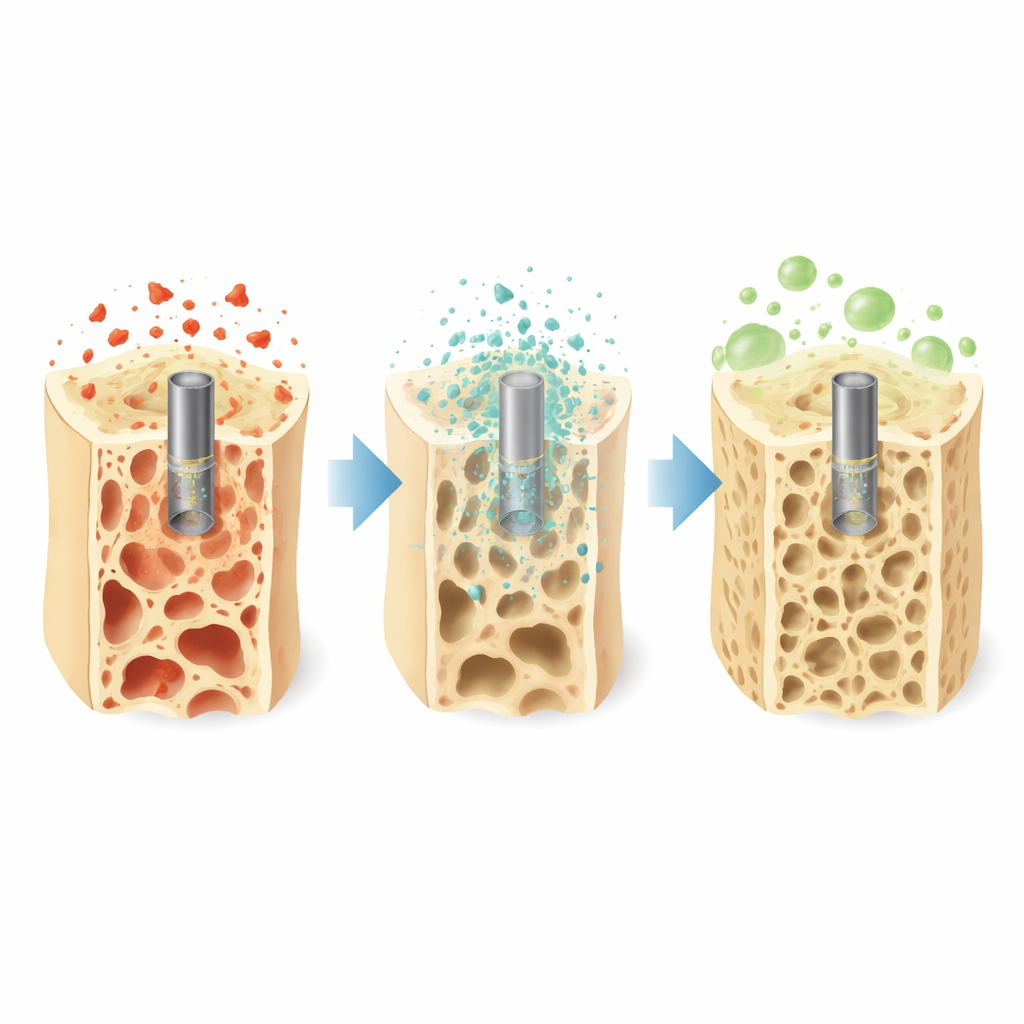
为什么脆弱的骨骼需要新型支撑
骨质疏松使骨骼变薄、多孔、易碎,尤其是65岁以上人群。标准的金属钢板和螺钉虽然非常坚固,但它们可能将周围骨骼与正常负荷隔离,实际上可能导致骨质进一步变弱,有时还需要第二次手术取出。同时,衰老的免疫系统往往处于持续的低度炎症状态。被称为巨噬细胞的免疫细胞常停留在一种有害的“激怒”状态,阻碍骨修复。作者认为,理想的老年患者植入物不仅应将骨折固定,还应能温和降解并主动引导免疫系统走向修复方向。
与机体协同工作的温和金属
研究人员设计了一种以镁为主、含有极少量(约1%)镝的简单合金,并通过低温挤压工艺调控其内部组织结构。该加工使植入物具有足够的强度,可匹配或超过天然骨的强度,并具有适度的刚度以提供支撑而不过于僵硬。当该合金浸泡在模拟体液的溶液中时,它以可控速率腐蚀,并在表面形成一层富含镝、氧化镁、钙和磷酸盐的致密薄膜——这些成分类似于骨的矿物质。这层保护膜减缓了进一步的分解,限制了气体产生,并形成了对周围组织有利的表面。
将有害炎症转化为有利修复
为观察材料对免疫系统的影响,团队将巨噬细胞置于与合金接触过的溶液中。在安全范围的镁离子浓度(约不超过8毫摩尔)下,细胞保持健康但行为发生了变化。促炎性“激怒”状态的标志下降,而有助愈合的“抚慰”状态的标志上升。这些“重编程”的巨噬细胞产生更少的炎性分子和活性氧,更多与组织修复相关的安抚因子。当它们的分泌物应用于来自骨髓的成骨干细胞时,这些干细胞激活了参与早期和晚期成骨的基因,并表现出与矿化沉积相关酶活性的升高。分子检测显示,一条称为NF‑κB的关键信号通路是将镁暴露、免疫细胞转变与增强成骨连接起来的途径之一。
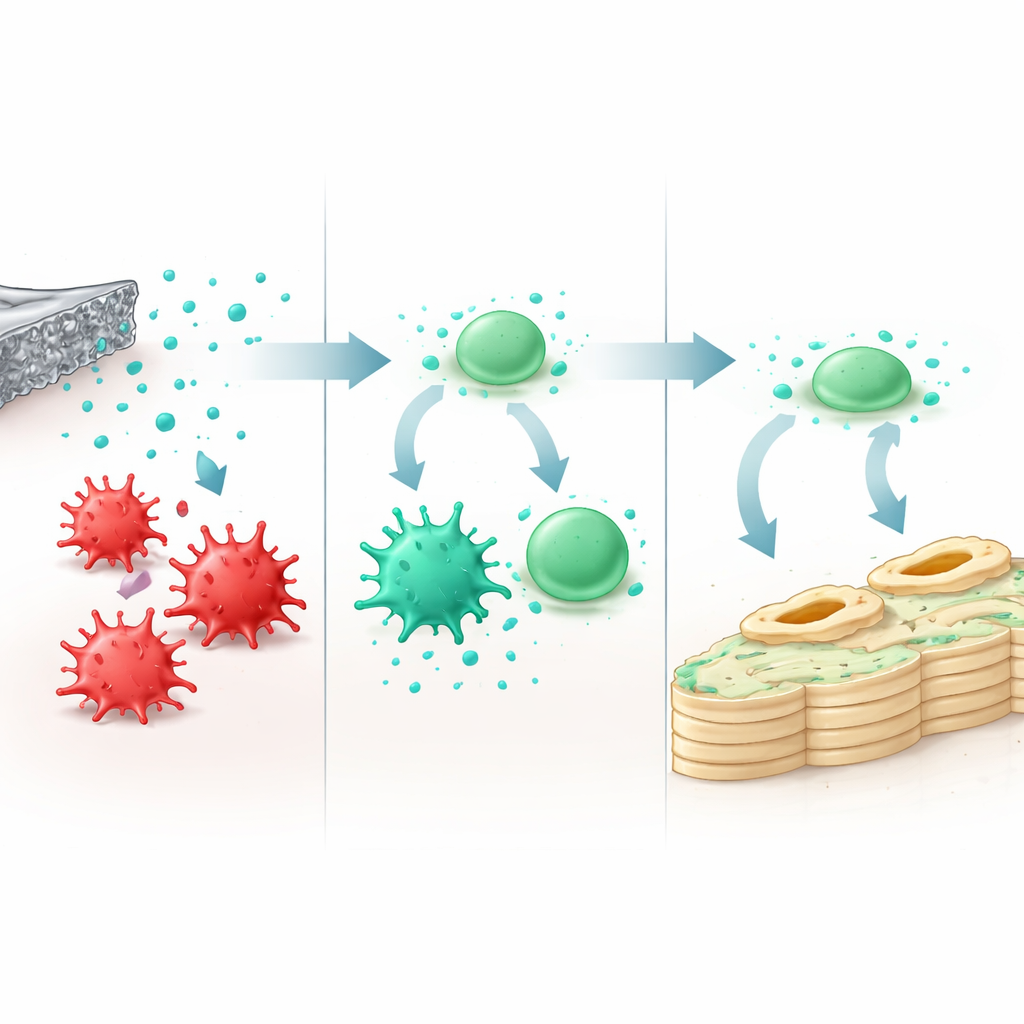
在活体动物中帮助老年骨愈合
研究者进一步在模拟衰老性骨质疏松的小鼠模型中测试了该合金。他们将小型Mg–Dy棒植入年老且骨质疏松的小鼠的骨缺损处,并在数周内通过高分辨率扫描和组织染色追踪愈合情况。与对照组相比,使用低温处理合金的骨折位点周围呈现更高的骨体积和矿物密度。显微镜下显示更多的骨痂(临时修复组织)、更好的向成熟骨的转变以及新生骨与正在降解金属之间更紧密的整合。重要的是,该合金以稳定速度降解,而不是过快瓦解,在新骨生长的同时维持机械支撑。
引导愈合的临时支架
综合来看,该研究表明这种可降解的镁–镝合金可作为脆弱骨骼的智能、可消失支架。它有足够的强度稳定骨折,缓慢溶解为机体可处理的离子,并且关键在于能将免疫细胞从慢性炎症状态引导至促进修复的状态,从而增强成骨干细胞的功能。对于骨质疏松的老年患者,这类植入物未来有望减少取出手术的需要,并提高骨折恢复强度的可能性,通过与骨骼和免疫系统协同工作而非对抗它们。
引用: Zhou, S., Chen, X., Cai, Z. et al. Biodegradable lean Mg-Dy alloy enhances bone repair in senile osteoporotic fractures by modulating macrophage mediated immune microenvironment. npj Mater Degrad 10, 43 (2026). https://doi.org/10.1038/s41529-026-00757-0
关键词: 骨质疏松, 可降解植入物, 镁合金, 骨愈合, 免疫调节