Clear Sky Science · zh
免疫胆道单细胞图谱解析2型常规树突状细胞与γδ T细胞在胆管炎中的相互作用
为什么胆管炎很重要
当肝脏引流胆汁的细小管道发生炎症或阻塞时,后果可能是持久的:持续损伤、瘢痕形成,最终导致肝功能衰竭。像原发性硬化性胆管炎这样的疾病常沿此路径发展,但将短期损伤转变为慢性纤维化的早期免疫事件仍不清楚。本研究通过逐细胞绘制胆管周围专门免疫细胞的通信方式,揭示了一个关键的相互作用回路,推动肝脏瘢痕形成。
肝脏胆管周围的繁忙“邻里”
研究者关注所谓的“免疫胆道环境”——胆管细胞、血管与驻留免疫细胞相遇的区域。利用人类肝组织样本和空间转录组学,他们显示树突状细胞、T细胞与胆管上皮细胞在较大胆管周围紧密聚集。健康小鼠肝脏也呈现类似结构。在模拟梗阻性胆管损伤的小鼠模型中,随着胆管对损伤的反应并吸引大量免疫细胞,该微环境显著扩展。胆管细胞激活了炎性信号与募集细胞的基因,提示它们并非被动承受损伤,而是主动召集并塑造周围免疫群体。
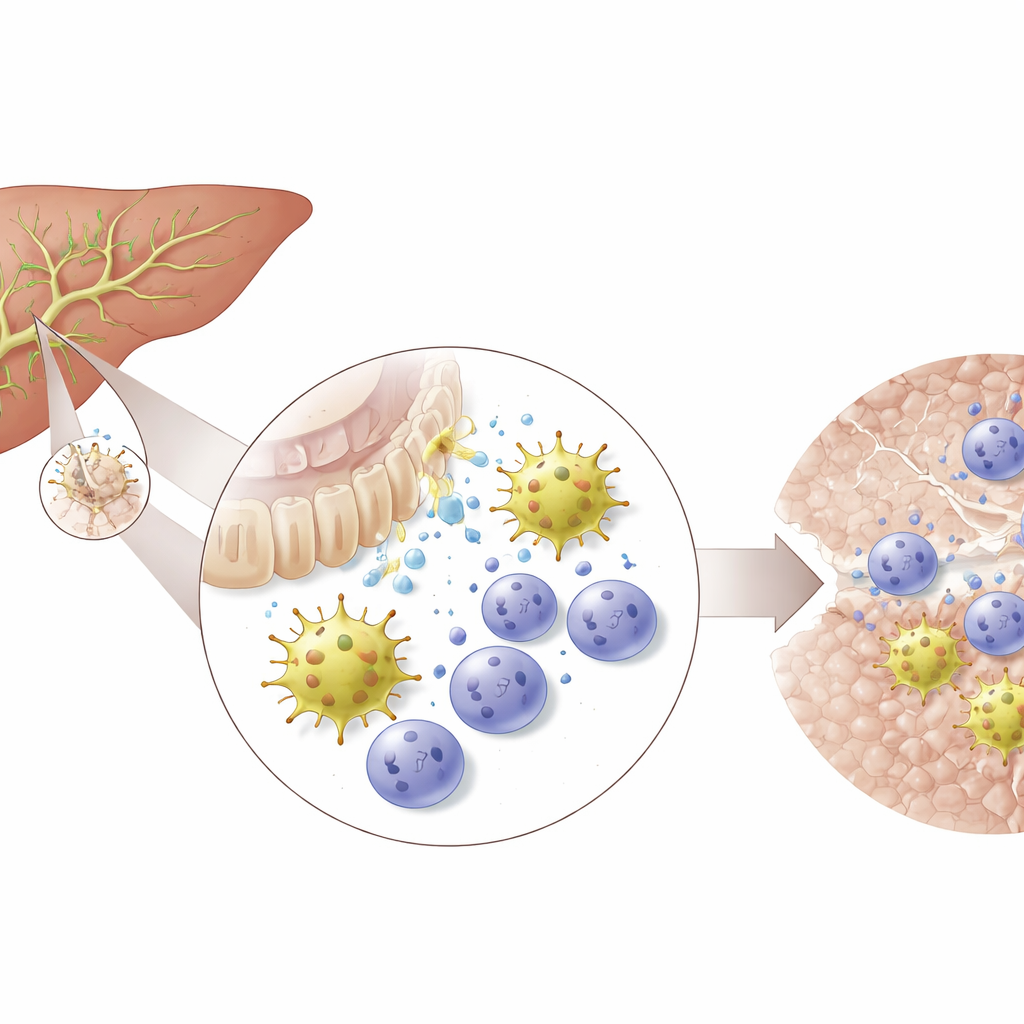
一种树突状细胞类型成为主角
在众多免疫细胞中,一类群体尤为突出:2型常规树突状细胞,尤其是名为cDC2B的亚群。跨多时间点的单细胞RNA测序显示,这些细胞在胆管损伤开始后不久数量增加,超过了其他树突状细胞类型。研究团队重构了从未成熟前体到成熟、组织适应性cDC2B的发育路径,这些成熟细胞由特定基因标记并具有促成某类免疫反应的信号特征。随着疾病进展,驻留的成熟cDC2B细胞出现耗竭,逐渐被新到来的前体所替代,这些前体仍可根据环境线索被引导向炎性或更具修复性的状态发展。
助长瘢痕形成的专门化T细胞
研究随后聚焦于一群相对少见的“非典型”T细胞——γδ T细胞。这些细胞被发现是IL‑17的主要产生者,而IL‑17已与肝脏炎症和纤维化相关。作者鉴定出不同的γδ T细胞亚群,包括驻留型和更具迁徙性的细胞,后者在淋巴结与血液中循环。两类细胞都能成为产生IL‑17的“γδ T17”细胞,但在基因调控程序与潜在的组织间迁移方式上有所不同。小鼠肝脏和人类原发性硬化性胆管炎组织的空间映射显示,γδ T细胞与cDC2B细胞在受损胆管周围近距离共存,使它们处于理想位置进行相互作用。
加重肝损伤的直接对话
通过结合计算配体–受体分析、体外共培养实验和小鼠中的选择性细胞去除,作者发现了cDC2B细胞与γδ T细胞之间的直接通信枢纽。被胆管损伤激活的树突状细胞通过可溶性因子和依赖接触的信号,促使γδ T细胞转向产生IL‑17的状态。其中一个关键接触信号涉及一对表面分子(树突状细胞上的Icosl与γδ T细胞上的Icos)。当研究者选择性去除cDC2B细胞时,肝脏及其引流淋巴结中的γδ T17细胞显著下降,早期纤维化标志物也减少。相反,去除γδ T细胞或基因上破坏IL‑17信号则降低了肝脏瘢痕形成和梗阻性肝病的生化指标,强调了该轴在促纤维化过程中的作用。
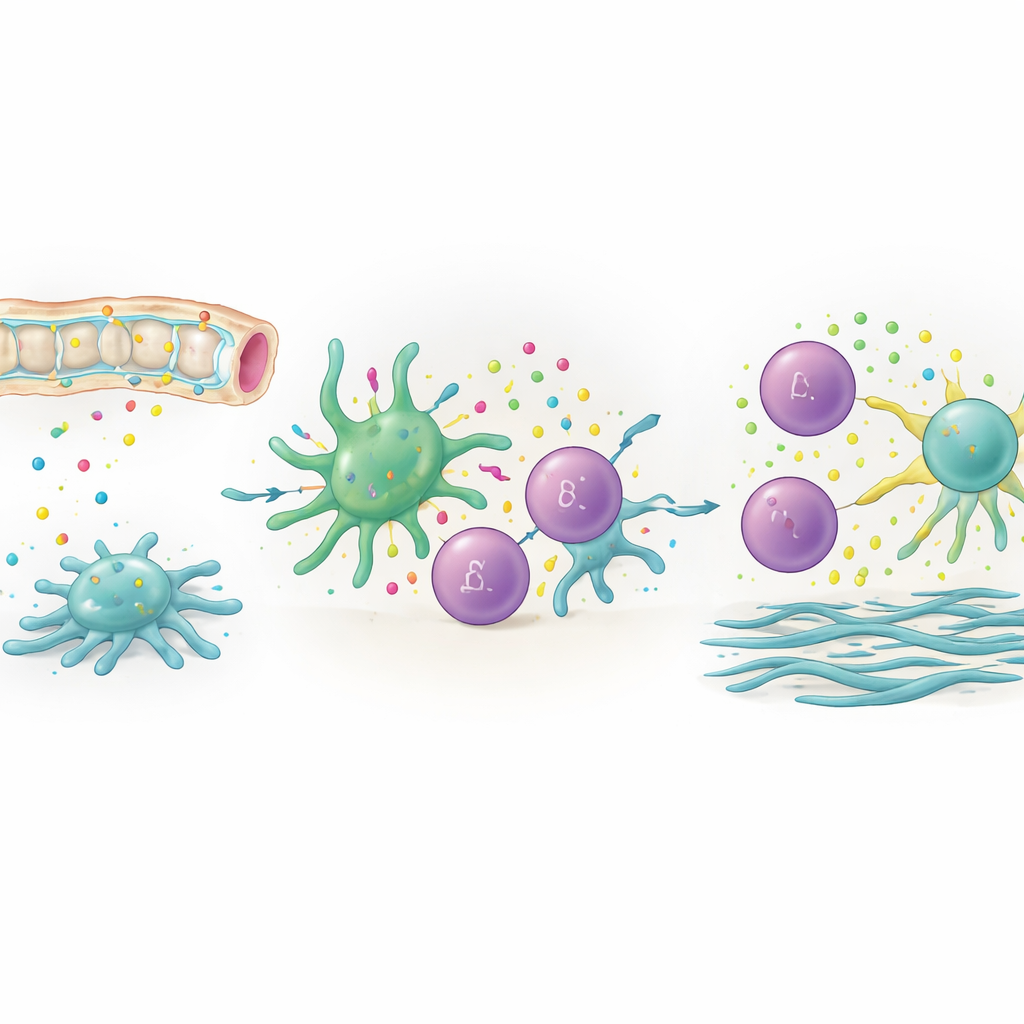
从局部对话到全器官影响
该研究还显示,这种相互作用并不限于肝脏本身。通过对肝脏引流淋巴结进行单细胞蛋白与RNA分析,团队发现成熟的cDC2B细胞会从肝脏迁移到这些淋巴结,在那里它们再次与γδ T细胞接触并促成偏向IL‑17的反应。在表观遗传层面,未成熟的树突状细胞前体在关键信号基因处缺乏开放染色质,意味着在完全成熟之前它们不太可能支持这种相互作用。在多种胆管损伤模型中,这一树突状细胞—γδ T细胞回路的变化反复出现,提示急性胆管损伤转化为慢性炎症与纤维化的共同通路。
这对胆管病患者意味着什么
对非专业读者而言,核心信息是:并非所有胆管周围的免疫细胞都相同。特定的树突状细胞亚群在被受损胆管细胞激活后,会使邻近的γδ T细胞产生IL‑17,两者共同推动肝脏瘢痕的累积。阻断这种对话——通过针对cDC2B细胞、它们用以激活γδ T细胞的信号,或它们诱导的IL‑17——可能为减缓或预防胆汁淤积性肝病(如原发性硬化性胆管炎)中的纤维化提供新策略。这份单细胞图谱为在这一关键免疫胆道回路中何处及如何干预提供了详细地图。
引用: Thomann, S., Hemmer, H., Agrawal, A. et al. An immunobiliary single-cell atlas resolves crosstalk between type 2 conventional dendritic cells and γδ T cells in cholangitis. Nat Commun 17, 3455 (2026). https://doi.org/10.1038/s41467-026-71537-2
关键词: 胆管炎, 胆管, 树突状细胞, γδ T细胞, 肝纤维化