Clear Sky Science · zh
联合物理和药理合成代谢性抗骨质疏松治疗可增强雌性小鼠的骨骼反应与机械调控
为什么强健的骨骼仍然重要
随着年龄增长,尤其是绝经后的女性,骨骼可能在不知不觉中变得脆弱、易于骨折。许多患者被开具强效抗骨质疏松药物,但他们常常会想:运动是否仍然有效,或者会不会干扰药物作用?这项在雌性小鼠上的研究通过测试不同抗骨质疏松药物与承重活动的相互作用,解答了这一日常疑问,揭示了何时运动与药物能够真正协同工作。
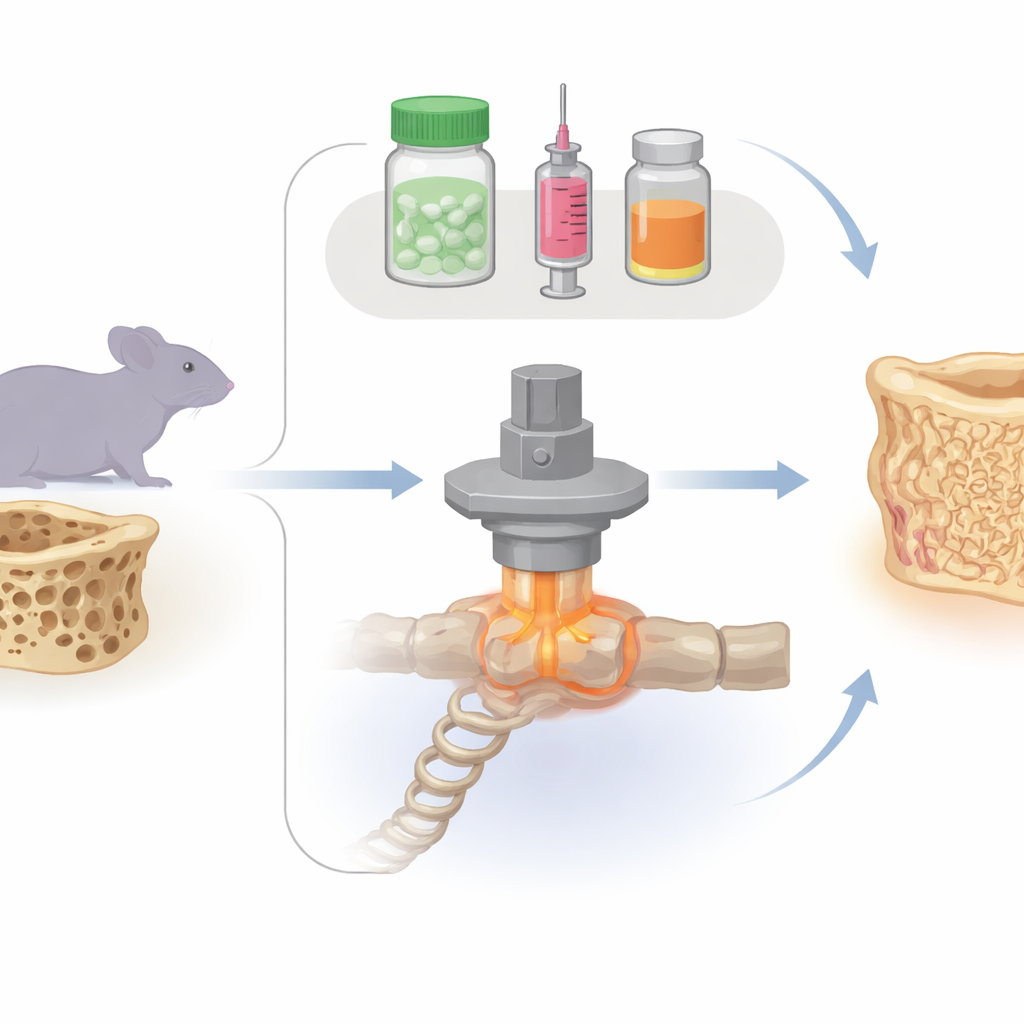
骨骼如何感知日常力学作用
骨骼并非静态支架;它是活组织,会持续感知并响应我们施加的力。当骨组织承受较高机械应变时,局部细胞倾向于形成更多组织;当应变较低时,则倾向于吸收骨组织。这个自我调节系统,有时被比作恒温器,旨在使骨强度与日常需求相匹配。在骨质疏松中,这一平衡被打破,破坏超过重建,内层海绵状结构被掏空,骨折风险上升。作者旨在考察三种广泛使用的治疗方法——一种抗吸收药(双膦酸盐)和两种促骨形成(合成代谢)方法(甲状旁腺激素和一种阻断抑制骨形成蛋白硬化素的抗体)——如何改变这种力学感知行为,尤其是在与模拟承重锻炼的受控机械负荷结合时的情况。
一种用于模拟脆弱脊椎骨的鼠模型
研究团队使用去卵巢的雌性小鼠来模拟绝经后骨质流失。他们集中研究一节小的尾椎,数周内反复用高分辨率微型CT扫描,三维观察骨组织的形成与消失。有些小鼠只接受对照注射;另一些接受双膦酸盐、甲状旁腺激素或阻断硬化素的抗体。另有一组在每种药物基础上加上通过尾部针脚施加的精确校准的周期性负荷,代表一种受控的机械锻炼形式。扫描数据与计算机模型配对,用以估算每个微小椎骨的强度以及机械能量如何在其内部细梁间分布。
药物与运动:谁在帮助谁?
各药物单独使用时表现符合预期。双膦酸盐主要通过强烈抑制骨吸收来保存现有的细薄骨梁,维持内部网络的连通性,但增加的新物质有限。促骨形成治疗则主要通过形成新组织来增加总体骨量,要么使现有骨梁变厚、要么添加新骨梁,或两者兼有。当加入机械负荷时,结果出现分化:将负荷与甲状旁腺激素或阻断硬化素的抗体联用,所预测的骨强度增益超过单独任何一种治疗;在硬化素抗体组中,联合效应大于各自效应之和,表现出真正的协同作用。相反,在双膦酸盐基础上叠加负荷几乎没有额外益处,在某些指标上,两者的影响还部分相互抵消。
新骨在哪里以及如何被增加
通过追踪相对于局部机械应变的骨增减位置,研究者显示,不论治疗方式如何,骨形成始终倾向发生在受力较大的区域,而吸收则偏向受力较小的区域。换言之,骨变化“定向”到正确部位的机制在很大程度上保持完整。关键差异在于这些趋势表现的强度。合并负荷的促骨形成治疗显著提高了在未先被吸收的情况下直接形成骨组织的数量(称为建模),尤其是在曾经承受较高应变的区域。这种高效的“填补薄弱处”策略降低了局部极端载荷并提高了预测强度。将机械刺激与净骨变化联系起来的数学曲线显示,所有药物都将触发骨形成的阈值向较低应变移动,但只有促骨形成疗法在有负荷存在时具备足够的构建能力,将这一阈值变化转化为显著的强度提升。
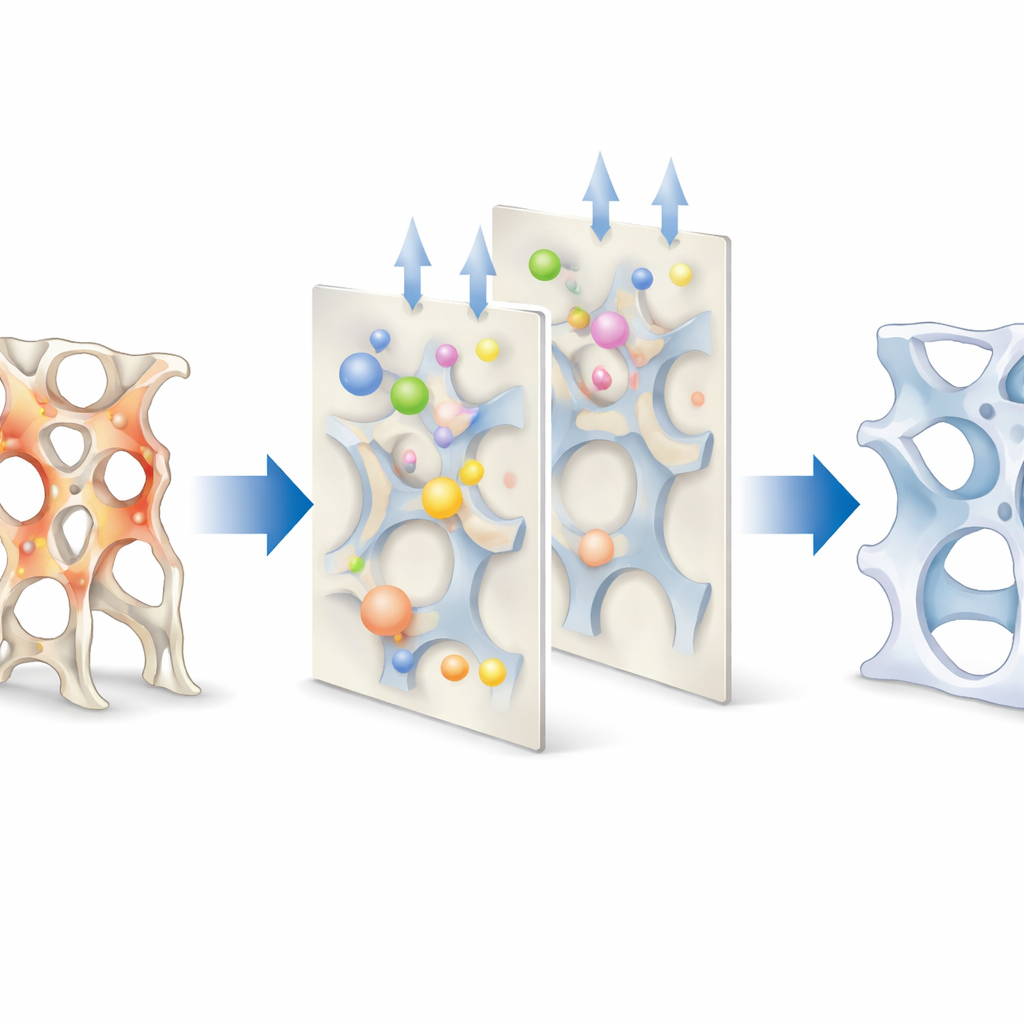
这对骨脆弱的人意味着什么
对普通读者而言,结论是:药物与运动并不是同一把旋钮上的可互换选项。在这个小鼠模型中,抗骨质疏松药物确实将骨代谢导向机械上有用的部位,但只有促骨形成疗法真正与承重活动联手,使椎骨变得更强。抗吸收药主要是将现有结构“固定”住,因此额外的负荷改善空间有限。相反,促骨形成药物与机械负荷共同作用,能在最关键的部位新增骨组织并减轻易损区域的应力。尽管仍需人体临床试验来验证,这项工作支持这样一种观点:在适当指导下,承重运动可以成为促骨形成治疗重建脆弱骨骼并降低骨折风险的特别有价值的助力。
引用: Schulte, F.A., Marques, F.C., Griesbach, J.K. et al. Combined physical and pharmacological anabolic osteoporosis therapies increase bone response and mechanoregulation in female mice. Nat Commun 17, 3759 (2026). https://doi.org/10.1038/s41467-026-70309-2
关键词: 骨质疏松, 骨重建, 机械负荷, 甲状旁腺激素, 硬化素抗体