Clear Sky Science · zh
FOXJ1通过调控微管动力学介导紫杉类药物耐药性
为什么一些抗癌药物会突然失效
许多晚期前列腺癌的男性起初对多西他赛等紫杉类化疗药物有反应,这类药物可以缩小肿瘤并延长生命。然而,几乎不可避免地,癌症学会了逃避这些药物并重新开始生长。这项研究提出了一个简单但关键的问题:在癌细胞内部,究竟是什么使它们能够躲过曾经非常有效的药物?
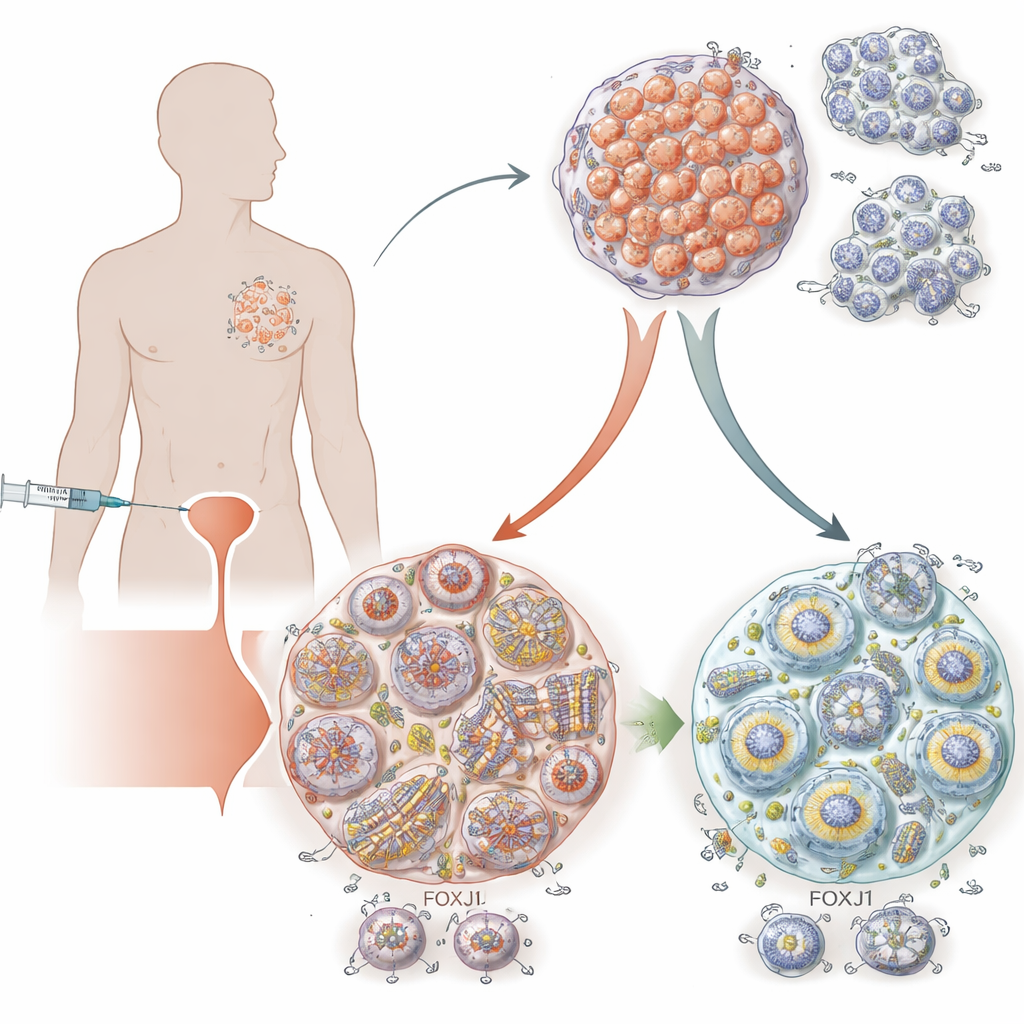
近距离观察细胞的内部支架
紫杉类药物通过作用于微管起效——微管是细胞内类似中空棒状的结构,既是细胞的支架又是运输“铁道”。当紫杉类药物与这些结构结合时,会使微管变得僵硬并聚集成束,阻塞细胞分裂和许多其它关键过程,直到癌细胞死亡。研究者使用了来源于真实前列腺癌患者并在小鼠体内生长的肿瘤样本来模拟临床情形:肿瘤最初对多西他赛缩小,随后变得耐药。通过比较耐药肿瘤与仍然敏感的肿瘤,他们寻找那些其活性发生改变、可能解释耐药的基因。
一个重塑药物反应的主开关
团队发现耐药肿瘤上调了一个名为FOXJ1的基因,该基因以帮助细胞形成称为纤毛的小毛状结构而著称。许多被FOXJ1下游激活的基因编码与微管直接相互作用的蛋白。在体外培养的前列腺癌细胞中,人为提高FOXJ1的表达使这些细胞更难被多西他赛及其类似药物卡巴他赛杀死。在显微镜下,富含FOXJ1的细胞在紫杉类药物结合后显示出较少的粗大聚集微管,提示药物不再有效地抓住其靶点。当研究者降低FOXJ1水平时,情况恰好相反:处理后微管更强烈地形成束状、药物与微管的结合增多,细胞更容易被杀死。
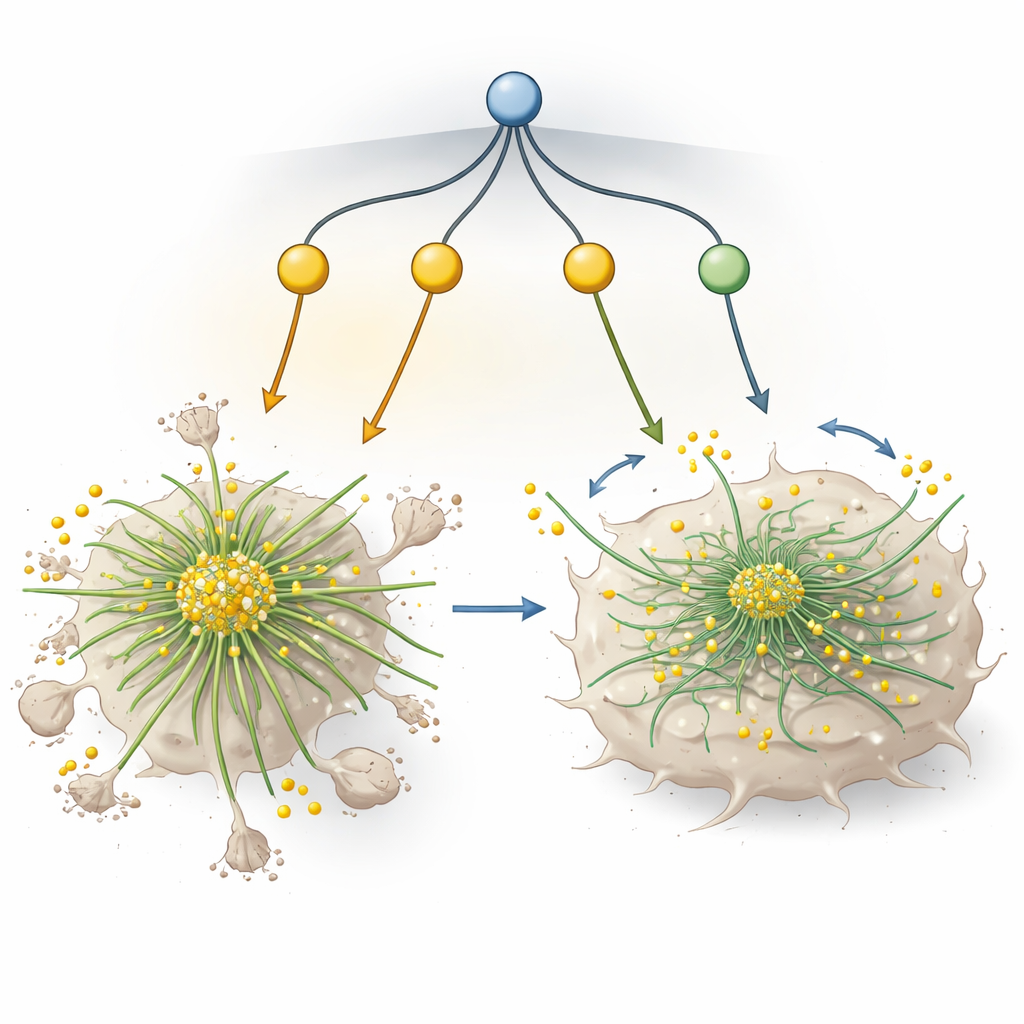
微管行为如何改变天平
进一步的实验证明,FOXJ1在任何药物加入之前就会改变微管的基本行为。缺乏FOXJ1的细胞具有生长速度更慢的微管以及与长期稳定纤维相关的化学修饰水平较低,但这些细胞却更容易结合紫杉类分子,并在处理时显著稳定。相反,较高的FOXJ1似乎促进了更为动态的微管网络,矛盾的是,这种网络更难被紫杉类药物冻结和束缚。一个受FOXJ1调控的蛋白TPPP3被发现是重要的同谋:当单独过度表达时,它在细胞培养和小鼠肿瘤中部分重现了相同的耐药表型。这表明存在一个由FOXJ1驱动的更广泛程序,细微地重塑微管支架,使紫杉类药物无法完全锁定它。
从培养皿到患者结局
研究者接着探问FOXJ1在真实患者中是否重要。在一组晚期前列腺癌男性的大型数据集中,先前接触过紫杉类药物的肿瘤更常见FOXJ1基因的拷贝增加并且倾向于表达更多FOXJ1。最显著的是,在一项大型临床试验中,患者接受了阻断激素治疗,部分患者加用多西他赛,那些肿瘤起始时FOXJ1水平高的患者似乎从化疗中获益不多。相比之下,FOXJ1低的患者在加入多西他赛后,无进展生存期和总体生存都明显改善。
这对未来癌症治疗意味着什么
简言之,这项工作将FOXJ1确定为一个细胞开关,通过改变细胞内部支架的行为,使前列腺癌细胞对紫杉类药物相对“视而不见”。在肿瘤样本中测量FOXJ1水平可能帮助医生预测哪些患者不太可能从紫杉类化疗中受益,从而避免他们承受无效治疗的副作用。从更长远看,抑制FOXJ1活性或针对像TPPP3这样的关键伙伴的疗法,或许可以重新使肿瘤恢复敏感,使已有药物(如多西他赛)再次发挥作用。通过理解癌细胞如何重接线其内部结构,研究者正开辟新的路径以延长关键化疗药物的有效期。
引用: Xie, F., Gjyrezi, A., Fein, D. et al. FOXJ1 mediates taxane resistance through regulation of microtubule dynamics. Nat Commun 17, 2763 (2026). https://doi.org/10.1038/s41467-026-69556-0
关键词: 前列腺癌, 化疗耐药, 紫杉类药物, 微管, FOXJ1