Clear Sky Science · zh
c-Myc转录活化CFL1以诱导类衰老表型并增强肺癌细胞迁移和增殖的旁观者效应
癌细胞变老却依然危险
我们大多数人认为衰老的细胞会减缓活性并变得无害。这项研究揭示了一个令人意外的转折:某些“衰老”肺癌细胞停止分裂,但释放的化学信号却实际上促使邻近的癌细胞生长和扩散。理解这一过程可能改变我们对癌症发展以及包括放疗在内的某些癌症治疗的认识。
具有黑暗面的生长开关
故事的中心是c-Myc,这个强大的基因推动细胞生长和分裂,并在许多癌症中表现为过度活跃。但当c-Myc被过度激活时,也可能把细胞推进一种称为衰老(senescence)的状态。衰老细胞仍然存活但永久停留在静止期,不再分裂。研究者显示,在正常肺成纤维细胞和非小细胞肺癌细胞中增强c-Myc使它们体积增大、停止细胞周期并呈现出衰老的经典特征——但并未引发细胞死亡。这些细胞没有消失,而是以改变并膨胀的形态持续存在。
细胞内会变形的蛋白质
衰老细胞不仅改变功能,还改变形态和内部支架。研究团队发现c-Myc强烈上调一种名为cofilin-1的蛋白,后者调控肌动蛋白(actin)的动力学,肌动蛋白赋予细胞结构并帮助其移动。c-Myc过表达的细胞在细胞质中出现更粗的肌动蛋白纤维,核内肌动蛋白含量也增加,类似老化细胞的模式。当研究者降低cofilin-1水平时,这些类衰老的改变被减弱,细胞的衰老标志染色明显减少,表明cofilin-1对c-Myc驱动的“老化”状态是必需的。
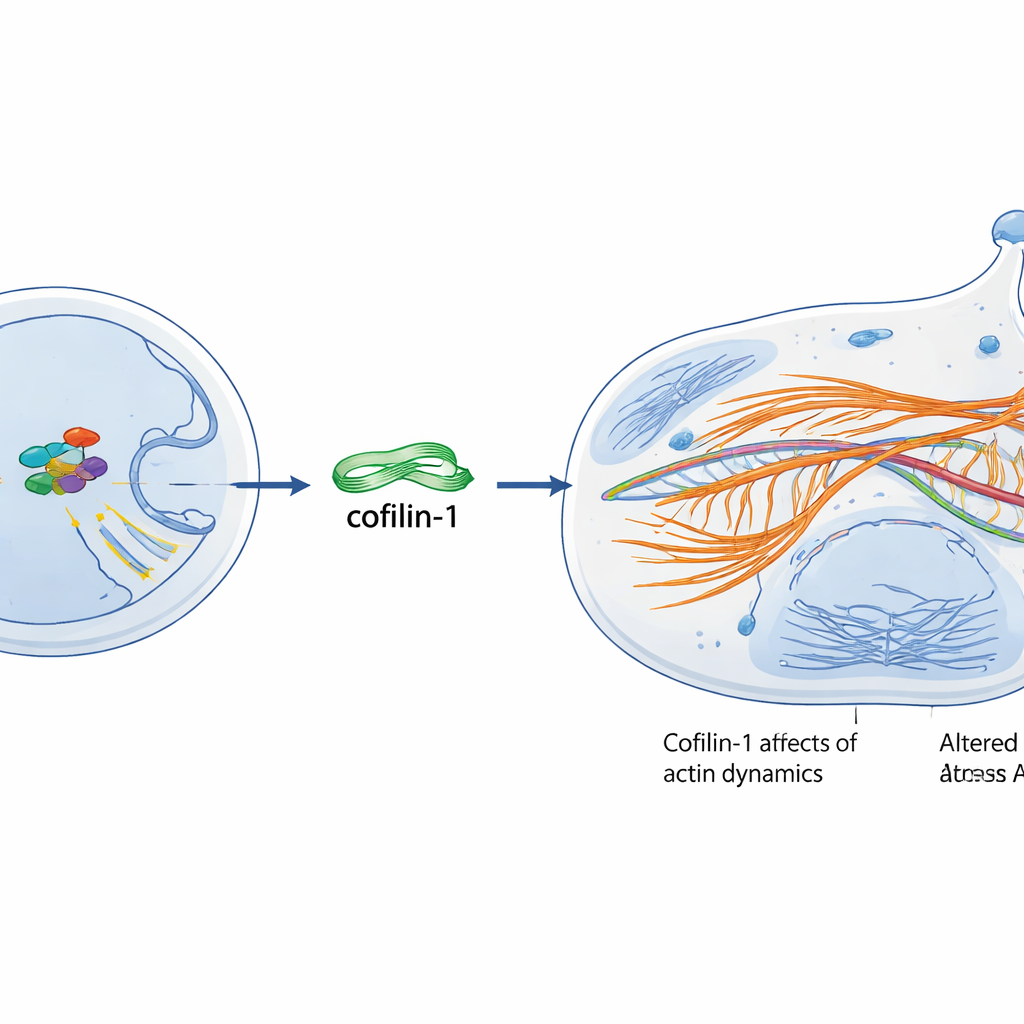
一个基因如何激活另一个基因
为了弄清c-Myc如何上调cofilin-1,研究者检查了控制CFL1基因(编码cofilin-1)的DNA开关或启动子。他们识别出c-Myc可以结合的特定短DNA基序。通过一系列报告基因构建和一种拉下c-Myc结合DNA的技术,他们证明在正常c-Myc水平下主要结合位于CFL1基因起始附近的位点,而在高表达条件下c-Myc可以占据三个被测位点。只有当c-Myc能进入细胞核并结合DNA时,cofilin-1水平才会上升并出现衰老表型——一种被工程化而留在细胞质的c-Myc形式无法触发这些效应。氧化应激(例如过氧化氢或X射线暴露)进一步强化了c-Myc与cofilin-1之间的关联,部分机制是通过增强关键位点的结合并促进两蛋白之间的物理相互作用。
促使邻居失范的“老”细胞
衰老细胞常常向周围释放一系列炎性和促生长分子,称为衰老相关分泌表型(SASP)。研究发现,被c-Myc驱动进入衰老的肺癌细胞产生的条件培养基,使未经处理的癌细胞迁移更快、形成更多克隆并增殖更多。当在衰老来源细胞中敲低cofilin-1时,这些旁观者效应显著下降,关键分泌因子白介素-6的水平也降低。这表明cofilin-1不仅是细胞内的结构蛋白,还参与控制衰老癌细胞释放以影响邻居的分子成分。
这对肺癌患者为何重要
为将实验室发现与真实疾病联系起来,作者分析了数百名非小细胞肺癌患者的数据。他们发现c-Myc和CFL1水平同时较高与较差的生存率相关,尤其在肺腺癌(最常见的亚型)中更为明显,而在鳞状细胞癌中则不明显。这提示c-Myc–cofilin-1轴可能在某一主要肺癌形式中尤为重要。简而言之,这项工作揭示了推进细胞进入表面上“老化”状态的基因,仍然可以通过重塑细胞骨架和分泌物来促进癌症进展。针对该通路——抑制c-Myc活性、cofilin-1或其在应激条件下的相互作用——可能为阻止衰老癌细胞助长更具侵袭性肿瘤提供新的策略。
引用: Chou, YT., Leu, JD., Yang, WY. et al. c-Myc transactivates CFL1 to induce senescence-like phenotype and potentiate the bystander effects for the migration and proliferation in lung cancer cells. Cell Death Discov. 12, 192 (2026). https://doi.org/10.1038/s41420-026-03065-3
关键词: 肺癌, 细胞衰老, c-Myc, cofilin-1, 肿瘤微环境