Clear Sky Science · zh
靶向脂肪细胞 ESRRA 通过中断补体 C3–CFD–MAC 级联的细胞器间串话缓解骨关节炎
为何关节痛不仅仅是磨损
许多人认为骨关节炎仅仅是关节随着年龄而磨损的结果。本研究呈现了一个截然不同的图景:我们的关节受到肝脏、骨髓脂肪和软骨之间隐秘对话的影响。理解这种远程的“器官间交流”可能为超越膝关节本身的新型治疗打开大门。
脂肪肝、骨髓脂肪与关节疼痛
研究者从一个重大难题出发:为何老化、肥胖或绝经后的人群常同时出现脂肪肝和脆弱、疼痛的关节?在小鼠中,他们发现当肝脏出现脂肪变(脂肪变性)且骨髓充满脂肪细胞时,膝关节软骨退化明显加速。骨髓脂肪细胞并非安静的储存组织,而是积极分泌一种称为 CFD 的蛋白;与此同时,脂肪肝释放另一种蛋白 C3。这两种循环因子在血液和关节内相遇,促使一个免疫系统的连锁反应被激活,从而损伤软骨细胞并加速骨关节炎进展。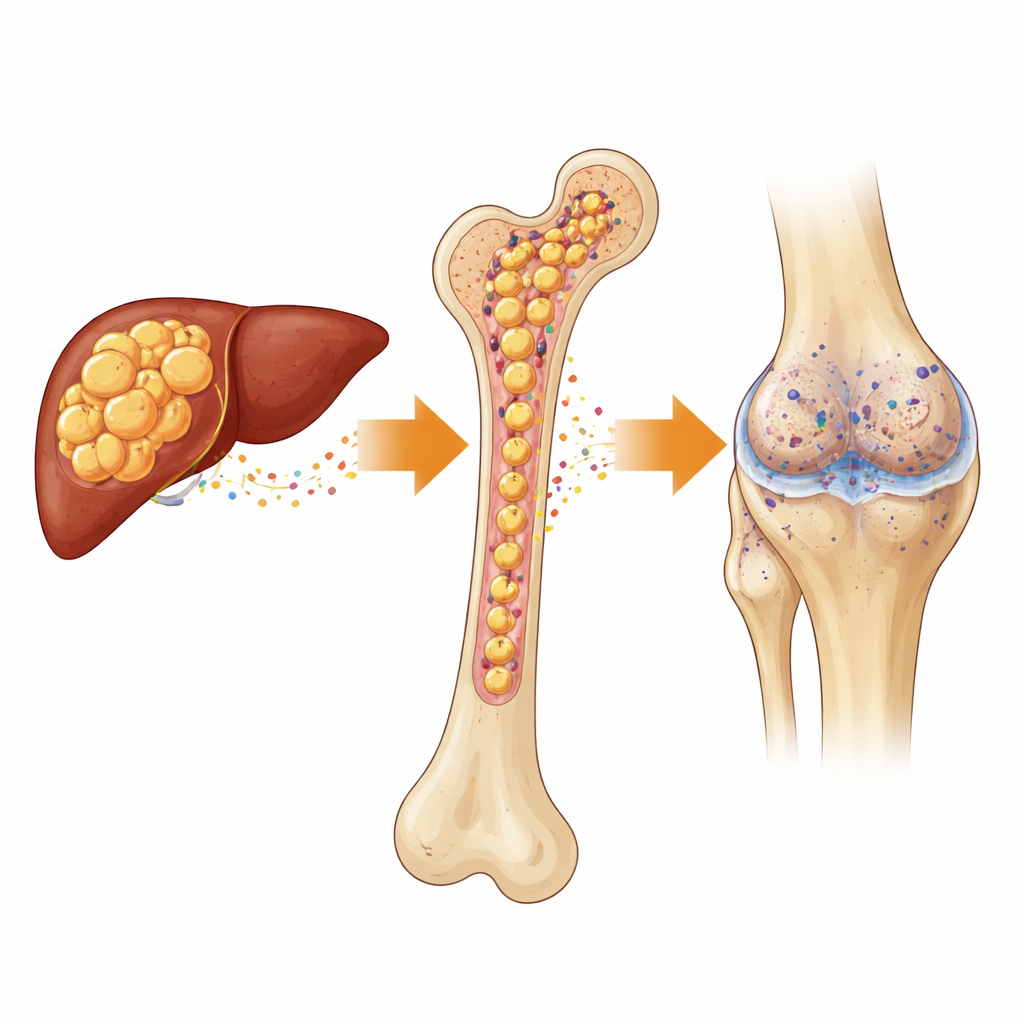
关节内的破坏性连锁反应
C3 和 CFD 属于补体系统,一组通常帮助抗感染的血浆蛋白。然而当该系统过度激活时,会伤害自身组织。在小鼠体内,肝源性的 C3 与髓源性的 CFD 联合,驱动强烈的“替代性补体”级联,最终形成的小型环状复合体(称为 MAC)刺入软骨细胞。在这些细胞内,损伤可追溯到信号开关(ERK1/2)的过度激活和线粒体的崩解——线粒体是维持细胞能量和健康的微小能量工厂。结果表现为细胞衰老、炎症增加以及软骨基质的降解。
抑制骨髓脂肪中的关键开关
团队随后探讨是否可以通过使骨髓脂肪细胞“静音”来保护关节。他们将注意力集中在脂肪细胞中的基因开关 ESRRA,该基因对代谢应激和胆固醇敏感。在仅在脂肪细胞中缺失 ESRRA 的基因工程小鼠中,他们发现骨髓脂肪不会随年龄或高脂高胆固醇饮食而扩张,尽管常规体脂和血脂大致不变。重要的是,这些缺乏 ESRRA 的骨髓脂肪细胞产生的 CFD 大大减少,使得会损伤关节的补体级联无法充分点燃。缺少脂肪细胞 ESRRA 的年老和过度喂养小鼠出现的骨关节炎程度明显更轻:关节软骨更厚,软骨下骨结构更趋正常,软骨细胞的 DNA 损伤更少、细胞死亡更少,且更显健康修复的迹象。
从肝–髓串话到人类相关性
为了将这些发现与人类疾病相联系,科学家们检查了公开的肝脏基因数据集和大型人类血浆蛋白研究。他们观察到脂肪肝患者的 C3 水平升高,CFD 随年龄上升并在低骨密度的女性中更高。在细胞培养实验中,用胆固醇或脂肪酸处理小鼠或人类肝细胞会促使 C3 的产生和分泌增加。当这种富含 C3 的肝细胞培养上清与富含 CFD 的骨髓脂肪培养上清共同作用于软骨细胞时,细胞迅速出现线粒体损伤和衰老标志。用已获批药物 Danicopan(专门靶向 CFD)阻断 CFD 活性,或通过化学抑制人类骨髓脂肪细胞中的 ESRRA 来减少 CFD 产生,在很大程度上可防止这些对类软骨细胞的有害影响。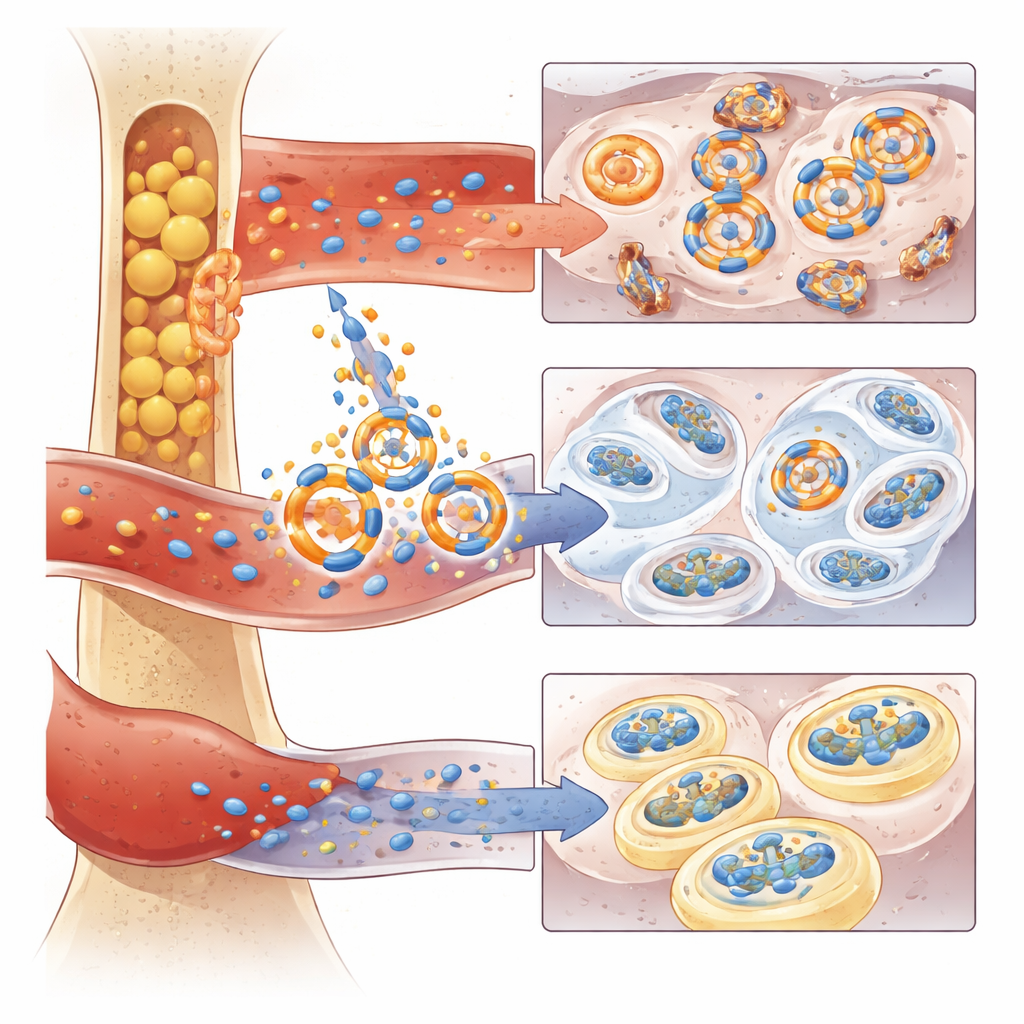
一种植物来源化合物可保护老化关节
最后,研究团队测试了一种天然的 ESRRA 阻断化合物是否能帮助整只动物。他们用来自传统药用植物的安道果内酯(andrographolide)处理极老龄小鼠。经过三个月,这些小鼠表现出肝脏脂肪减少、血中 C3 和 CFD 水平下降、骨髓脂肪减少以及骨骼更强。最引人注目的是,它们的膝关节自发性骨关节炎明显减少:软骨病变更少,软骨下骨和滑膜的增厚与瘢痕减轻,软骨中细胞衰老与损伤标志减少。与此同时,对健康软骨结构和细胞更新至关重要的蛋白恢复增加。
对骨关节炎患者的意义
这项工作把骨关节炎重新框定为不仅是局部关节问题,而是连接脂肪肝、骨髓脂肪与软骨的三向轴的结果。当肝脏和骨髓脂肪超载时,它们释放 C3 和 CFD,两者联合在软骨细胞上形成破坏性复合体并损伤其能量工厂。通过在脂肪细胞中下调 ESRRA——或直接阻断 CFD——可能有望切断这条有害链,同时保留免疫系统的大部分功能。尽管这些发现基于小鼠与细胞模型,但它们指向了靶向代谢与免疫串话的未来疗法,为与年龄和代谢相关的骨关节炎带来病程修正的希望。
引用: Huang, T., Wang, Z., Gao, L. et al. Targeting adipocyte ESRRA alleviates osteoarthritis via interrupting inter-organelle crosstalk of complement C3-CFD-MAC cascade. Bone Res 14, 49 (2026). https://doi.org/10.1038/s41413-026-00527-3
关键词: 骨质疏松, 脂肪肝, 骨髓脂肪, 补体系统, 关节退化