Clear Sky Science · zh
基于临床特征、认知特性、炎症相关蛋白和 EEG 数据预测抑郁发作
为何将脑电波与血检转化为情绪线索
抑郁症影响数以亿计的人群,但临床上医生仍主要通过与患者交谈和问卷来作出诊断。本研究探讨是否可以将睡眠问题、认知能力、脑活动和血液中免疫分子的潜在模式,与现代计算技术结合,提供一种更客观的信号来判断某人是否处于抑郁发作期。如果这种信号被证实可靠,未来可能帮助医生更早检测抑郁并更精确地定制治疗方案。
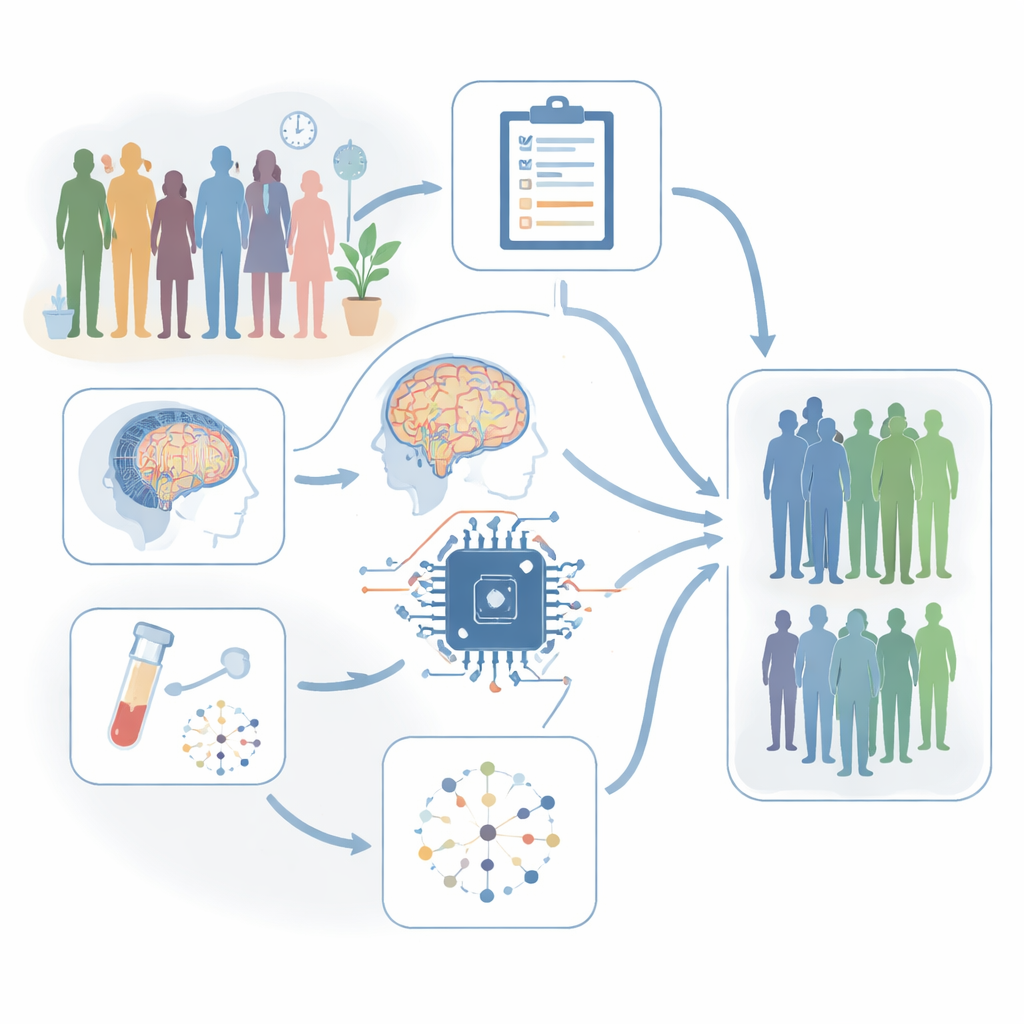
将多种线索汇聚一处
研究者随访了115名重性抑郁成人,并与66名健康志愿者进行了比较。对每位参与者,他们收集了广泛的信息:抑郁、焦虑、快感缺失与失眠的症状量表;记忆、注意力与视觉思维的详细测试;一种称为 EEG 微状态的特殊脑电记录,用以追踪脑网络的快速切换;以及血液中 30 多种与炎症相关蛋白的水平。56 名患者在四周抗抑郁治疗后进行了复测。用于训练计算模型的是患者的初次数据加上全部健康对照,而复测数据连同相同的健康组则用于检验这些模型在新测量中识别抑郁的能力。
计算机如何寻找抑郁的指纹
由于数据集信息丰富但样本量中等,团队首先对数据进行了仔细清理,去除常缺失的测量项,并用成熟的统计方法填补较小的缺失值。随后,他们使用一种称为 Lasso 回归的技术,将数十个候选测量项缩减为对区分抑郁与非抑郁最有信息量的一小部分。从中筛选出八项突出特征:失眠严重度、衡量视觉信息处理与构建能力的视空间任务表现、特定 EEG 模式微状态 D 的平均持续时间,以及血液中五种炎症相关蛋白(IL-8、IL-18、MMP-8、CD40 和 CASP-8)。这些特征被输入到六种不同的机器学习算法中,算法学习识别将抑郁者与健康者区分开的模式。
模型学到的关于抑郁时身体与大脑的信息
六种计算模型均表现良好,但在复测数据的验证中,k 近邻(k-NN)模型表现突出,约 95% 的病例被正确分类,并展示出抑郁与非抑郁参与者之间几乎完全的分离。为探查哪些信号最重要,研究者采用了一种解释方法,将每个特征视为对模型决策有贡献的“参与者”。两种免疫蛋白 IL-8 与 IL-18 显得尤其有影响力,其次是失眠评分、蛋白 MMP-8、免疫受体 CD40、酶 CASP-8、视空间思维能力以及 EEG 微状态 D 的平均时长。当模型中移除所有炎症蛋白时,其性能显著下降,这表明免疫系统标志物并非对其他临床或脑部测量的冗余回声,而是提供了独特的信息。
这对睡眠、认知与炎症意味着什么
结果模式与越来越多将慢性低度炎症与紊乱脑网络与抑郁联系起来的研究相一致。本研究中的抑郁者往往睡眠较差、在某些视空间任务上思维不够清晰、EEG 中微状态 D 的时序发生改变,并且血液中若干免疫蛋白的水平也有变化。与其依赖任何单一测量,不如说这些领域的联合模式共同形成了对抑郁发作的有力信号。研究结果还强调,失眠和微妙的认知变化不仅是副作用,而是抑郁症图景中的核心部分。
这项工作如何助力未来护理
对非专业读者来说,结论是抑郁在身体与大脑中留下可被精心挑选的检测项和智能计算分析捕捉到的痕迹。该研究表明,一套相对较小的睡眠评分、认知测量、脑电特征与血液蛋白面板,能够共同高精度地区分抑郁者与健康个体。尽管此项工作在单一医院完成,还需在更大、更多样化的人群和更长随访期中得到验证,但它展示了一条通向更客观、以生物学为依据的工具的路径,这些工具未来或许能辅助(而非替代)临床访谈用于抑郁的诊断与监测。
引用: Sun, W., Yang, H., Sun, C. et al. Prediction of depressive episodes based on clinical features, cognitive characteristics, inflammation-related proteins, and EEG data. Transl Psychiatry 16, 202 (2026). https://doi.org/10.1038/s41398-026-03960-4
关键词: 重性抑郁障碍, 生物标志物, 炎症, EEG 微状态, 机器学习