Clear Sky Science · tr
Klinik kaynaklı çekirdek biyopsiler kullanılarak hastaların sınıflandırılması ve ilaç hedeflerinin değerlendirilmesi için gastrointestinal tümörlerin kişiselleştirilmiş sinyal yolakları analizi
Bu araştırma hastalar için neden önemli
Kanser hekimleri giderek daha fazla tedavileri her hastanın tümörünün benzersiz biyolojisine göre eşleştirmeye çalışıyor. Pankreas, kolon, karaciğer veya safra yolları gibi sindirim sistemi kanserleri için bu özellikle acildir; çünkü bu kanserler yaygındır, çoğunlukla geç evrede teşhis edilir ve tedavileri zordur. Bu çalışma, küçük biyopsi örneklerinden birçok kanserle ilişkili proteinin aktivitesini okuyabilen yeni bir laboratuvar yöntemini araştırıyor; amaç, doktorların bireysel hastalar için daha kesin tedaviler seçmesine yardımcı olmaktır.
DNA listelerinden yaşayan sinyallere
Günümüzde çoğu “kişiselleştirilmiş” kanser bakımı tümördeki DNA değişikliklerini okumaya dayanıyor. Güçlü olmakla birlikte, yalnızca DNA hücre içindeki hangi sinyallerin gerçekten aktif olduğunu ve büyümeyi yönlendirdiğini göstermez. Bu sinyaller proteinler tarafından taşınır; bunların birçoğu doğrudan ilaçlarla hedeflenebilir. Araştırmacılar, klasik Western blot yönteminin modern bir uyarlaması olan ve DigiWest olarak adlandırılan yüksek verimli bir teknik kullanarak aynı anda yaklaşık 130–200 protein ve bunların aktif formlarını ölçtüler. Önemli olarak, bu yöntem tek bir iğne biyopsisi kadar materyal gerektirir, bu da gerçek klinik kullanım için uygun olmasını sağlar.
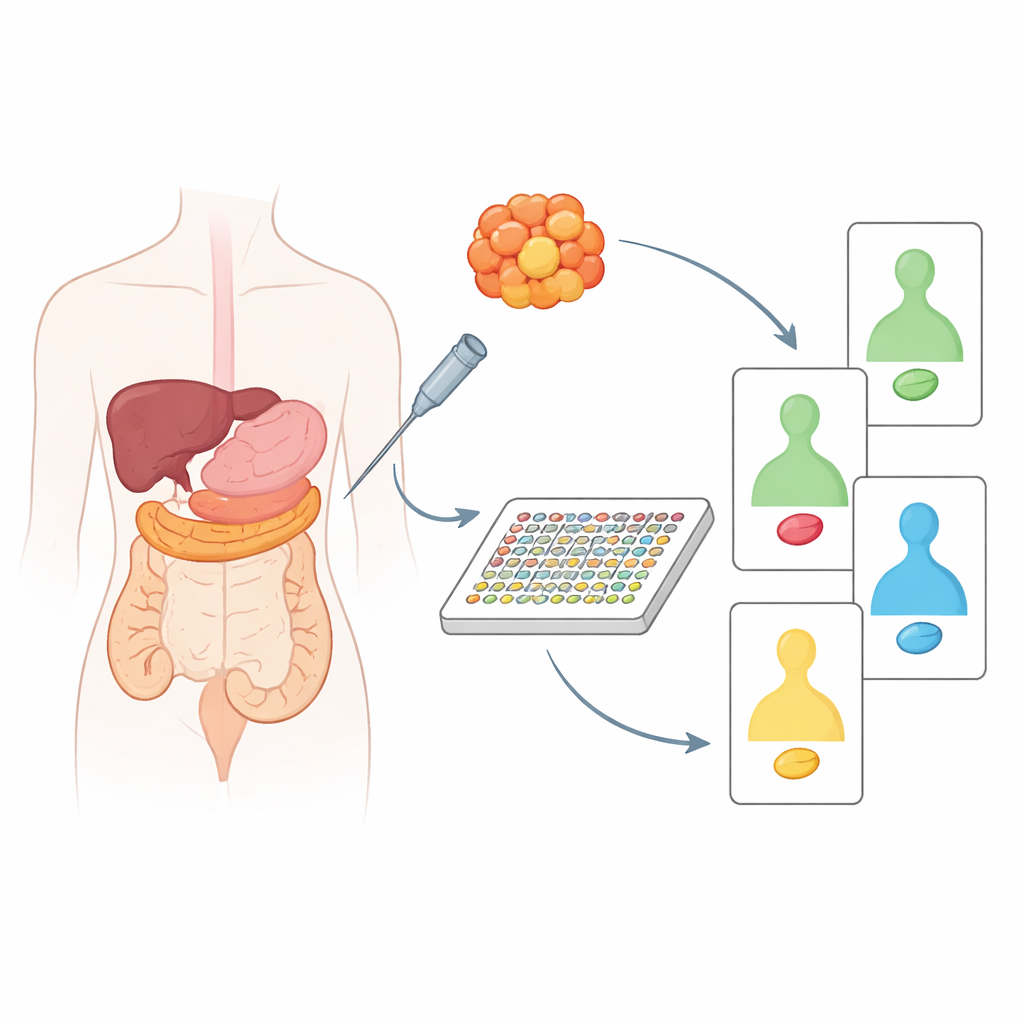
Tümör dokusunun sağlıklı komşusuyla karşılaştırılması
Çalışma ekibi önce pankreas veya kolorektal kanserli 20 hastadan saklanmış dokuları, her zaman aynı kişiden alınmış yakınlardaki kansersiz doku ile eşleştirerek analiz etti. Tümörleri kendi sağlıklı karşıtlarıyla karşılaştırarak, hangi proteinlerin gerçekten kansere bağlı olarak değiştiğini—organlar arasındaki normal farklılıkları yansıtmak yerine—görebildiler. Bu, p53, Ras, PTEN gibi iyi bilinen kanser koruyucuları ve sürücülerin davranışlarında belirgin farklılıklar ortaya koydu. Örneğin pankreas tümörleri büyümeyi teşvik eden sinyallerin artması ve koruyucu proteinlerin kaybını gösterme eğilimindeyken, kolon tümörleri kendi özgün bozulan yol desenlerine sahipti. Araştırmacılar bu protein değişikliklerine göre örnekleri kümelediğinde, pankreas kanserlerini biyolojik olarak farklı iki gruba ayırabildiler ve kolon kanserleri arasında hasta yaşı ve tümörün bağırsaktaki konumuyla ilişkili anlamlı farklar tespit ettiler.
Bireysel tümörlerin sinyal aktivitesi “barkodları”
Grup ortalamalarının ötesine bakarak, bilim insanları her tümör için ayrıntılı bir protein profili oluşturdular. Bu profiller, mTOR, MAPK/Erk, Wnt veya bağışıklıkla ilgili faktörleri içeren gibi hangi sinyal yollarının özellikle aktif veya kapalı olduğunu öne çıkardı. Ölçülen birçok protein mevcut ilaçların doğrudan hedefleri veya bu hedeflerin hemen aşağısında yer aldığından, ekip hangi ilaçların bir tümörün ana büyüme motorlarına müdahale edebileceğini çıkarabildi. Retrospektif olgularda üçte ikisinde, tümör ilerlemesini muhtemelen besleyen bir veya daha fazla yolu işaret edebildiler. Ayrıca bağışıklık hücresi belirteçleriyle dolu “sıcak” immünoterapiye cevap verebilecek kanserleri ve çarpıcı biçimde benzersiz imzalara sahip sıra dışı vakaları belirlediler.
Yöntemi gerçek hastalarda uygulamak
Klinikte ne kadar işe yaradığını test etmek için araştırmacılar daha sonra DigiWest’i Moleküler Tümör Kurulu tarafından incelenen çeşitli gastrointestinal kanserleri olan 14 hastadan alınan taze iğne biyopsilerine uyguladılar. Bu hastaların karmaşık hastalık öyküleri ve sıklıkla daha önce aldıkları tedaviler vardı. Eşleşmiş sağlıklı doku mevcut olmadığından, her tümörün protein düzeyleri anormal derecede yüksek veya düşük sayılacak değerleri tanımlamak için grup içindeki medyan düzeyle karşılaştırıldı. Bu daha sıkı düzenlemeye rağmen, 14 tümörden 12’si açık, tedaviyle ilişkili yol aktivitesi desenleri gösterdi. İki ayrıntılı örnekte protein verileri, bir kolorektal kanserde FGFR2 geninin DNA düzeyinde amplifikasyonunu ve bir karaciğer kanserinde mTOR baskılayıcısının kaybını doğrulayarak Kurul’un FGFR engelleyici veya mTOR engelleyici ilaçları değerlendirme yönündeki kararını güçlü biçimde destekledi. Genel olarak, DigiWest bulguları ana genetik sürücülerle uyumlu bulundu ve değerlendirilebilen olguların çoğunda ilaç hedefleri önerdi.
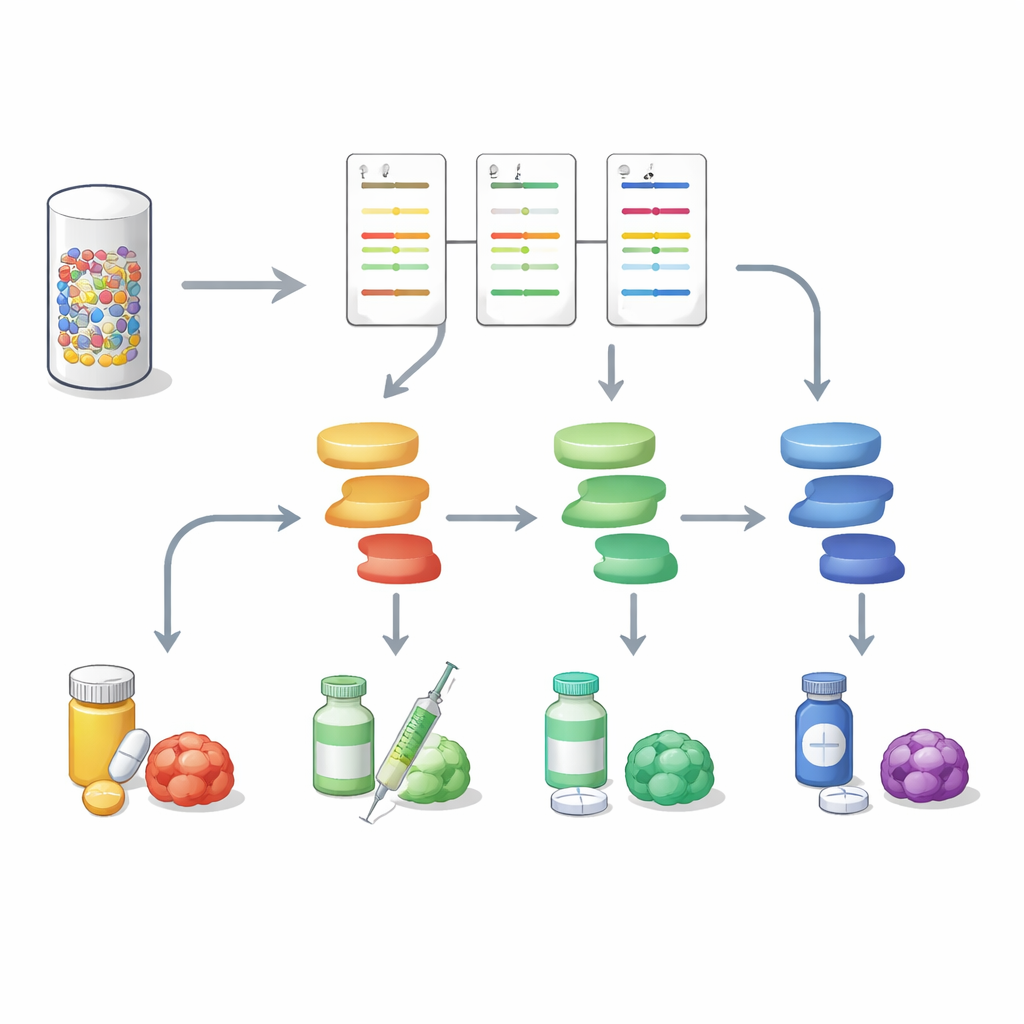
Daha eksiksiz tümör portrelerine doğru
Bu çalışma, protein sinyallemesini DNA dizilemesiyle paralel olarak analiz etmenin gastrointestinal tümörler hakkında daha zengin ve eyleme geçirilebilir bir tablo sağlayabileceğini gösteriyor. Küçük bir biyopsiyi çoklu yol aktivite haritasına çevirerek, DigiWest belirli bir kanserde hangi moleküler anahtarların gerçekten açık olduğunu ve hangi ilaçların bunlara en iyi şekilde müdahale edebileceğini ayırmaya yardımcı olur; ayrıca ortaya çıkan direnç yollarını da işaretleyebilir. Daha büyük çalışmalara hâlâ ihtiyaç olsa da, bu yaklaşım yüksek içerikli protein profillemeyi günlük kişiselleştirilmiş onkolojiye pratik bir şekilde getirme ve her hastanın yaşayan tümörüne, sadece genetik planına değil, daha uygun tedavi planları sunma yolunda bir adım sunuyor.
Atıf: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Anahtar kelimeler: kişiselleştirilmiş onkoloji, gastrointestinal kanser, proteomik, biyopsi profilleme, hedefe yönelik tedavi