Clear Sky Science · tr
Kvantil-spesifik genetik etkileri modelleyerek poligenik risk tahminini geliştirmek
Genetik riski tahmin etmek göründüğünden neden daha zor
Genetik risk skorları bize kimin diyabet veya kalp hastalığı gibi durumlara daha yatkın olduğunu söyleme vaadinde bulunuyor, ancak bugünkü araçlar çoğunlukla genlerin herkesin riskini aynı basit şekilde etkilediğini varsayıyor. Oysa birçok gerçek dünya özellikleri çarpık: çoğu insan normal değerler etrafında kümelenirken daha küçük bir grup yüksek risk kuyruğunda yer alır. Bu çalışma, genetik risk skorları oluşturmanın yeni bir yolunu tanıtıyor; sadece ortalama kişiye bakmak yerine genlerin sonuç dağılımının tamamı boyunca, özellikle sağlık kararları için en önemli olan yüksek risk kuyruklarında nasıl davrandığını inceliyor.
Ortalama kişinin ötesine bakmak
Standart poligenik risk skorları, yüzlerce veya binlerce DNA varyantının küçük etkilerini toplayarak bir kişinin bir özellik veya hastalığa genetik yatkınlığını tahmin eder. Bu skorlar genellikle bir nüfustaki ortalama sonucu hedefleyen yöntemlere dayanır. Bu, bir özellik yaklaşık olarak simetrik olduğunda, örneğin birçok grupta boy gibi, iyi çalışır. Ancak glukoz ve trigliseridler gibi kan ölçümleri için dağılım çarpıktır: çoğu insan sağlıklı seviyelerde kümelenirken azınlık çok daha yüksek değerlere sahiptir. Önceki çalışmalar bazı genetik varyantların orta yerine uçları etkilediğine işaret etmiş; bu da tek bir "ortalama-temelli" skorun önemli sinyalleri kaçırabileceği anlamına gelir.

Spektrum boyunca genetik riski puanlamanın yeni bir yolu
Araştırmacılar kvantil-temelli poligenik risk puanlaması (QPRS) adını verdikleri bir yöntem geliştirdiler. Her bir DNA varyantı için tek bir genetik etki tahmin etmek yerine QPRS, bu etkinin özellik dağılımının düşükten yükseğe çeşitli noktalarında nasıl değiştiğini ölçer. Teknik olarak bu, ortalama yerine bir özelliğin örneğin %10, %50 veya %90’lık yüzdeliklerini modelleyen kvantil regresyonunu kullanır. Her yüzdelik için ekip varyant etkilerini tahmin etmek üzere genom çapında bir tarama yapar, standart filtreleme araçlarıyla bilgilendirici varyantları seçer ve ayrı bir risk skoru inşa eder. Bu çoklu skorlar—her yüzdelik için bir tane—ardından birlikte bir tahmin modeline beslenir, böylece nihai risk tahmini dağılımın farklı kısımlarında etkili olan genetik etkileri yansıtır.
Simüle ve gerçek genomlarla yöntemi test etmek
QPRS’nin ne zaman işe yaradığına bakmak için yazarlar önce geniş bir Kore kohortundan alınan gerçek genetik verileri kullanarak kontrollü simülasyonlar yaptılar. Bir grup senaryoda bazı genetik varyantlar ortalama düzeyi değiştirmek yerine özelliğin ne kadar değiştiğini etkileycek şekilde tasarlandı; bu, öncelikle dağılımın uçlarını etkileyen varyantları taklit ediyor. Bu durumda QPRS, konvansiyonel skorlardan daha iyi bir şekilde özelliğin düşük ve yüksek yüzdeliklerini tahmin etti ve özellikle özellik değerleri gürültülü veya güçlü bir şekilde çarpık olduğunda tahmin hatasını önemli ölçüde azalttı. Ayrıca gerçekten etkili varyantların daha fazlasını geri kazandı; tam dağılımı modellemenin ortalama-temelli yöntemlerin gözden kaçırdığı sinyalleri ortaya çıkarabileceğini gösterdi. Aşırı aykırı değerlerle boğulmuş başka bir simülasyon setinde QPRS genellikle standart yaklaşımlardan daha dayanıklıydı, ancak çok şiddetli bozulmalarda yöntemin daha basit, medyan odaklı bir versiyonu en iyi performansı gösterdi.
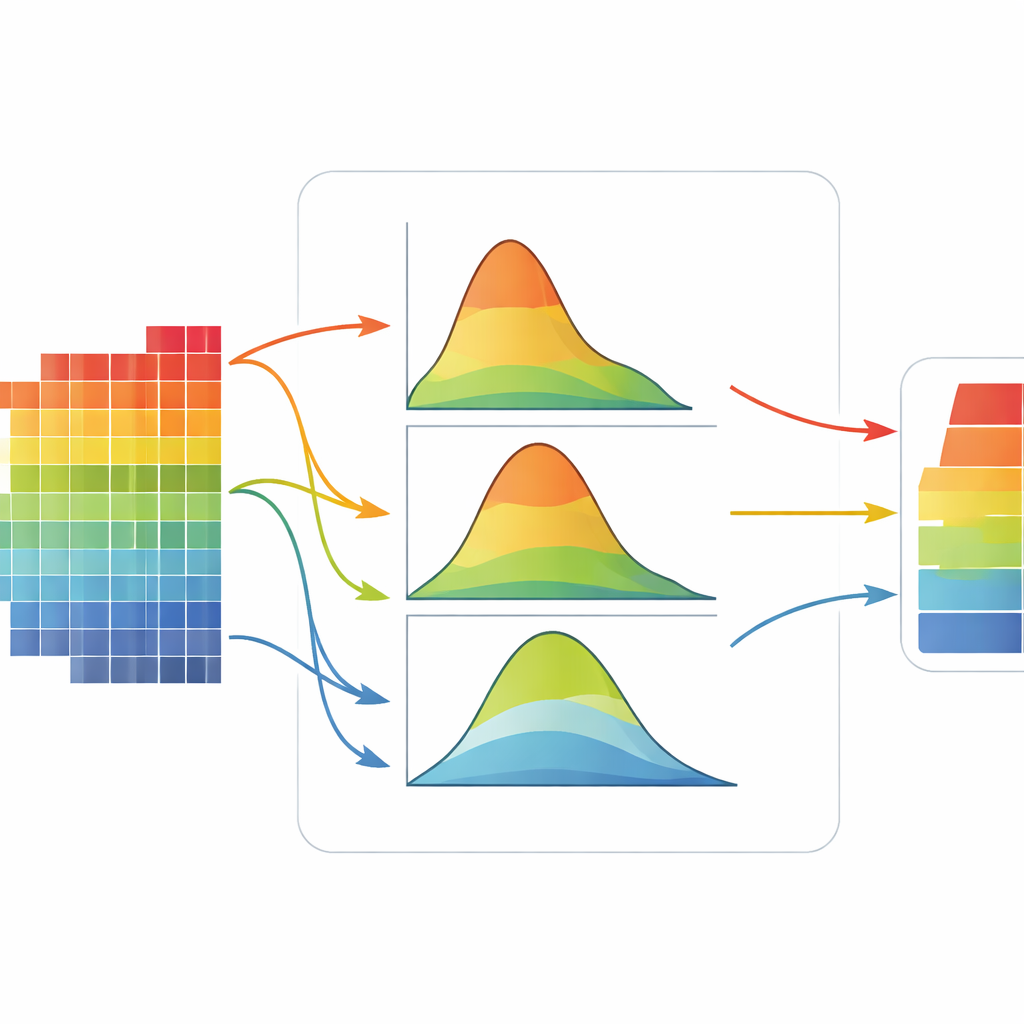
Kan yağları ve şeker hakkında verilerin söyledikleri
Ekip ardından QPRS’yi Kore Genom ve Epidemiyoloji Çalışması’ndan sekiz binden fazla yetişkinin gerçek verilerine uyguladı; odak noktası metabolik sağlığın ana göstergeleri olan post-müdahale kan glukozu ve kan trigliseridleriydi. Bu özellikler belirgin şekilde sağa çarpık olup yüksek riskli bireylerin belirgin bir kuyruğuna sahiptir. Trigliseridler için QPRS, tek başına veya yaş, vücut kitle indeksi ve sigara içme durumu gibi klinik faktörlerle birleştirildiğinde, popüler çeşitli puanlama yöntemlerini açıkça geride bıraktı. Glukozda, klinik faktörler hesaba katıldıktan sonra genel genetik sinyal daha zayıf olduğundan kazançlar daha ılımlı ama hâlâ görülebilirdi; özellikle QPRS geleneksel skorların üzerine eklendiğinde fark belirgindi. Analiz ayrıca glukoz dağılımının düşük ve yüksek bölümleri arasında etkileri tersine dönen veya güç değiştiren bireysel genetik varyantları ortaya koydu—tek bir ortalama-temelli tahminin büyük ölçüde gizleyeceği desenler.
Genetik risk tahmini için bunun anlamı
Bu çalışma, genetik riski ortalama sonuçla bağlanan tek bir sayı olarak ele almanın çarpık veya yüksek değişkenliğe sahip özellikler için yanıltıcı olabileceğini gösteriyor. Genetik etkilerin bir özelliğin tüm spektrumu boyunca nasıl farklılaştığını açıkça modelleyerek QPRS, özellikle klinik olarak en çok kaygı duyulan yüksek risk kuyruklarında risk tahminini keskinleştiriyor. Ayrıca hastalıkla ilişkili özellikleri genlerin nasıl şekillendirdiğine dair daha zengin bir resim sunuyor; uç değerler için özellikle önemli olan varyantları öne çıkarıyor. Uzun vadede, geleneksel ortalama-temelli skorları QPRS gibi kvantil-farkındalıklı yaklaşımlarla birleştirmek, kişiselleştirilmiş tıp için daha nüanslı ve bilgilendirici genetik risk araçlarına yol açabilir.
Atıf: Kim, S., Goo, T., Park, T. et al. Enhancing polygenic risk prediction by modeling quantile-specific genetic effects. Sci Rep 16, 11749 (2026). https://doi.org/10.1038/s41598-026-47082-9
Anahtar kelimeler: poligenik risk skorları, kvantil regresyonu, genetik tahmin, kan yağları, tip 2 diyabet