Clear Sky Science · tr
SNCA üçlemesi, insan orta beyin organoidlerinde nörodejenerasyondan önce proteostaz ve ekstrasellüler mimariyi bozuyor
Bu araştırma gündelik yaşam için neden önem taşıyor
Parkinson hastalığı titreme ve hareket sorunlarıyla bilinir, ancak belirtiler ortaya çıkmadan çok önce beyin hücreleri kendi iç ve dış ortamlarını dengede tutmakta zorlanmaya başlar. Bu çalışma, insan orta beyninin laboratuvarda yetiştirilen küçük modellerini kullanarak bu en erken değişimleri gerçek zamanlı izlemesine olanak tanıyor. Parkinson’a bağlı önemli bir genin fazladan kopyalarının hem sinir hücreleri içindeki proteinleri hem de onları çevreleyen destekleyici matrisi nasıl bozduğunu ortaya koyarak, nöronlar ölmeden çok önce hastalığı tespit etmeye ve belki de yavaşlatmaya yönelik yeni yaklaşımlara işaret ediyor.
Laboratuvarda mini insan orta beyinleri inşa etmek
Bu erken olayları incelemek için araştırmacılar, insan deri veya kan hücrelerinden indüklenmiş pluripotent kök hücrelere dönüştürülmüş hücrelerle başladılar. Bu hücrelerden bazılarında alfa-sinükleini kodlayan SNCA geninin üç kopyası bulunuyordu; bu genin çoğaltılması agresif, erken başlangıçlı Parkinson’a yol açtığı biliniyor. Diğerleri aynı hastadan dikkatle düzeltilmiş kontrol sürümleriydi ve ayrıca SNCA’nın silindiği bir hücre hattı da vardı. Bu hücreleri aşamalı bir tarif takip ederek yönlendirerek ekip, insan orta beyninin mimarisini taklit eden ve Parkinson’da dejenerasyona uğrayan dopamin üreten nöronları içeren üç boyutlu orta beyin organoidleri—küresel kümeler—yetiştirdi. 
Protein üretiminin kapanması olmadan nöron içinde erken stres
Bilim insanları bu organoidleri 50 ve 100 günlük büyüme dönemlerinde incelediler; bu pencere nöronların olgunlaştığı ancak geniş ölçekli hücre ölümü henüz başlamadığı bir dönemi kapsıyor. SNCA üçlemesine sahip organoidlerde alfa-sinüklein ve hastalıkla ilişkili modifiye formları ile doğal olarak oluşan neuromelanin belirgin şekilde yükselmişti. Bu hücrelerin içinde protein üretimi ve stres yanıtlarını düzenleyen birkaç ana kontrol anahtarı aşırı aktif hale geldi; özellikle mTOR, AKT, ERK ve eIF2α yolları. İlginç bir şekilde, bu “büyüme ve stres” sinyallerindeki artışa rağmen yeni protein sentezinin genel hızı sabit kaldı. Ayrıntılı ribozom profillemesi, toplu bir yavaşlama ya da hızlanma yerine hücrelerin belirli mesajların proteinlere çevrilmesini ince ayarladığını gösterdi—gen aktivitesi değişse bile protein çıktısını kontrol altında tutan bir tamponlama stratejisi gibi görünüyordu.
Nöral bağlantılarda ve çevreleyen iskelette kaymalar
Bu değişmiş sinyallemenin sonuçlarını anlamak için ekip binlerce proteini ve RNA molekülünü aynı anda taradı. Fazladan SNCA taşıyan organoidlerde sinapslarla, sinyal salınımıyla ve akson büyümesiyle ilişkili olanlar da dahil olmak üzere sinir iletişimine katılan birçok proteinde koordineli bir artış bulundu; bu, nöronal devrelerin yeniden kablolanmakta olduğunu düşündürüyor. Aynı zamanda hücreleri stabilize eden ve bağlantılarını şekillendiren ağsı iskelet olan ekstrasellüler matrisin bileşenlerinde geniş bir düşüş vardı. İlginç bir şekilde, nöronların etrafında yoğun örtüler oluşturan perinöronal ağları meydana getiren bazı matris öğeleri, diğer matris bileşenleri azalırken RNA ve protein düzeylerinde artmıştı; bu, beynin yapısal ortamında karmaşık, tekdüze olmayan bir yeniden düzenlemeye işaret ediyor.
Kırılgan dopamin nöronlarının çevresinde kalınlaşan ağlar
Yüksek çözünürlüklü konfokal görüntüleme kullanarak araştırmacılar bu yeniden düzenlemeyi doğrudan görselleştirdiler. SNCA üçlemesine sahip organoidlerde, özellikle kondroitin sülfat proteoglikanları ve aggrecan proteini açısından zengin periselüler ve interstisyel matris yapılarda daha güçlü boyama gözlendi. Genel nöronal popülasyonların etrafında bu değişiklikler 100. günde belirgin hale geldi. Ancak tirosin hidroksilaz ile işaretlenmiş dopamin üreten nöronların etrafında perinöronal ağ birikimi daha erken ortaya çıktı; 50. günde zaten belirgindi ve olgunlaşmayla birlikte sürdü. SNCA tamamen eksik olan organoidlerde bile bu nöronların çevresinde değişmiş matris görüldü; bu durum alfa-sinükleinin fazlasının olduğu kadar yokluğunun da ekstrasellüler ortamın hassas dengesini bozabildiğini gösteriyor. 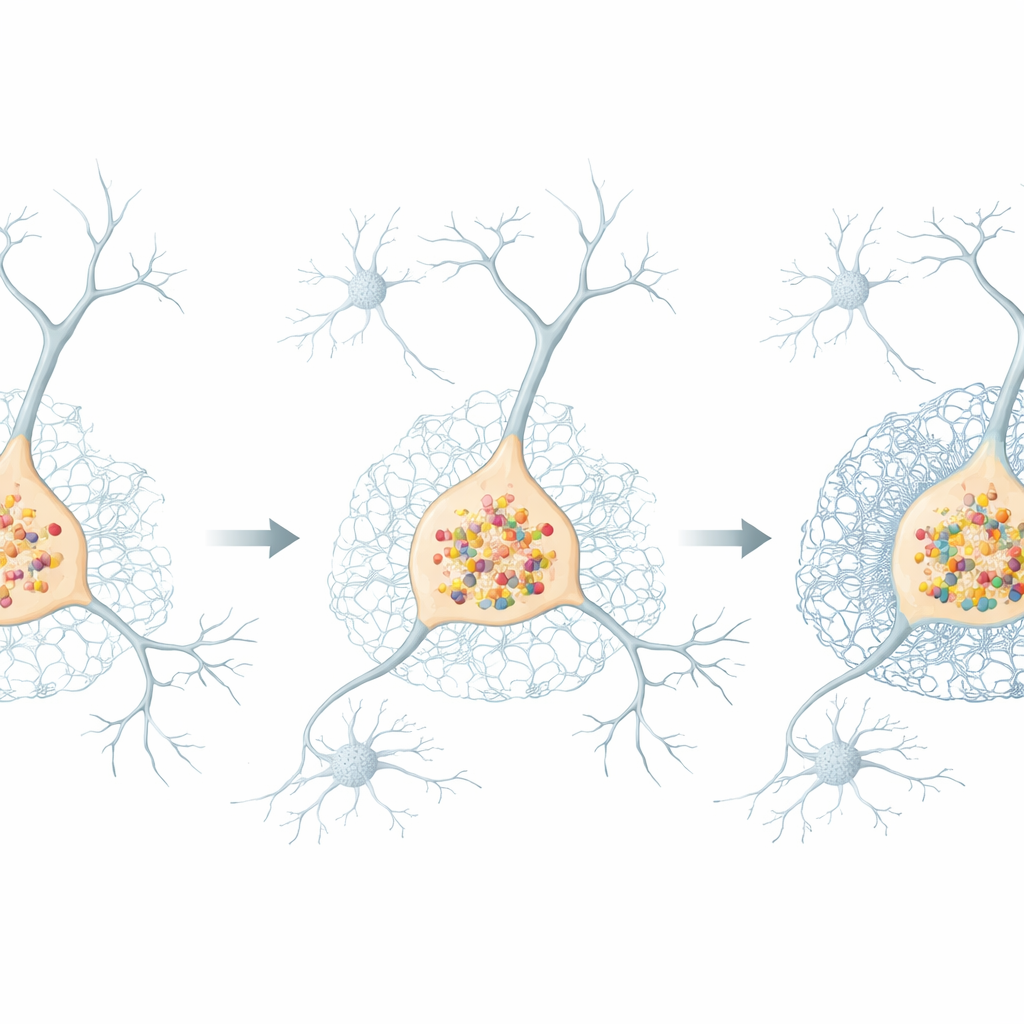
Parkinson anlayışı için bunun anlamı ne
Bir arada ele alındığında, bulgular bu insan orta beyin modelinde SNCA’nın fazladan kopyalarının dopamin nöronları ölmeden çok önce hücrenin protein yönetim sistemlerini bozduğunu ve ekstrasellüler iskeli yeniden şekillendirdiğini gösteriyor. Basit bir yüklenme sonucu protein üretiminin kapanması yerine hücreler çeviri konusunda hedeflenmiş ayarlamalar yapıyor ve erken, hücre tipine özgü perinöronal ağ kalınlaşması gözleniyor. Halk için bunun anlamı, Parkinson’un nöronların içindeki ve etraflarındaki dokuda ev içi düzenin ince bir başarısızlığı olarak başlayabileceği; bu da zamanla bu hücreleri daha kırılgan hale getiren sert, değişmiş bir çevre yaratıyor. Bu erken “proteostaz–matris” eksenini tanımlayarak çalışma, Parkinson’u daha erken tespit etme ve hem hücrelerin iç protein ekonomisini hem de dış destek ağını dengeleyerek sinir hücrelerini koruyacak tedaviler geliştirme fırsatlarını öne çıkarıyor.
Atıf: Statoulla, E., Zafeiri, M., Chalkiadaki, K. et al. SNCA triplication disrupts proteostasis and extracellular architecture prior to neurodegeneration in human midbrain organoids. npj Parkinsons Dis. 12, 81 (2026). https://doi.org/10.1038/s41531-026-01292-0
Anahtar kelimeler: Parkinson hastalığı, alfa-sinüklein, orta beyin organoidleri, perinöronal ağlar, proteostaz