Clear Sky Science · sv
Personlig analys av signalvägar i gastrointestinala tumörer för patientstratifiering och utvärdering av läkemedelsmål med kliniskt erhållna kärnbiopsier
Varför denna forskning är viktig för patienter
Cancerläkare försöker i allt större utsträckning anpassa behandlingar till varje tumörs unika biologi. För cancer i matsmältningssystemet—såsom i pankreas, tjocktarm, lever eller gallgångar—är detta särskilt angeläget eftersom dessa cancerformer är vanliga, ofta upptäcks sent och är svåra att behandla. Denna studie undersöker en ny laboratoriemetod som kan läsa aktiviteten hos många cancerrelaterade proteiner från mycket små biopsiprover, med målet att hjälpa läkare välja mer precisa behandlingar för enskilda patienter.
Från DNA-listor till levande signaler
Idag förlitar sig större delen av ”personlig” cancerbehandling på att läsa DNA-förändringar i en tumör. DNA är kraftfullt, men visar inte vilka signaler inne i cellen som faktiskt är påslagna och driver tumörtillväxt. De signalerna förmedlas av proteiner, många av vilka kan riktas direkt med läkemedel. Forskarna använde en höggenomströmningsteknik kallad DigiWest, en modern variant av den klassiska Western blot, för att mäta omkring 130–200 proteiner och deras aktiva former samtidigt. Viktigt är att metoden bara kräver ungefär lika mycket material som en enkel nålbiopsi, vilket gör den lämplig för kliniskt bruk i verkligheten.
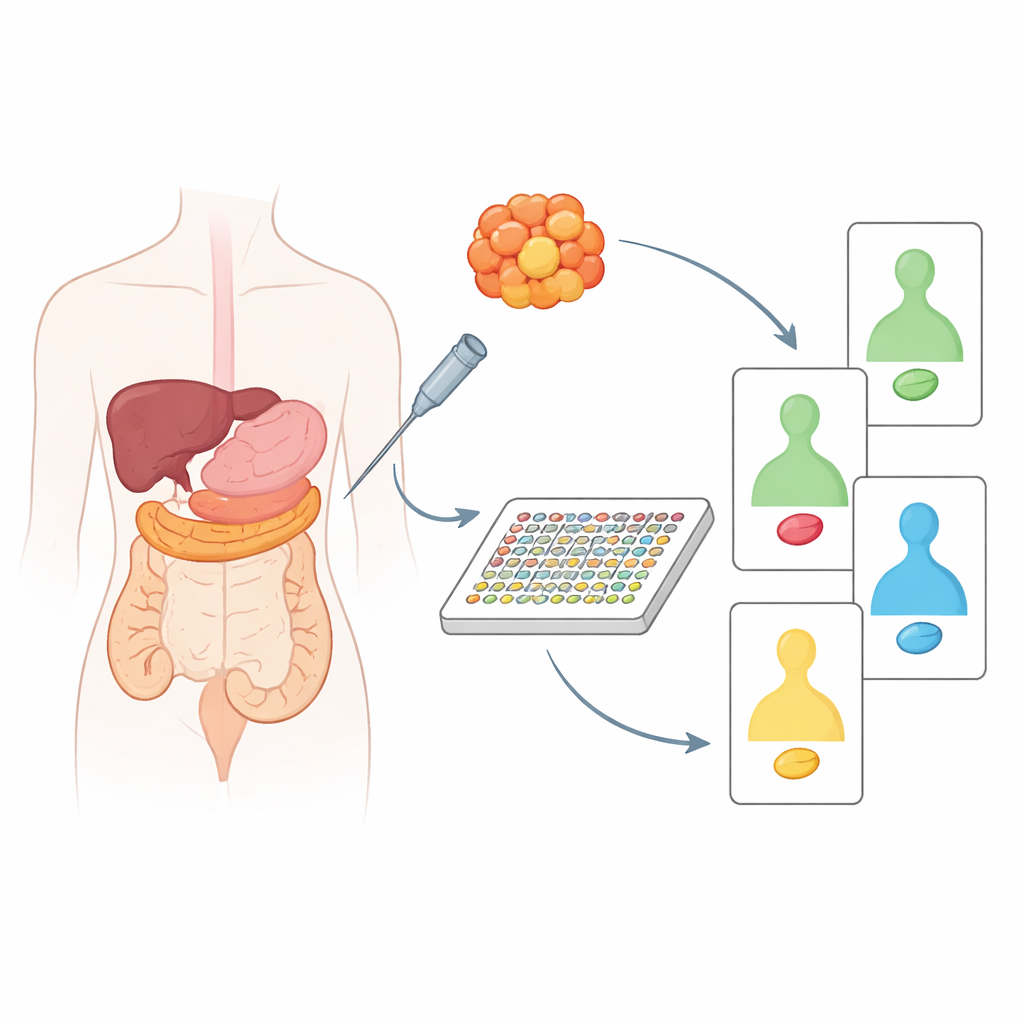
Jämförelse av tumörvävnad med dess friska granne
Teamet analyserade först arkiverad vävnad från 20 patienter med pankreas- eller kolorektalcancer, alltid parvis med närliggande icke‑cancerös vävnad från samma person. Genom att jämföra tumörer med deras egna friska motsvarigheter kunde de se vilka proteiner som verkligen förändrats av cancer snarare än att spegla normala skillnader mellan organ. Detta avslöjade tydliga skillnader i beteendet hos välkända cancerbeskyddare och drivare, såsom p53, Ras, PTEN med flera. Pankreastumörer visade till exempel ofta förbättrade tillväxtfrämjande signaler och förlust av skyddande proteiner, medan kolonstumörer hade ett eget distinkt mönster av störda vägar. När forskarna klustrade proverna baserat på dessa proteinförändringar kunde de dela in pankreascancer i två biologiskt skilda grupper och upptäcka meningsfulla skillnader bland koloncancer i relation till patienternas ålder och tumörens placering i tarmen.
Individuella tumör ”streckkoder” för signalaktivitet
Bortom gruppmedelvärden byggde forskarna en detaljerad proteinprofil för varje tumör. Dessa profiler lyfte fram vilka signalvägar—såsom de som involverar mTOR, MAPK/Erk, Wnt eller immunsystemrelaterade faktorer—som var särskilt aktiva eller nedreglerade. Många av de mätta proteinerna är direkta mål för befintliga läkemedel, eller ligger precis nedströms sådana mål, vilket gjorde det möjligt för teamet att härleda vilka läkemedel som kan störa en tumörs huvudsakliga tillväxtmotorer. I tre fjärdedelar av de retrospektiva fallen kunde de peka ut en eller flera vägar som sannolikt drev tumörprogression. De identifierade också tumörer med många immuncellsmarkörer, vilket tyder på ”heta” cancerformer som kan svara på immunterapi, samt ovanliga fall med särskilt unika signaturer.
Användning av metoden på verkliga patienter
För att testa nyttan vid sängkanten tillämpade forskarna DigiWest på färska nålbiopsier från 14 patienter med olika gastrointestinala cancerformer vars fall granskades av en molekylär tumörkonferens. Dessa patienter hade komplexa sjukdomshistorier och ofta tidigare behandlingar. Eftersom matchande frisk vävnad inte fanns tillgänglig jämfördes varje tumörs proteinnivåer med medianvärdet i gruppen för att definiera vad som räknades som abnormt högt eller lågt. Även med denna striktare uppställning visade 12 av de 14 tumörerna tydliga, behandlingsrelevanta mönster av pathway‑aktivitet. I två detaljerade exempel bekräftade proteindata en DNA‑nivåförstärkning av FGFR2‑genen i en koloncancer och förlusten av en mTOR‑broms i en levercancer, vilket starkt stödde konferensens överväganden om FGFR‑blockerande respektive mTOR‑blockerande läkemedel. Sammantaget överensstämde DigiWest‑fynden med centrala genetiska drivkrafter och föreslog läkemedelsmål i de flesta bedömbara fallen.
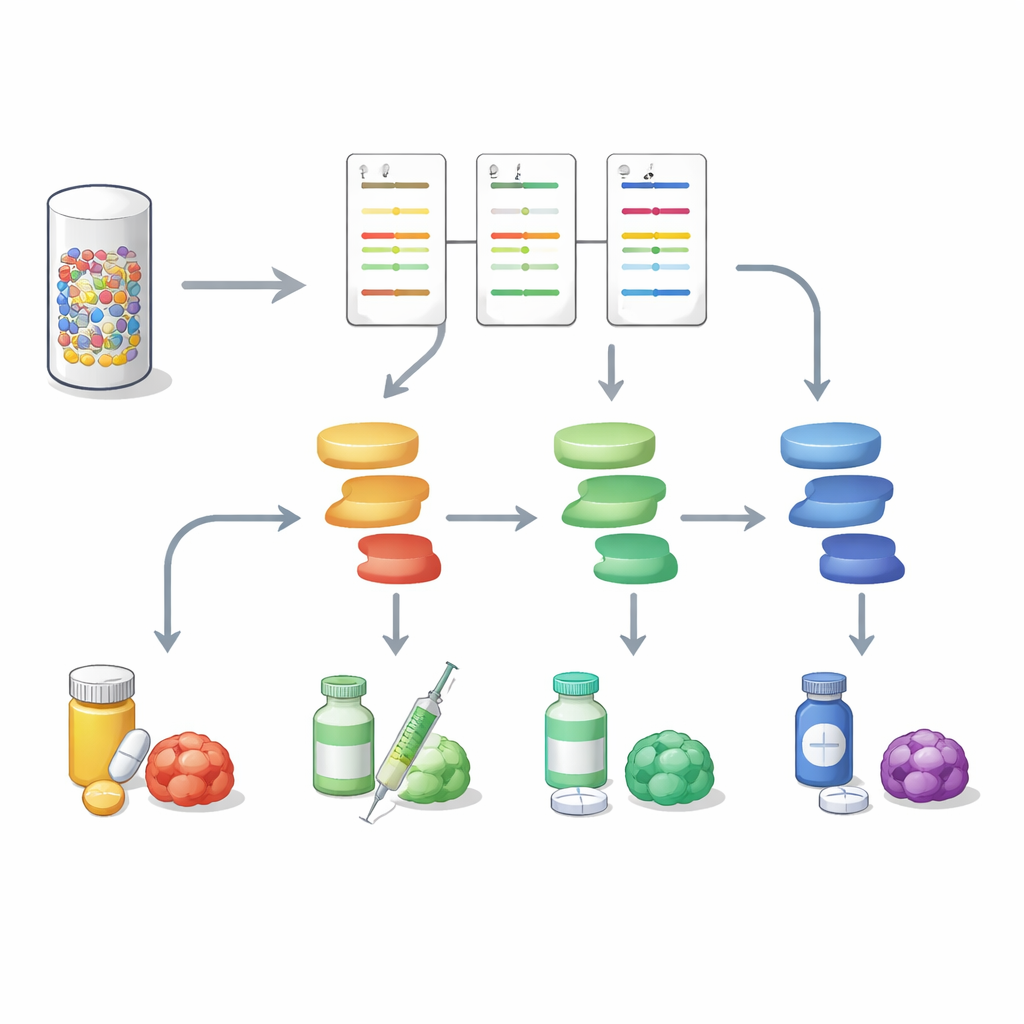
Mot mer fullständiga tumörporträtt
Denna studie visar att analys av proteinsignalering parallellt med DNA‑sekvensering kan ge en rikare och mer handlingsbar bild av gastrointestinala tumörer. Genom att förvandla en liten biopsi till en karta över aktivitet i flera vägar hjälper DigiWest att skilja vilka molekylära strömbrytare som verkligen är på i en given cancer och vilka läkemedel som bäst kan slå mot dem, och kan också peka ut framväxande resistensvägar. Även om större studier fortfarande krävs, erbjuder tillvägagångssättet ett praktiskt sätt att föra höginnehålls‑proteinprofilering in i vardaglig precisionsonkologi och komma närmare behandlingsplaner skräddarsydda efter varje patients levande tumör, inte bara dess genetiska ritning.
Citering: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Nyckelord: precisionsonkologi, gastrointestinal cancer, proteomik, biopsiprofiler, målinriktad terapi