Clear Sky Science · sv
miRNA:s roll i regleringen av CYP450-enzymer och UDP-glukuronosyltransferaser i den mänskliga levern
Varför detta spelar roll för läkemedel
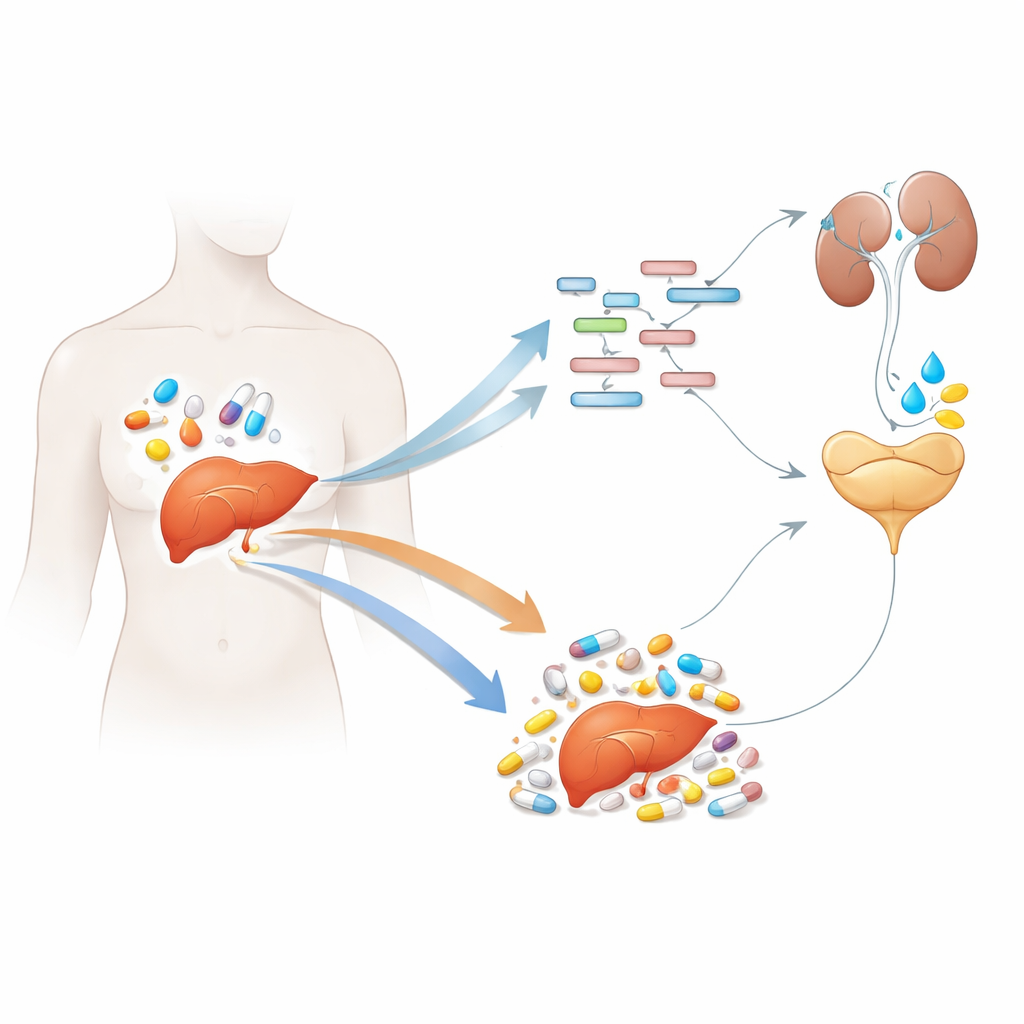
När du sväljer en tablett måste kroppen omvandla den kemikalien till något den säkert kan använda eller göra sig av med. Mycket av detta arbete sker i levern, som förlitar sig på en stor uppsättning hjälpproteiner för att bryta ner läkemedel. Den här studien undersöker hur små RNA-molekyler, kallade mikroRNA, tyst kan skruva upp eller ner dessa hjälpare och därigenom potentiellt förändra hur olika personer svarar på samma läkemedel.
Små regulatorer med stor påverkan
MikroRNA är korta bitar av genetiskt material som inte bygger proteiner själva utan i stället finjusterar hur mycket protein andra gener producerar. Genom att fästa vid slutet av en gens budskap kan de bromsa eller blockera produktionen av motsvarande protein. Eftersom ett enda mikroRNA kan påverka många gener samtidigt, och varje gen kan påverkas av flera mikroRNA, bildar de ett tätt styrnät som hjälper levern att anpassa sig vid stress, infektion och skada. Samma nätverk kan också ändra hur snabbt läkemedel bearbetas.
Levern verktygslåda för läkemedelsnedbrytning
Levern förlitar sig i hög grad på två enzymfamiljer för att hantera läkemedel och andra främmande kemikalier. Den ena familjen, känd som CYP450-enzymer, utför de inledande kemiska förändringarna som börjar bryta ner läkemedelsmolekyler. En annan familj, kallad UGT-enzymer, fäster sedan en liten sockerliknande tagg som gör dessa föreningar lättare att lösa i vatten och spola ut ur kroppen. Ett fåtal CYP- och UGT-medlemmar gör det mesta av jobbet för de läkemedel vi använder dagligen, så en förändring i deras nivåer kan starkt påverka hur mycket läkemedel som finns i blodet och hur länge det kvarstår.
På jakt efter mikroRNA–enzym-länkar
Forskarna använde först flera online-databaser för att förutsäga vilka mikroRNA som kan binda till generna bakom viktiga CYP- och UGT-enzymer. Av nästan 500 möjliga parningar begränsade de listan till 22 mikroRNA som faktiskt var detekterbara i mänskliga leverprov. Dessa prover kom från personer med en rad allvarliga leversjukdomar samt en jämförelsegrupp utan sådana tillstånd. För varje prov fanns redan precisa mätningar av enzymproteinnivåer. Genom att jämföra mikroRNA-mängder med enzymmängder sökte de mönster där högre mikroRNA-nivåer motsvarade lägre enzymnivåer, vilket är ett kännetecken för direkt kontroll.
Vad mönstren avslöjade
Flera mikroRNA visade sådana negativa samband med viktiga enzymer. Till exempel tenderade vissa mikroRNA att öka när CYP2C8, CYP2C9 eller CYP3A4—enzymer som hanterar många vanliga läkemedel—minskade. Liknande relationer framträdde för UGT-enzymer som är involverade i andra steget av läkemedelsbearbetningen. För att undersöka dessa relationer djupare inriktade sig teamet på två särskilt lovande kombinationer: ett mikroRNA (miR-655-3p) som misstänktes rikta in sig på CYP2C8 och ett annat (miR-200a-3p) som misstänktes rikta in sig på UGT1A3. De introducerade dessa mikroRNA, tillsammans med 3'-ändarna av enzymgenerna, i leverliknande celler odlade i labbet och mätte hur starkt en ljusproducerande testsignal släcktes.
Inzoomning på en bekräftad kontrollbrytare
Cellförsöken visade att miR-200a-3p tydligt och kraftigt minskade signalen kopplad till UGT1A3, vilket indikerar att det kan fästa direkt vid denna gens budskap och dämpa dess aktivitet. I kontrast försvagade miR-655-3p endast CYP2C8-signalen svagt och inte på ett statistiskt övertygande sätt, vilket tyder på att om det påverkar detta enzym alls kan det ske endast under vissa förhållanden eller i samspel med andra faktorer. Studien lyfte också fram andra intressanta mikroRNA som följde förändringar i enzymnivåer över olika leversjukdomar, vilket antyder ett bredare kontrollnät som fortfarande behöver kartläggas.
Vad detta betyder för patienter och läkemedel
Sammanfattningsvis stöder arbetet idén att mikroRNA fungerar som subtila dimmerknappar för leverns läkemedelshanterande maskineri. Genom att bidra till att identifiera vilka mikroRNA som justerar specifika enzymer lägger studien grunden för att förklara varför två personer som får samma dos av ett läkemedel kan uppleva olika nytta eller biverkningar—särskilt när leversjukdom föreligger. Ett tydligt exempel är miR-200a-3p, som direkt kan sänka nivåerna av ett nyckel-UGT-enzym och därigenom eventuellt sakta ned elimineringen av vissa läkemedel. På sikt kan förståelsen av dessa små regulatorer förbättra läkemedelsdosering, vägleda valet av säkrare behandlingar för personer med leversjukdom och öppna dörren för nya terapier som justerar mikroRNA-aktivitet i sig.
Citering: Szeląg-Pieniek, S., Perużyńska, M., Komaniecka, N. et al. The involvement of miRNAs in CYP450 enzymes and UDP-glucuronosyltransferases regulation in the human liver. Sci Rep 16, 14255 (2026). https://doi.org/10.1038/s41598-026-45113-z
Nyckelord: mikroRNA, läkemedelsmetabolism, leverenzym, farmakogenomik, epigenetisk reglering