Clear Sky Science · sv
Capecitabin kombinerat med fekal mikrobiotatransplantation förhindrar kolorektal cancers progression genom korrigering av mikrobiell dysbios och immunreglering
Varför din tarm kan spela roll vid tjock- och ändtarmscancer
Kolorektal cancer är en av världens dödligaste cancerformer, och de flesta patienter behandlas med kemoterapeutiska läkemedel som kan vara hårda för kroppen. Samtidigt har forskare funnit att de biljoner mikrober som lever i våra tarmar påverkar både cancerrisk och hur vårt immunsystem beter sig. Denna studie ställer en enkel men kraftfull fråga: om vi kombinerar ett standardläkemedel mot tjocktarmscancer med en transplantation av hälsosamma tarmbakterier, kan vi då både dämpa sjukdomen och återställa den mikrobiella gemenskap som kemoterapi och cancer rubbar?
En ny samverkan mellan läkemedel och mikrober
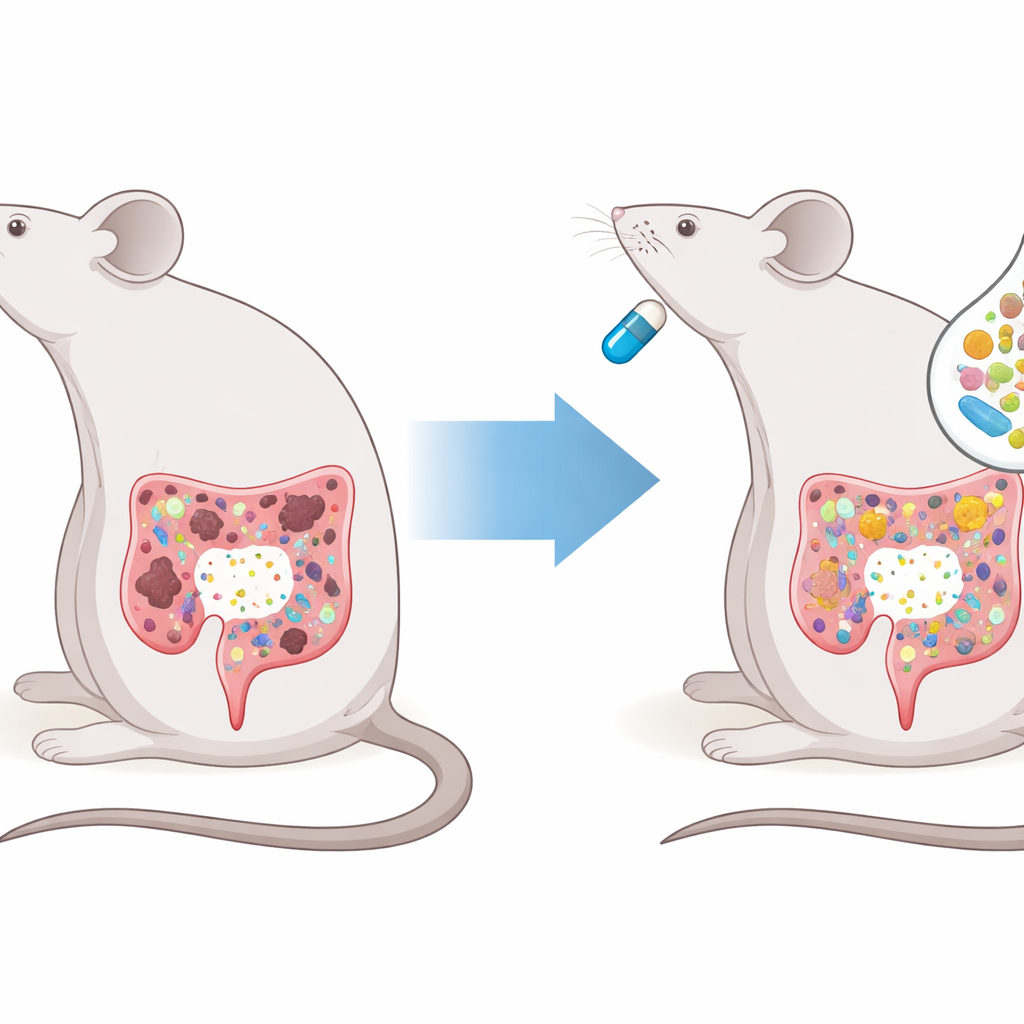
Forskarna använde en väletablerad musmodell för kolorektal cancer och jämförde fyra grupper: friska möss, tumörbärande möss, möss behandlade med kemopillret capecitabin, och möss behandlade med både capecitabin och fekal mikrobiotatransplantation (FMT). FMT innebär att leverera tarmmikrober från friska donatorer in i tarmen, här via en skonsam lavemang. Capecitabin ensam minskade antalet och storleken på cancerväxter i tarmen, men kombinationsbehandlingen gav ännu bättre resultat. Möss som fick båda behandlingarna hade färre och mindre tumörer, längre tarmar som närmade sig normallängd, mindre vävnadsskada vid mikroskopi, mindre viktminskning och en högre överlevnadsgrad.
Att laga en rubbad tarmgemenskap
Tjocktarmscancer och dess kemiska behandlingar störde den normala balansen av tarmbakterier hos mössen. Nyttiga grupper som vanligtvis hjälper till att bryta ner fiber och producera skyddande kortkedjiga fettsyror minskade, medan potentiellt skadliga arter som driver inflammation och kan skada DNA blev vanligare. Capecitabin minskade flera av dessa misstänkta bakterier men störde också vissa hjälpsamma typer ytterligare, vilket tyder på en blandad påverkan på den mikrobiella gemenskapen. Tillägg av FMT skiftade systemet åt ett hälsosammare håll: mått på rikedom och diversitet återhämtade sig, och den övergripande artsammansättningen närmade sig den som ses hos normala möss. Datoranalys av mikrobiella gener antydde att sjukdomsassocierade banor blev mindre aktiva, medan banor kopplade till skydd, reparation och kontrollerad celltillväxt återställdes.
Hur tarmförändringar formar immunförsvaret
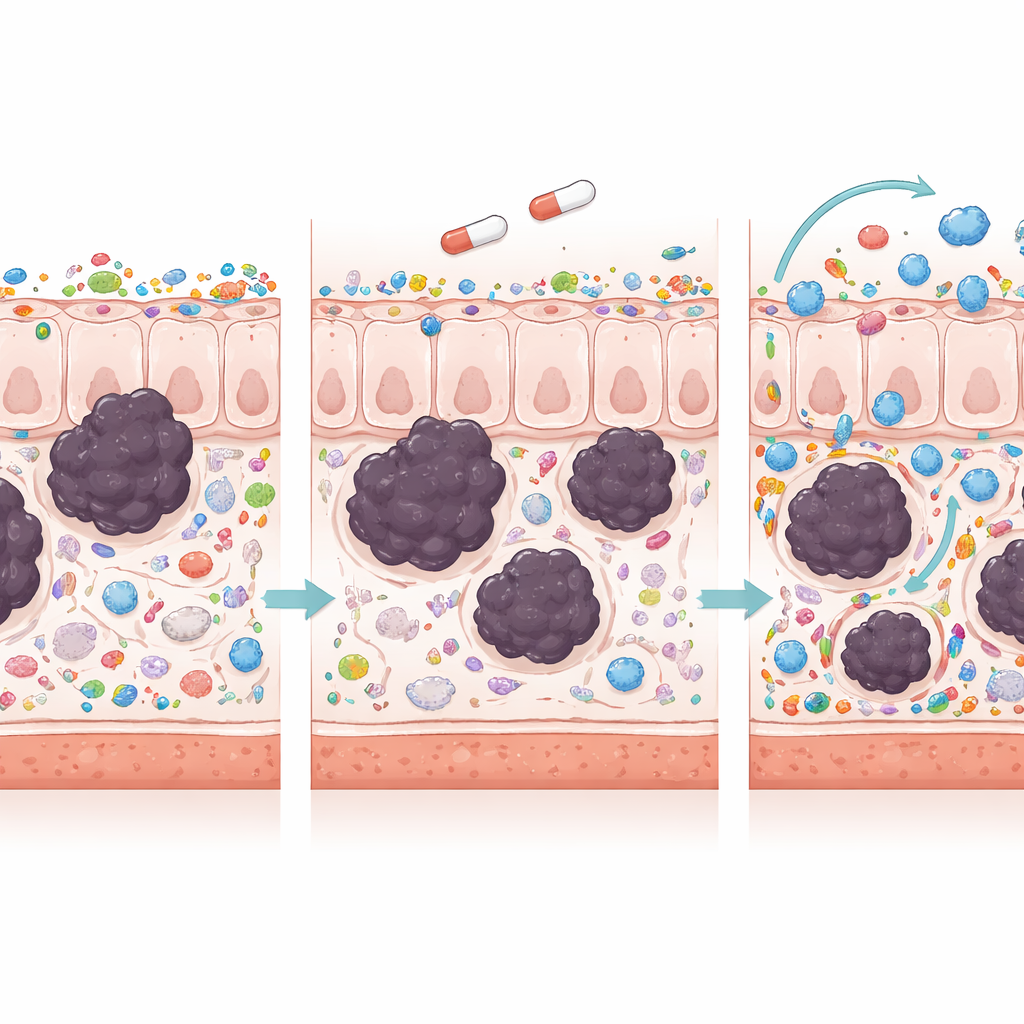
Eftersom immunsystemet ständigt övervakar tarmen efter avvikande celler undersökte teamet hur immuncellerna beter sig i de olika grupperna. Hos obehandlade tumörbärande möss var tarmväggen fylld av en blandning av immunceller som speglade en kronisk, oordnad strid. Vissa celltyper som kan döda cancerceller direkt, såsom vissa T‑celler och neutrofiler, var faktiskt minskade. Capecitabin, som väntat för kemoterapi, minskade i allmänhet infiltrationen av immunceller, vilket kan hjälpa mot cancer men också försvagar försvaret. När FMT lades till förändrades bilden: det skedde en selektiv ökning av cancerbekämpande celler, inklusive hjälpar‑ och cytotoxiska T‑celler, natural killer‑celler och neutrofiler, samtidigt som celler och makrofager förknippade med suppression och tumörstöd minskade. Detta mönster tyder på en mer fokuserad, effektiv attack mot tumörer snarare än ett kaotiskt inflammatoriskt tillstånd.
Tysta skadliga signaler, förstärka de hjälpsamma
Cancer och rubbade tarmmikrober översvämmar tarmmiljön med signalsubstanser kallade cytokiner, som antingen kan elda på sjukdom eller hjälpa till att kontrollera den. Hos de tumörbärande mössen var många inflammatoriska och tumörfrämjande signaler förhöjda, inklusive faktorer som driver blodkärlsbildning, blockerar celldöd eller hjälper tumörer att undgå immunangrepp via checkpoints såsom PD‑1 och PD‑L1. Capecitabin ensam dämpade många av dessa signaler men minskade också vissa nyttiga immunsignaler. Kombinationen av capecitabin och FMT gick längre: nyckeldrivande inflammatoriska faktorer sjönk mer markant, medan skyddande signaler såsom IL‑10 och interferon‑gamma ökade, och molekyler som styr immuncellers inriktning till tumörzonen ökade. Statistiska samband mellan specifika bakterier och specifika cytokiner antydde att vissa vänliga mikrober kan hjälpa till att omprogrammera immummiljön mot tumörkontroll.
Vad detta kan innebära för framtida behandling
Sammanfattningsvis visar studien att kombinationen av ett standardläkemedel mot tjocktarmscancer och en noggrant förberedd transplantation av hälsosamma tarmmikrober kan bromsa cancerprogression hos möss mer effektivt än kemoterapi ensam. Den dubbla strategin verkar på två fronter: den återställer ett mer balanserat tarmekosystem och omformar det lokala immunförsvaret så att anticancerceller och -signaler gynnas framför tumörfrämjande sådana. Även om dessa resultat är i djurstudier och FMT medför praktiska och säkerhetsmässiga överväganden, stöder de idén att framtida behandling av kolorektal cancer kan innefatta inte bara direkt riktade insatser mot tumörceller utan också omhändertagande av tarmens “inre trädgård” för att hjälpa kroppen att bekämpa sjukdomen.
Citering: Arshad, M., Zhang, CY., Gao, ZK. et al. Capecitabine combined with fecal microbiota transplantation prevents colorectal cancer progression through correction of microbial dysbiosis and immune regulation. Sci Rep 16, 13531 (2026). https://doi.org/10.1038/s41598-026-43626-1
Nyckelord: kolorektal cancer, tarmmikrobiom, fekal mikrobiotatransplantation, kemoterapi, immunrespons