Clear Sky Science · sv
Elimusertib förstärker cytotoxiska effekter av konventionell kemoterapi och ökar känsligheten för strålning i prekliniska modeller av Ewing-sarkom
Varför denna forskning är viktig för familjer
Ewing-sarkom är en ovanlig men aggressiv cancer som främst drabbar barn, tonåringar och unga vuxna. Även om modern behandling har förbättrat överlevnaden för patienter vars sjukdom inte har spridit sig, förblir prognosen dyster för dem med metastaser eller återfall, och den intensiva kemoterapin och strålningen kan ge allvarliga långsiktiga biverkningar. Denna studie undersöker om tillsats av en nyare typ av läkemedel, kallat elimusertib, kan göra befintliga behandlingar mer effektiva mot Ewing-sarkom samtidigt som det potentiellt möjliggör lägre doser av de hårda terapierna.
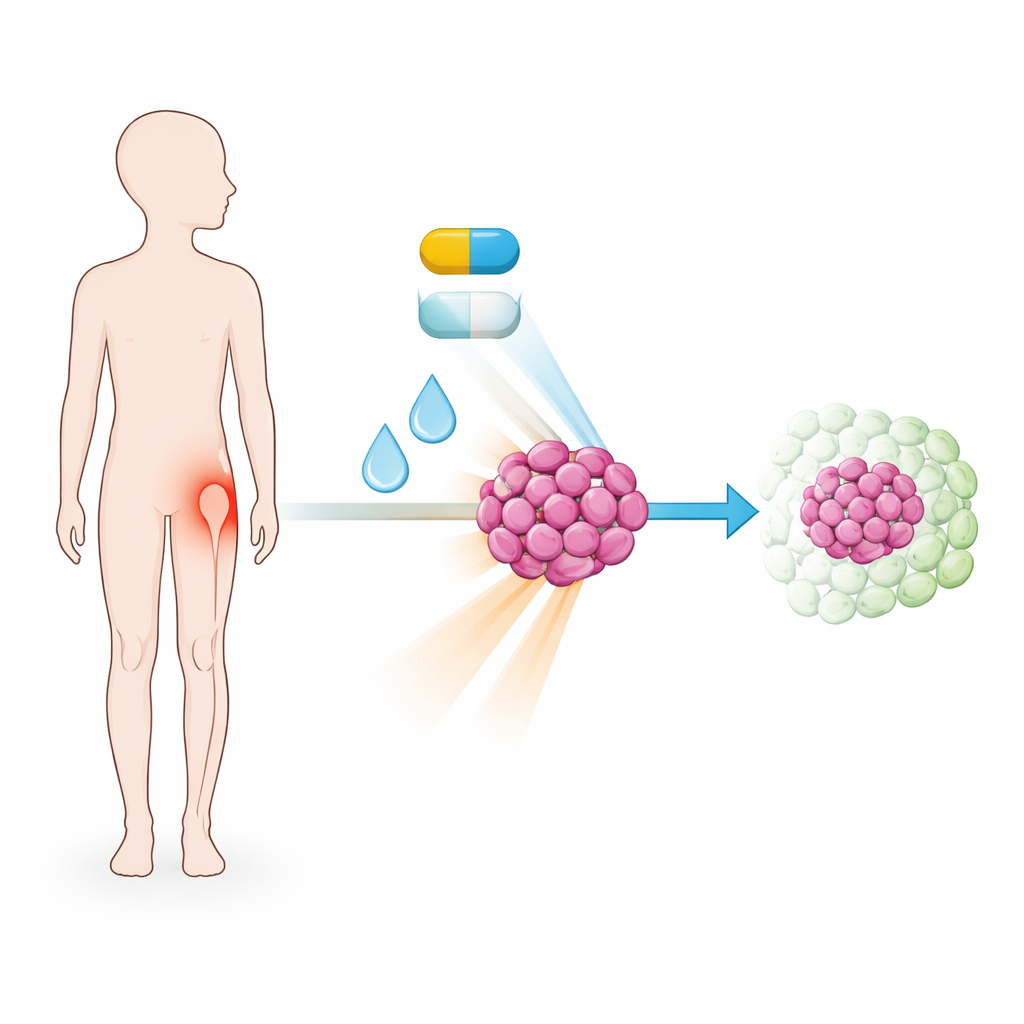
A ett svagt ställe i tumörens reparationssystem
Cancerceller växer snabbt och gör ofta misstag när de kopierar sitt DNA. Ewing-sarkomceller drivs av ett fusionsprotein som får dem att dela sig snabbt, vilket gör dem starkt beroende av ett internt nödsystem som upptäcker och reparerar DNA-stress. Elimusertib är utformat för att slå av en nyckelregulator i detta system, känd som ATR. Forskarna jämförde först elimusertib med flera andra experimentella läkemedel i flera Ewing-sarkomcellinjer. De fann att elimusertib var mest effektivt för att stoppa cancercellstillväxt, fungerade vid mycket låga koncentrationer, medan liknande icke-cancerceller var ungefär tio gånger mindre känsliga. Detta antydde att Ewing-sarkomceller har en särskild sårbarhet för ATR-blockad.
Test av läkemedlet i cellkulturer och små tumörer
För att se hur elimusertib påverkar cancerceller mer i detalj undersökte teamet om behandlade celler helt enkelt saktade ner eller faktiskt dog. Med hjälp av flödescytometri och proteintester visade de att elimusertib utlöste programmerad celldöd i flera Ewing-sarkomcellinjer. Läkemedlet ökade markörer för sena stadier av celldöd och aktiverade molekylära ”självdestruktions”-signaler inne i cellerna. Forskarna gick sedan vidare till en tredimensionell modell genom att odla tumörer på chorioallantoiska membranet i utvecklande hönsägg, en vanlig experimentell modell. När Ewing-sarkomceller förbehandlades med elimusertib före implantation bildades tumörer mindre ofta, och de tumörer som växte fram var betydligt mindre än de som bildades av obehandlade celler. Detta indikerade att ATR-hämning kan minska både cancercellernas förmåga att starta tumörer och storleken på tumörer som utvecklas.
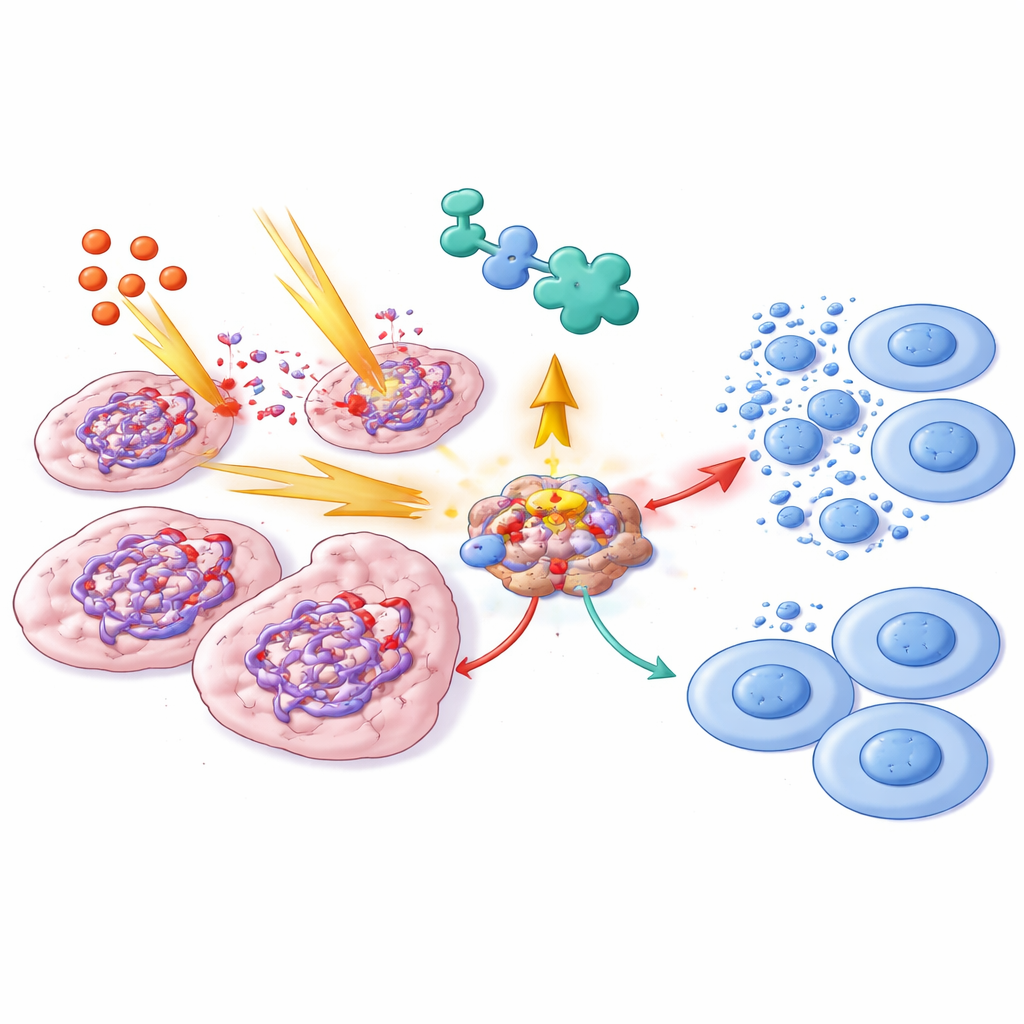
Samarbete med kemoterapi
Eftersom Ewing-sarkom vanligtvis behandlas med kombinationer av standardkemoterapier frågade forskarna nästa om elimusertib skulle krocka med eller komplettera befintliga regimer. De kombinerade ATR-hämmaren med fyra ofta använda läkemedel—ifosfamid, etoposid, doxorubicin och vincristin—över ett brett dosintervall. Med matematiska modeller som jämför effekterna av varje läkemedel ensamt och i kombination fann de tydlig synergi mellan elimusertib och både ifosfamid och etoposid, särskilt vid lägre doser. I dessa sammanhang dödade läkemedelsparen fler cancerceller än vad som skulle förväntas av att enbart lägga samman deras individuella effekter. Doxorubicin visade blandade resultat, med synergi i vissa cellinjer och additiva effekter i andra, medan vincristins påverkan mestadels var additiv. Endast några få kombinationer med höga doser visade mild antagonistisk effekt, och dessa uppstod där endera läkemedlet ensamt redan slog ut nästan alla celler.
Förstärkt effekt av strålning
Strålbehandling är ett viktigt verktyg för att kontrollera Ewing-sarkom men begränsas av skador på frisk vävnad, särskilt hos unga som kan drabbas av sena effekter och sekundära cancerformer under sin livstid. Eftersom strålning orsakar DNA-skador som normalt aktiverar ATR testade teamet om elimusertib kunde fungera som en radiosensitiserare—göra cancerceller mer sårbara för lägre doser strålning. I celldödassays gav kombinationen av elimusertib och röntgenexponering långt fler döende celler än någon av behandlingarna ensam, och effekten ökade med stigande stråldos. På molekylär nivå dämpade läkemedlet aktiveringen av ett nedströms kontrollproteinet som normalt hjälper celler att pausa och reparera sitt DNA. I långsiktiga koloni-bildningstester var en måttlig stråldos ihop med elimusertib mer effektiv än en mycket högre stråldos ensam och minskade skarpt antalet överlevande cancercellskluster.
Vad detta kan innebära för framtida behandling
Sammantaget visar dessa prekliniska experiment att elimusertib ensam kan bromsa och krympa Ewing-sarkommodeller och att det kraftigt förstärker effekterna av både DNA‑skadande kemoterapi och strålning. Genom att inaktivera en reparationsväg som Ewing-sarkomceller starkt förlitar sig på, tycks läkemedlet förvandla standardbehandlingar till ett mer avgörande slag mot tumören. Även om dessa studier gjordes i celler och experimentella tumörmodeller—inte ännu på patienter—stöder resultaten att utvärdera ATR-hämmare som elimusertib i kliniska studier för Ewing-sarkom. Om liknande fördelar ses hos människor kan detta tillåta läkare att använda lägre doser av toxiska terapier samtidigt som chansen till långsiktig kontroll förbättras, vilket ger nytt hopp för barn och unga vuxna som står inför denna svåra cancer.
Citering: Koch, L., Kerkhoff, M., Bretschneider, M. et al. Elimusertib enhances cytotoxic effects of conventional chemotherapy and sensitizes to radiation in preclinical Ewing sarcoma models. Sci Rep 16, 10953 (2026). https://doi.org/10.1038/s41598-026-41751-5
Nyckelord: Ewing-sarkom, ATR-hämmare, elimusertib, kemoradioterapi, DNA-skadereparation