Clear Sky Science · sv
Bedömning av antitumöreffekter av plasmaaktiverad fosfatbuffrad saltlösning i 2D- och 3D-modeller av bröstcancerceller
Nya sätt att ta sig an svåra brösttumörer
Många kvinnor med bröstcancer har nytta av dagens läkemedel, men vissa tumörer är antingen resistenta från början eller lär sig att försvara sig över tiden. Den här studien undersöker en ovanlig, elektricitetsbaserad metod som förvandlar en enkel saltlösning till en potentiellt cancerbekämpande vätska. Arbetet visar hur denna "plasmaaktiverade" saltlösning skadar både vanliga och läkemedelsresistenta bröstcancerceller odlade i laboratoriet, vilket väcker möjligheten till ett nytt alternativ för patienter vars tumörer inte längre svarar på standardkemoterapi.
Att göra enkel saltlösning till en aktiv behandling
Forskarnas utgångspunkt var fosfatbuffrad saltlösning, en enkel, kroppsvänlig saltlösning som ofta används i biologiska laboratorier. De utsatte vätskan för ett kallt elektriskt urladdning, en typ av icke-termisk plasma som varken värmer eller bränner. Denna process fyllde lösningen med reaktiva syre- och kvävespecies—högenergetiska former av syre och kväve som kan skada celler. Ju längre vätskan exponerades för plasma, desto mer av dessa reaktiva molekyler byggdes upp, och deras nivåer förblev i stort sett stabila i minst en dag vid kroppstemperatur, vilket tyder på att en sådan vätska skulle kunna förberedas i förväg för medicinskt bruk. 
Testning på platta cellager och mini‑tumörer
För att se om denna aktiverade vätska kunde skada cancer testade teamet den på två nära besläktade humana bröstcancercellinje: en som är känslig för cytostatikumet paklitaxel (MCF‑7) och en systerlinje som gjorts starkt resistent mot det (MCF‑7/PAX). I vanliga platta (2D) kulturer minskade en en timmes exponering för plasmabehandlad saltlösning kraftigt cellöverlevnaden i båda linjerna på ett dosberoende sätt—ju intensivare plasmabehandlingen av vätskan var, desto färre celler fanns kvar efter tre dagar. Under mikroskopet förlorade behandlade celler sin normala form och sitt fäste på skålen och visade klassiska tecken på programmerad celldöd snarare än plötslig upplösning.
Hur vätskan driver cancerceller mot död
Flödescytometrimätningar—en metod som räknar och kategoriserar enskilda celler—bekräftade att huvud effekten av den plasmaaktiverade saltlösningen var att utlösa apoptos, en kontrollerad form av celldöd. När plasmabearbetningstiden för vätskan ökade sjönk andelen levande celler medan andelen tidigt och sent apoptotiska celler steg, i både den läkemedelskänsliga och den läkemedelsresistenta linjen. Viktigt är att vanlig, obehandlad saltlösning inte visade denna effekt, vilket pekar på de reaktiva molekyler som bildas av plasman som den verkliga orsaken. Tidigare arbete med liknande vätskor har visat att kombinationer av väteperoxid och kvävebaserade arter verkar tillsammans för att driva cancerceller bortom deras redan stressade gränser, medan friska celler tål dessa nivåer bättre.
Angrepp på 3D tumörliknande sferoider
Eftersom verkliga tumörer är tredimensionella formade forskarna också kompakta klot av cancerceller kallade sferoider, som bättre efterliknar tumörers struktur och beteende i kroppen. Dessa sferoider exponerades för plasmabehandlad saltlösning antingen i en timme eller tjugofyra timmar. I både läkemedelskänsliga och läkemedelsresistenta sferoider ledde högre plasmadoser till antingen tillväxthämning eller synlig krympning under de följande sex dagarna. Sferoider behandlade med den starkaste dosen blev mindre, mindre kompakta och omgivna av cellulärt skräp, tecken på allvarlig skada. Noterbart var att de läkemedelsresistenta sferoiderna ofta påverkades ännu mer än de känsliga, där mycket höga doser ledde till en nästan fullständig förlust av viabilitet. 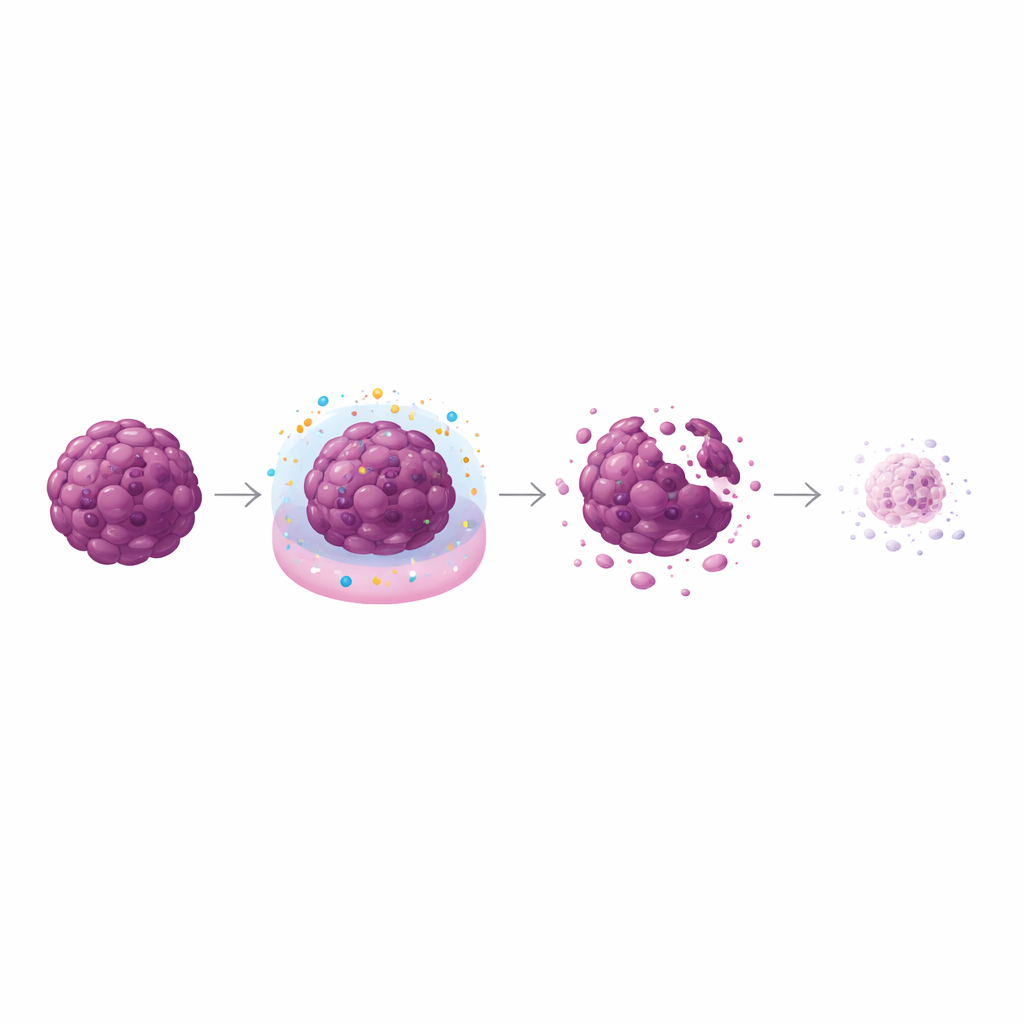
Vad detta kan innebära för framtida cancerbehandling
Samlade tyder fynden på att plasmaaktiverad saltlösning kan döda bröstcancerceller odlade både i enkla lager och i mer realistiska 3D mini‑tumörer, och kan göra det även när dessa celler har blivit resistenta mot ett stort cytostatikum. Eftersom de aktiva molekylerna i vätskan är stabila i många timmar och baslösningen i sig är enkel och säker, skulle en sådan behandling en dag kunna ges genom direkt injektion i tumörer eller användas tillsammans med befintliga läkemedel. Även om detta fortfarande är laboratoriebaserade experiment och mycket arbete återstår innan någon patientanvändning, pekar studien mot en lovande framtid där en noggrant energiserad saltlösning hjälper till att oskadliggöra några av de mest seglivade bröstcancerformerna.
Citering: Kužmová, D., Gbelcová, H. & Machala, Z. Assessing antitumor effects of plasma-activated phosphate buffered saline in breast cancer cell 2D and 3D models. Sci Rep 16, 13299 (2026). https://doi.org/10.1038/s41598-026-41704-y
Nyckelord: bröstcancer, kall plasma, läkemedelsresistens, plasmaaktiverad saltlösning, 3D tumörmodeller