Clear Sky Science · sv
Bedömning av lipidmediatorer i urinen hos patienter med borrelia, fästingburen encefalit och human granulocytär anaplasmos
Varför urin kan avslöja dolda fästinginfektioner
Fästingbett avfärdas ofta som en mindre olägenhet, men de smittoämnen som fästingar bär på kan tyst utlösa allvarliga hjärn- och nervproblem. Att ställa diagnos tidigt är svårt eftersom symtomen är ospecifika och blod- eller likvorprover är invasiva och långsamma. Denna studie undersöker en enkel men kraftfull idé: kan vanlig urin, rik på kemiska spår från hela kroppen, avslöja typiska ”röksignaler” från fästingburna infektioner och hjälpa läkare att skilja olika sjukdomar åt?
Fästingbett och svårtolkade sjukdomar
Fästingar kan överföra flera patogener samtidigt, inklusive borreliabakterien Borrelia burgdorferi, fästingburen encefalit (TBE)-virus och bakterien som orsakar human granulocytär anaplasmos (HGA). Dessa infektioner börjar ofta med influensaliknande symtom, trötthet eller ett utslag som lätt kan förbises, vilket försvårar att fastställa orsaken. Om borrelia inte behandlas kan den sprida sig från ett hudutslag som kallas erythema migrans (EM) till nervsystemet och orsaka neuroborrelios (NB). TBE kan utvecklas från mild feber till hjärninflammation. Eftersom dessa tillstånd överlappar i symtom och kan förekomma samtidigt hos en patient behöver kliniker bättre verktyg för att reda ut vilken infektion som föreligger och hur kroppen reagerar.
Fetter, stress och kemiska budbärare
När patogener invaderar ökar kroppens försvar produktionen av mycket reaktiva molekyler kallade reaktiva syreföreningar. I måttlig mängd hjälper de till att bekämpa infektion; i överskott skadar de cellkomponenter, särskilt membranfetter. Denna process, känd som oxidativ stress, klyver långkedjiga fetter till mindre, reaktiva fragment och aktiverar även enzymer som ombygger membranlipider. Resultatet blir ett utflöde av fettsyra-budbärare, inklusive endokannabinoider och eikosanoider, som styr inflammation och immunitet. Eftersom dessa molekyler och deras nedbrytningsprodukter så småningom filtreras av njurarna kan förändringar i deras nivåer upptäckas i urin, vilket ger en icke-invasiv ögonblicksbild av vad som händer i vävnader som hjärna, hud och blod.
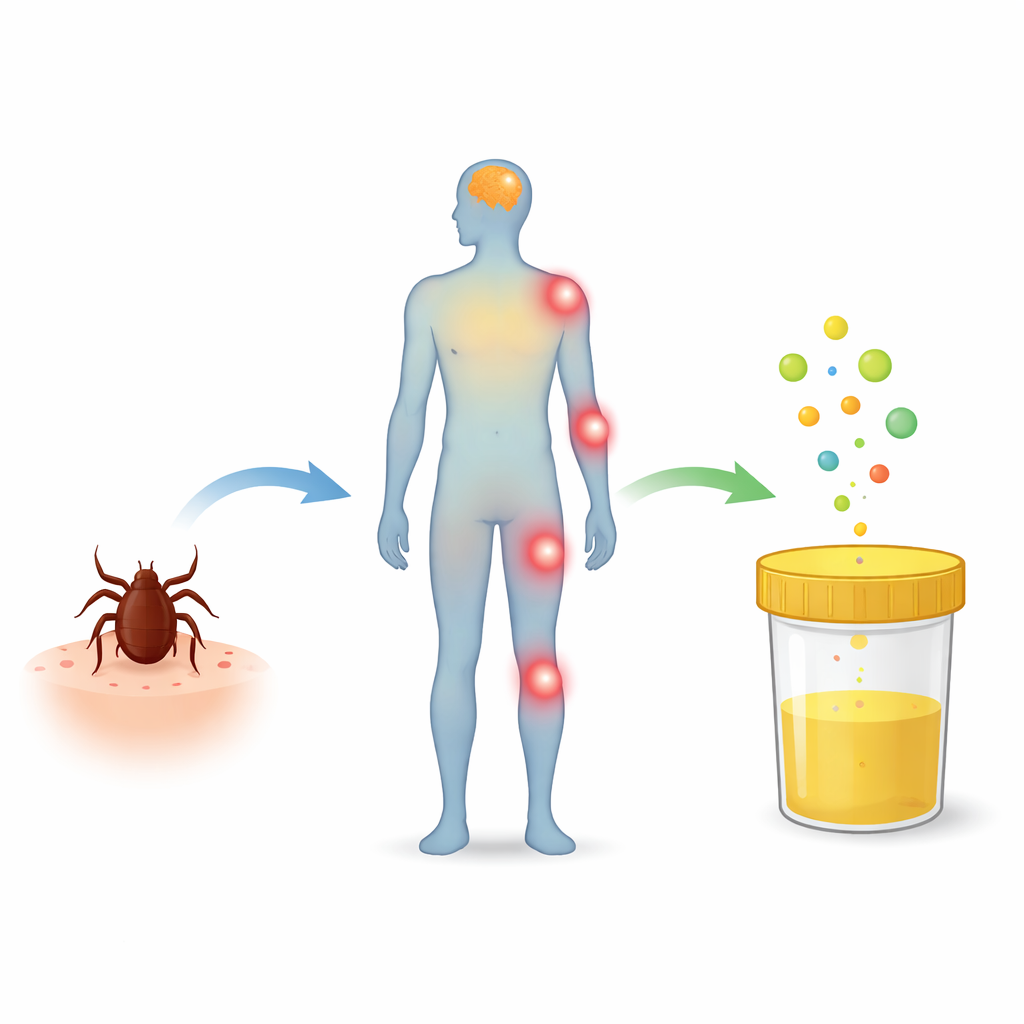
Hur studien genomfördes
Forskarnas samlade urinprover från vuxna med flera bekräftade fästingburna tillstånd: tidig borrelia med EM, neuroborrelios, TBE, HGA och koinfektion med TBE och borrelia, samt från friska frivilliga. Prover togs före behandling och igen efter terapi. Med hjälp av mycket känslig masspektrometri mätte man markörer för fettskada (såsom 8-isoprostanderivat och 4-hydroxi-2-nonenal) och ett panel av lipidmediatorer: endokannabinoider som oleoylethanolamid (OEA) och palmitoylethanolamid (PEA), samt eikosanoider såsom prostaglandiner, leukotriener och hydroxyeikosatetraensyror (HETEs). Därefter sökte man efter konsekventa skillnader mellan patientgrupper och friska kontroller, samt om behandling förändrade dessa kemiska profiler.
Distinkta kemiska fingeravtryck i urinen
Före behandling visade patienter med tidig borrelia, neuroborrelios eller TBE alla högre urinnivåer av 8-isoprostaner än friska personer, vilket signalerar ökad oxidativ stress och fettoxidation. Bland endokannabinoiderna utmärkte sig OEA: dess nivå var signifikant högre hos TBE-patienter än hos friska kontroller, vilket tyder på att kroppen kan förstärka antiinflammatoriska och antioxidantiska försvar i denna virala hjärninfektion. För eikosanoiderna såg teamet en ökning av den proinflammatoriska prostaglandinen PGE2 hos TBE-patienter och skiftningar i andra mediatorer såsom leukotrien LTD4 och 5-HETE mellan olika borreliarelaterade grupper, samt förändringar i antiinflammatoriska molekyler som PGD2 och 15-HETE. Dessa mönster antyder att varje infektion – och till och med olika stadier av borrelia – lämnar ett subtilt annorlunda ”lipidsignatur” i urinen.
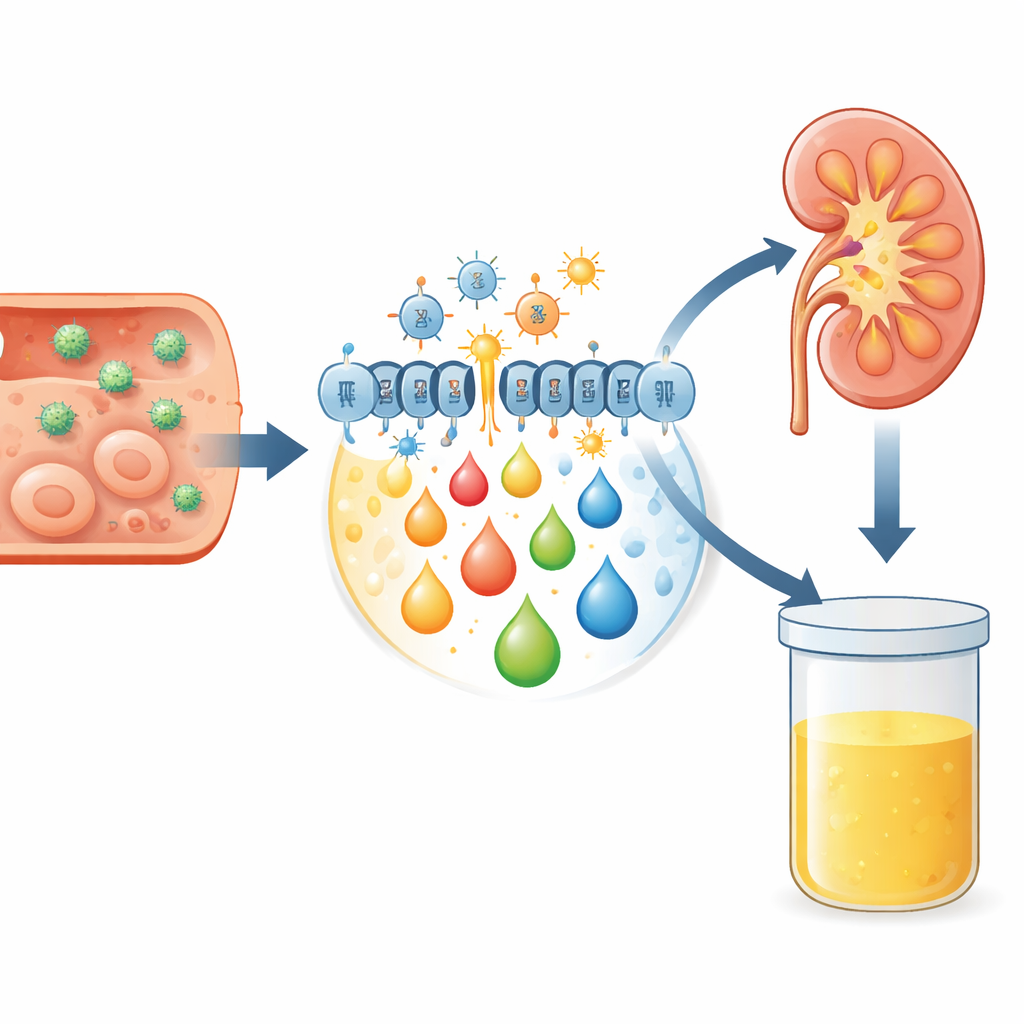
Vad mönstren visar – och inte visar
Intressant nog förändrades inte de övergripande profilerna av dessa lipidmediatorer i ett statistiskt tydligt avseende när samma patienter testades igen efter behandling, varken jämfört med deras egna nivåer före behandling eller mellan sjukdomsgrupper. Den stabiliteten kan återspegla det lilla antalet deltagare, särskilt för HGA, eller kvarstående metabola förändringar som överstiger symtomens varaktighet. Det understryker också att dessa molekyler ingår i komplexa, överlappande vägar som svarar inte bara på själva patogenen utan också på kroppens försök att begränsa skada och återställa balans. Ändå stöder den konsekventa förhöjningen av specifika markörer som 8-isoprostaner och OEA i vissa infektioner deras roll som indikatorer på oxidativ stress och immunaktivering.
Varför detta är viktigt för patienter
För personer med svårtolkade fästingburna symtom ger denna forskning en inblick i en framtid där ett enkelt urinprov skulle kunna hjälpa till att skilja mellan borrelia, TBE, anaplasmos eller koinfektioner, och kanske även indikera sjukdomsstadium eller svårighetsgrad. Studien visar att fästingburna infektioner rubbar fettmetabolismen på sätt som kan upptäckas utanför kroppen, utan nålar eller lumbalpunktion. Samtidigt betonar författarna att deras patientgrupp var liten och att behandlingarna varierade, så dessa resultat är ett lovande första steg snarare än ett färdigt diagnostiskt verktyg. Större studier behövs för att bekräfta om urinens lipidmediatorer på ett tillförlitligt sätt kan vägleda diagnos och uppföljning, men arbetet lyfter fram urinen som ett överraskande informativt fönster in i hur kroppen försvarar sig mot fästingburna hot.
Citering: Biernacki, M., Skrzydlewska, E., Dobrzyńska, M. et al. Assessment of lipid mediators in the urine of patients with Lyme disease, tick-borne encephalitis and human granulocytic anaplasmosis. Sci Rep 16, 11418 (2026). https://doi.org/10.1038/s41598-026-40464-z
Nyckelord: fästingburna sjukdomar, borrelia, fästingburen encefalit, lipidmediatorer, oxidativ stress