Clear Sky Science · sv
Strukturella insikter i hur bitter smak från kaffe uppfattas av receptorn TAS2R43
Varför ditt morgonkaffe smakar bittert
Många uppskattar kaffets rika bitterhet, men den skarpa tonen i varje klunk är också kroppens tidiga varningssystem mot gifter. Denna studie avslöjar, atom för atom, hur en specifik smakreceptor i munnen, kallad TAS2R43, upptäcker bittra kemikalier från kaffe och från ett kraftfullt växttoxin. Genom att visualisera receptorn i en aldrig tidigare skådad detalj visar forskarna hur bitterhet omvandlas till en elektrisk signal till hjärnan och antyder sätt att finjustera besk smak i livsmedel — och till och med utnyttja dessa receptorer för nya läkemedel.
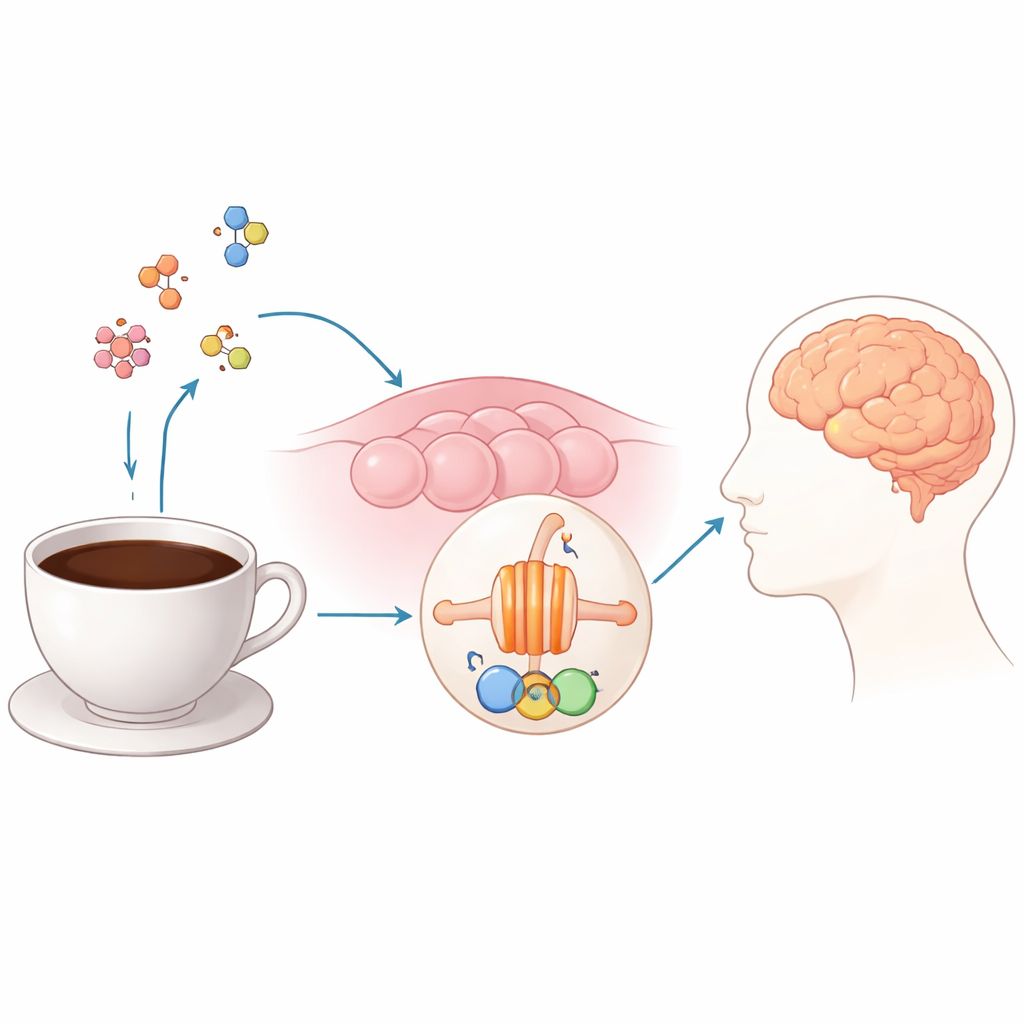
Kroppens bittra alarmsystem
Människor känner fem grundsmaker: söt, sur, salt, umami och bitter. Medan sötma och umami uppmuntrar oss att äta socker och proteiner fungerar bittert mer som en inbyggd varningsskylt som hjälper oss att undvika ruttnande eller giftiga ämnen. Bitter smak detekteras inte av enkla porer eller kanaler, utan av en familj specialiserade receptorer på smakcellerna, kända som TAS2R. En medlem i denna familj, TAS2R43, är särskilt viktig för att känna igen bittra föreningar i kaffe, inklusive koffein och flera mindre kända molekyler som bildas vid rostning. Intressant nog finns TAS2R43 även utanför tungan — i tarmen, luftvägarna och andra vävnader — där dess aktivering har kopplats till hormonfrisättning, avslappning av luftvägar, immunsvar och ämnesomsättning.
Fånga receptorn i arbete
För att se exakt hur TAS2R43 fungerar använde författarna kryoelektronmikroskopi, en teknik som avbildar snabbfrysta proteiner i nästan atomupplösning. De fångade den mänskliga TAS2R43-receptorn i ett aktivt tillstånd med hjälp av aristolochinsyra I, ett mycket bittert växttoxin som binder receptorn extremt tätt, och kopplade den till två olika cellulära omkopplare, så kallade G-proteiner: ett typiskt för smakceller (gustducin) och ett som är vanligare på andra håll i kroppen (Gi). De resulterande strukturerna — tillräckligt skarpa för att följa individuella sidokedjor — visade att aristolochinsyran lägger sig i en djup ficka i den yttre halvan av receptorn, en plats som delas med andra bittra receptorer men formad på ett sätt som ger TAS2R43 dess egna kemiska preferenser.
Hur bittra molekyler passar och växlar omkopplaren
Inuti denna ficka omfamnas toxinet av en ringformad aminosyra som staplar mot dess aromatiska ringar och av flera närliggande fettliknande rester som kragar det från sidorna. En positivt laddad rest sträcker sig in som ett fingertopp för att greppa toxinets negativt laddade grupper, medan en liten vattenklump bildar en brygga mellan toxinet och receptorn och stabiliserar inpassningen. När forskarna förändrade dessa nyckelrester en efter en i mänskliga celler föll receptorernas förmåga att reagera på toxinet kraftigt, vilket bekräftar deras betydelse. De visade också att kaffeföreningar som koffein, cafestol och kahweol kan aktivera TAS2R43, även om de generellt är mindre potenta än toxinet; vissa rostade kaffemolekyler utlöste till och med starkare signalering genom det smakkopplade G-proteinet än aristolochinsyra själv.
Från bindningsficka till hjärnsignal
Strukturerna visar vidare hur TAS2R43 förmedlar budskapet inåt. På receptorernas inre yta bildar en klunga helixar en dockningsgrop för G-proteinet. När den bittra molekylen binder utanför omorganiserar denna inre yta sig, vilket tillåter G-proteins spets att skjuta djupt in i receptorn. Specifika laddade rester i TAS2R43 griper tag i motsvarande sura fläckar på G-proteinet, medan en liten vattenmolekyl hjälper till att limma ihop de två. Mutationer i några av dessa kontaktpunkter störde signaleringen utan att påverka receptorernas nivåer på cellens yta — tydliga bevis på att detta är de mekaniska leder som förvandlar ett kemiskt möte på tungan till en efterföljande signal som hjärnan tolkar som bitterhet.
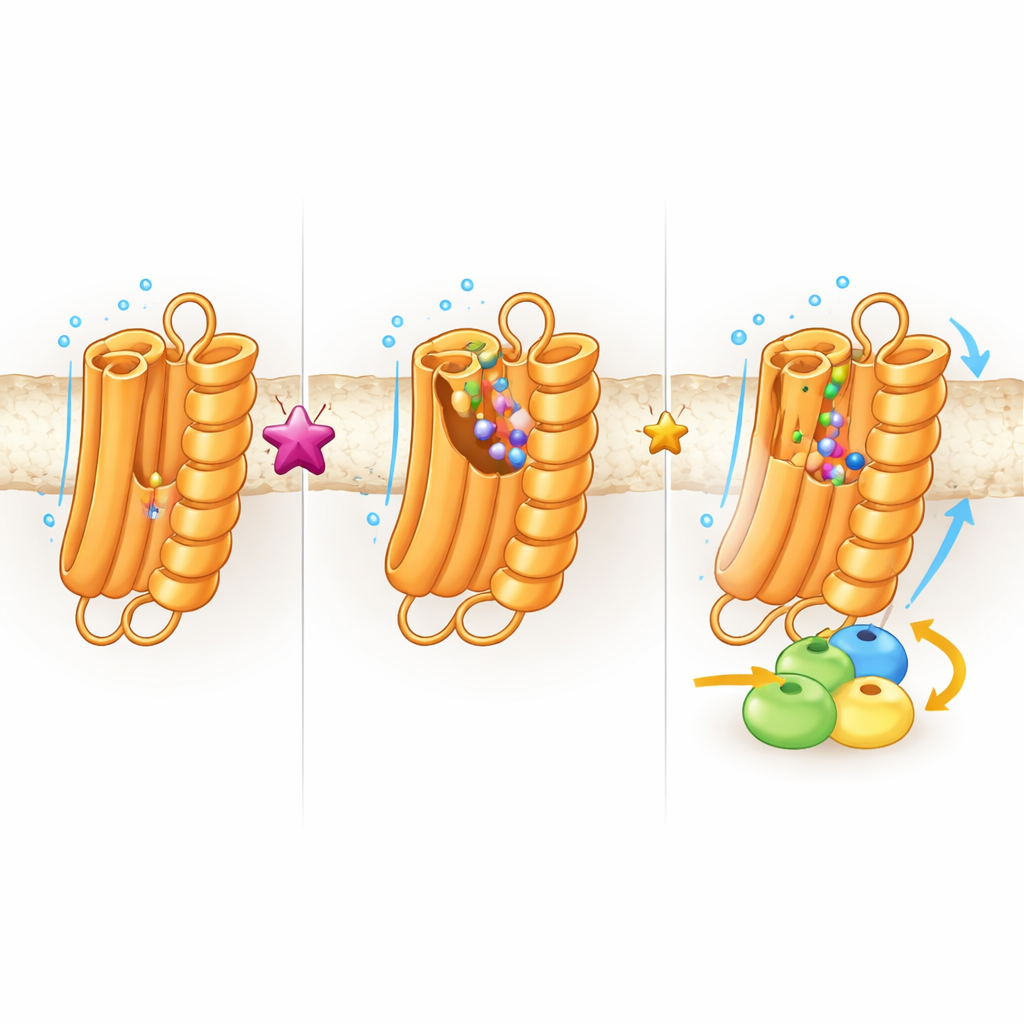
Dolda fickor och framtida möjligheter
För att utforska hur flexibel TAS2R43 är körde teamet långa datorsimuleringar av receptorn som rörde sig i ett virtuellt membran, med och utan bundet toxin. Dessa filmer visade att när ingen ligand är närvarande öppnar sig delar av receptorn och skapar tillfälliga inre håligheter och förstorar huvudfickan; när toxinet binder låser det strukturen i ett mer stängt, stabilt tillstånd. Sådana formskiftande "kryptiska fickor" kan göra det möjligt för TAS2R43 att känna igen ett brett spektrum bittra kemikalier — eller erbjuda nya fästen för läkemedel som skruvar upp eller ner dess aktivitet. Receptorn visade också tecken på att vara något aktiv även utan någon ligand, vilket kan förklara varför den så lätt samarbetar med G-proteiner i celler.
Vad detta betyder för smak och hälsa
Enkelt uttryckt förklarar detta arbete hur en av tungans bittra detektorer greppar både kaffekomponenter och ett farligt växttoxin, och hur den händelsen drar i en intern spak som i slutändan resulterar i upplevelsen av bitterhet. Genom att kartlägga den exakta formen av TAS2R43:s huvudficka och dess dolda kavitetter lägger studien en ritning för att designa molekyler som mildrar eller blockerar bitterhet i mat och dryck eller, omvänt, selektivt aktiverar dessa receptorer i tarm eller lungor för terapeutisk nytta. Din dagliga kopp kaffe är alltså också ett fönster mot ett finjusterat molekylärt alarmsystem som skyddar kroppen samtidigt som det formar din smakupplevelse.
Citering: Kim, Y., Gumpper, R.H., Zhuang, Y. et al. Structural insights into coffee bitter taste perception by TAS2R43 receptor. Nat Struct Mol Biol 33, 701–710 (2026). https://doi.org/10.1038/s41594-026-01776-w
Nyckelord: bitter smak, kaffe, smakreceptorer, G-proteinsignalering, kryoelektronmikroskopi