Clear Sky Science · sv
Clathrin-associerade SCYL2 bidrar till aktivering av PI3K/AKT-signalering och tumörbildning genom PTEN-fosforylering vid vuxen T-cellsleukemi/lymfom
Varför detta betyder något för cancer och immunitet
Vuxen T-cellsleukemi/lymfom (ATL) är en aggressiv blodcancer orsakad av infektion med humant T-cellsleukemivirus typ 1. Många ATL-celler behåller ett viktigt tumörsuppressorenzym kallat PTEN, men har stängt av det så att kraftfulla tillväxtsignaler får löpa fritt. Denna studie avslöjar ett tidigare okänt sätt som cancerceller använder små membranblåsor inne i cellen som signalnav för att inaktivera PTEN, öka en huvudväg för tillväxt och hålla leukemiceller vid liv — och pekar på ett omräknat psykiatriskt läkemedel som en potentiell metod för att avbryta denna process.
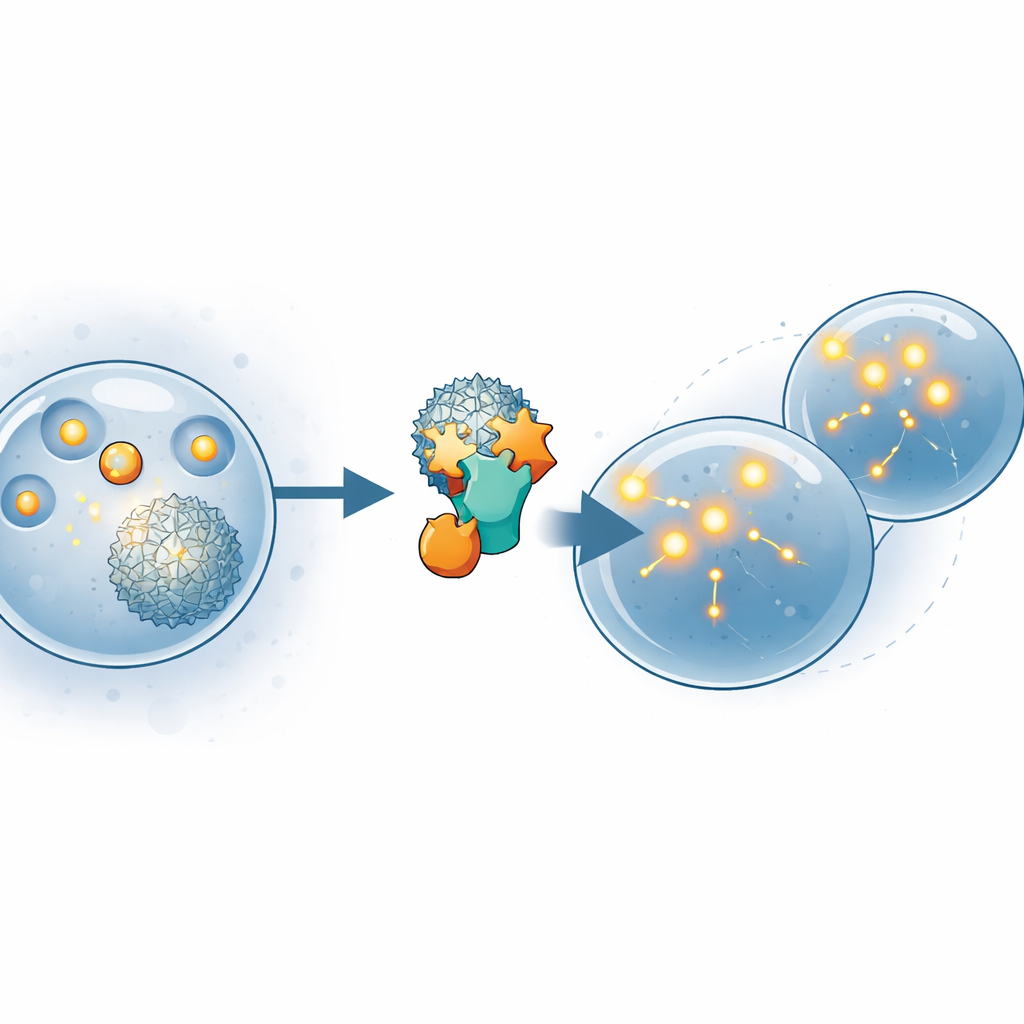
En cellulär broms som cancer lär sig kringgå
PTEN fungerar normalt som en molekylär broms för celltillväxt. Den tar bort en kemisk märkning från ett fettliknande molekyl i cellmembranet och stänger därigenom ner PI3K/AKT-vägen — en signalkedja som främjar cellsurvival, tillväxt och rörelse. Många tumörer förlorar inte PTEN helt; i stället modifierar de det kemiskt så att det inte längre fungerar korrekt. I ATL och flera solida tumörer är tre lägen nära PTEN:s svansända ofta dekorerade med fosfatgrupper, vilket låser PTEN i en mindre aktiv form. Författarna ville ta reda på vilka cellulära partners som är ansvariga för denna specifika modifiering i ATL, med antagandet att dessa partners kan bli nya läkemedelsmål.
En dold hjälpare som binder PTEN
Med hjälp av leukemiceller från en ATL-cellinje fiskade forskarna upp proteiner som fysiskt hakar fast vid PTEN och identifierade ett protein kallat SCYL2 som en stark kandidat. SCYL2 innehåller en domän som liknar ett proteinkinas och är känt för att associera med klatrin, ett skelettprotein som formar små, belagda vesiklar som används för transport av last inne i celler. Teamet bekräftade att SCYL2 och PTEN finns tillsammans på samma platser i ATL-celler — huvudsakligen i cytoplasman nära kärnan — och att SCYL2-nivåerna är mycket högre i primära ATL-celler och virusinfekterade cellinjer än i friska T-celler. Förhöjda nivåer av SCYL2 korrelerade med högre fosforylering av PTEN:s svans och aktivering av AKT, vilket tyder på att SCYL2 hjälper till att tysta PTEN och stärka tillväxtsignaleringen i leukemiceller.
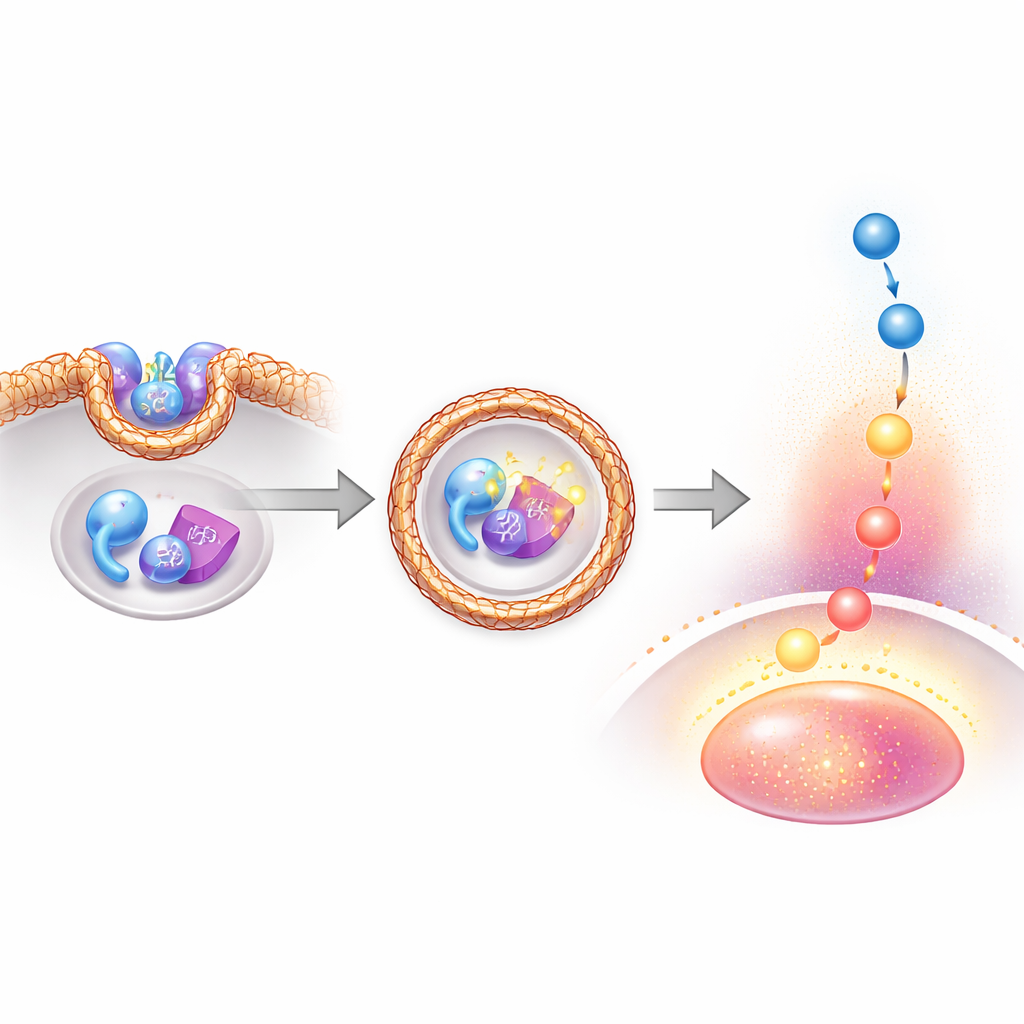
Vesiklar som rörliga plattformar för tillväxtsignaler
För att förstå hur SCYL2 påverkar PTEN undersökte författarna vilka delar av respektive protein som interagerar och vilka andra partners som ansluter till komplexet. De fann att den främre "kinasliknande" regionen av SCYL2 binder till PTEN:s svansregion, medan en annan region av SCYL2 associerar med klatrin tung kedja, huvudbyggstenen i klatrinbelagda vesiklar. När SCYL2 och klatrin var närvarande tillsammans blev PTEN kraftigt fosforylerat på sina kritiska svansställen och AKT-signalering ökade. Däremot ledde minskade nivåer av SCYL2 eller klatrin, eller blockering av vesikelformation, till minskad PTEN-fosforylering, återställd PTEN-enzymaktivitet och dämpad AKT. Avbildningsexperiment visade att SCYL2, klatrin, PTEN och endosommarkörer klustrar på samma vesiklar, vilket stöder idén att dessa belagda bubblor fungerar som rörliga plattformar där PTEN inaktiveras och tillväxtsignaler förstärks.
Att stänga av SCYL2 försvagar leukemiceller
Eftersom ATL-celler är beroende av detta vesikelbaserade signalnav testade teamet vad som händer när SCYL2 slås av. Short hairpin-RNA som sänkte SCYL2 i ATL-cellinjer ledde till mindre fosforylerat PTEN och AKT, starkare PTEN-aktivitet, minskad aktivering av NF-κB (en annan överlevnadsväg) och mer cancercellsdöd. Fibroblaster från möss som saknar SCYL2 visade likaledes svagare AKT-signalering och långsammare tillväxt. I en mus-xenograftmodell var tumörer härledda från SCYL2-depleterade ATL-celler mycket mindre än de från kontrollceller och visade minskad PTEN-svansfosforylering och AKT-aktivering, vilket understryker SCYL2:s roll i tumörtillväxt i levande djur.
Ett välbekant läkemedel som riktar in sig på cancervesiklar
Studien undersökte också om störning av själva vesiklarna kan vara terapeutiskt. Klorpromazin, ett antipsykotiskt läkemedel känt för att störa bildandet av klatrinbelagda vesiklar, minskade kraftigt överlevnaden hos ATL-cellinjer och många primära ATL-prover, men hade mindre effekt på närbesläktade T-cellsleukemilinjer. Behandlingen sänkte PTEN- och AKT-fosforylering, försvagade NF-κB-signalering och utlöste celldöd utan att ändra de övergripande nivåerna av SCYL2 eller klatrin. Blockering av PTEN:s enzymaktivitet återställde delvis effekten på AKT, vilket indikerar att frigörandet av PTEN från dess hämmande fosforylering är en nyckelkomponent i klorpromazins verkan i dessa celler.
Vad detta betyder för framtida cancerbehandlingar
Detta arbete visar att SCYL2, tillsammans med klatrinbelagda vesiklar, hjälper leukemiceller att stänga av PTEN vid specifika svansställen och därigenom eldar upp PI3K/AKT- och NF-κB-överlevnadsvägarna. Istället för att ta bort PTEN omvandlar ATL-celler normal trafikmachinery till ett signalnav som håller gasen nedtrampad. Genom att identifiera SCYL2 och klatrinassocierade vesiklar som centrala aktörer i denna process antyder studien att läkemedel riktade mot detta komplex — inklusive omplacerade medel som klorpromazin — skulle kunna återställa PTEN:s bromsfunktion och erbjuda en ny strategi för behandling av ATL och potentiellt andra cancerformer som förlitar sig på liknande PTEN-tystningsmekanismer.
Citering: Ichikawa, T., Shimosaki, S., Nakahata, S. et al. Clathrin-associated SCYL2 contributes to the activation of PI3K/AKT signaling and tumorigenesis through PTEN phosphorylation in adult T-cell leukemia/lymphoma. Cancer Gene Ther 33, 314–322 (2026). https://doi.org/10.1038/s41417-026-01008-9
Nyckelord: PTEN, PI3K AKT-vägen, vuxen T-cellsleukemi, klatrinbelagda vesiklar, SCYL2