Clear Sky Science · ru
Таргетирование дегацетилирования гистонов, регуляторов клеточного цикла и белков теплового шока как новые терапевтические стратегии при раке полового члена
Почему это исследование рака важно
Рак полового члена встречается редко, но при его распространении варианты лечения ограничены и часто радикально меняют качество жизни, иногда требуя частичного или полного удаления полового члена. Стандартная химиотерапия помогает только части пациентов, а у тех, кто не отвечает на лечение, долгосрочная выживаемость крайне низка. Это исследование подробно изучает белки и сигнальные пути, управляющие клетками рака полового члена, с целью выявить более мягкие и точные лекарственные подходы, которые могли бы сохранить больше тканей и улучшить исходы.
Внимательное изучение «механики» раковых клеток
Исследователи начали с выращивания нескольких клеточных линий непосредственно из опухолей пациентов и из опухолей, развившихся в мышах. Вместо того чтобы сосредотачиваться только на ДНК‑мутациях, они проанализировали полный набор белков внутри клеток, белки, секретируемые в окружение, и те же белки с химическими «вкл/выкл» метками. Такое широкое исследование выявило повторяющиеся темы: клетки опухоли были богаты белками, контролирующими упаковку ДНК (гистоны), белками, помогающими другим белкам правильно сворачиваться (белки теплового шока), и компонентами сигнальных путей роста, особенно связанными с образованием сосудов и реакцией на низкий уровень кислорода. Сравнение опухолевых клеток с нормальными фибробластами позволило выделить белковые паттерны, значительно более выраженные в раке, что указывает на уязвимые места для новых терапий.
Новые лекарственные мишени, скрытые на виду
Несколько групп белков оказались особенно перспективными. Во‑первых, ключевые компоненты системы упаковки и распаковки ДНК — белки, модифицирующие гистоны — были избыточно представлены, что подразумевает зависимость опухоли от изменённого эпигенетического ландшафта для поддержания активности генов роста. Во‑вторых, молекулы, стимулирующие прогрессию клеточного цикла, включая связанные с путём Wnt/β‑catenin и «мотор» CDK4/6, активно работали. В‑третьих, многочисленные белки теплового шока, особенно семейства HSP70 и HSP90, были обильны и часто фосфорилированы, что указывает на серьёзную зависимость раковых клеток от шаперонов сворачивания белков в условиях стресса. В совокупности эти данные наметили дорожную карту к трём основным классам лекарственных мишеней: гистоновым дегацетилазам (HDAC), регуляторам клеточного цикла CDK4/6 и шаперонам HSP90.
Испытание потенциальных препаратов
Чтобы проверить, можно ли эксплуатировать эти уязвимости, команда подвергла клетки рака полового члена панели из пятнадцати агентов, включая стандартные химиопрепараты и новые таргетные ингибиторы. Традиционные лекарства, такие как цисплатин и некоторые таксаны, работали, но зачастую только при более высоких дозах и с сильной вариабельностью между клеточными линиями. Напротив, несколько таргетных соединений последовательно оказывали сильный эффект при низких микромолярных концентрациях. Два ингибитора HDAC (ромидепсин и квизиностат), один ингибитор CDK4/6 (пальбоцикслиб) и два ингибитора HSP90 (17‑AAG и PU‑H71) значительно снижали жизнеспособность раковых клеток. Эти препараты вызывали арест клеток в фазе G2/M клеточного цикла и запускали программируемую клеточную гибель, преимущественно через внутренний, митохондриальный путь апоптоза. Важно, что нормальные фибробласты в целом были менее чувствительны, что намекает на терапевтическое окно, при котором опухолевые клетки можно поражать сильнее, чем здоровую ткань.
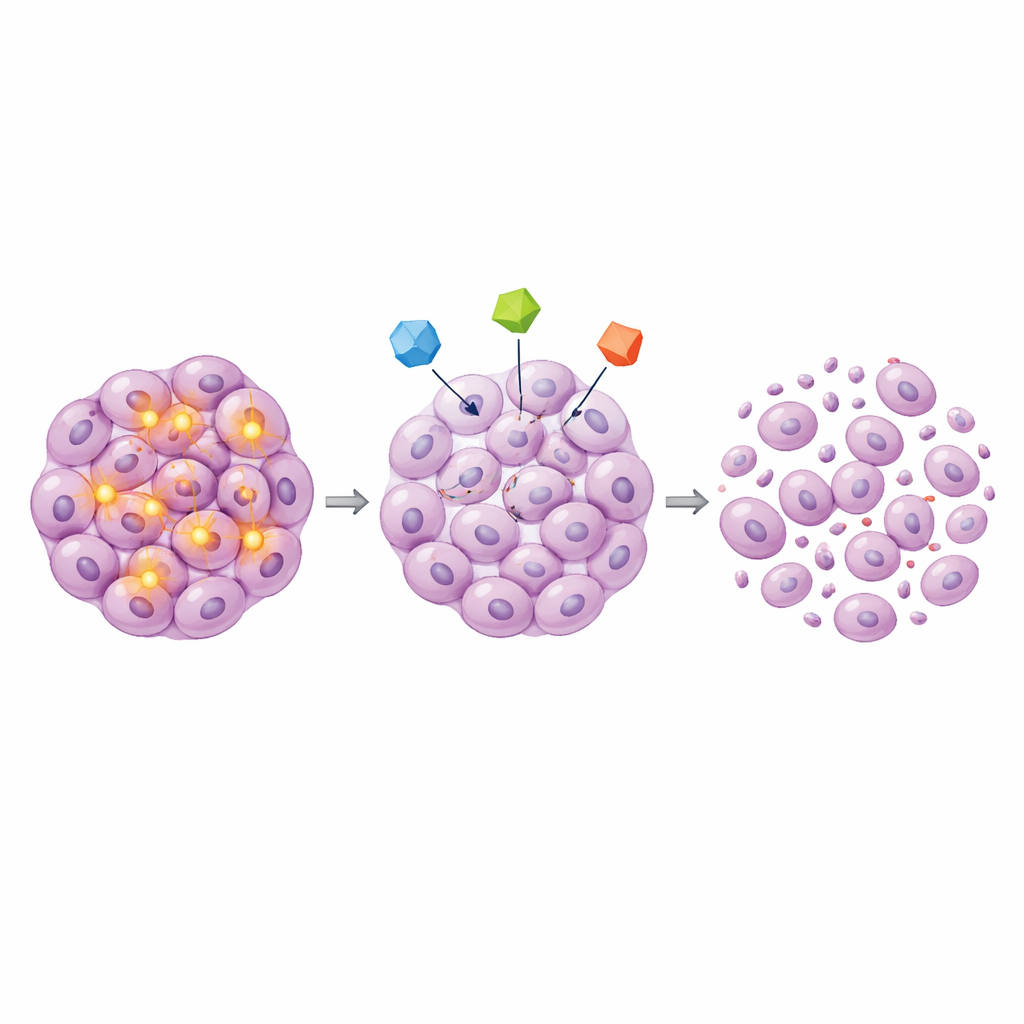
Сигналы стресса и гибели клеток внутри опухоли
Углублённый анализ показал, как лечение меняет активность генов, связанных со стресс‑ответом и апоптозом. Блокаторы HDAC усиливали набор генов, ранее связанных с остановкой роста в других урологических опухолях, и снижали про‑выживаемые сигналы, что согласуется с приведением раковых клеток в не жизнеспособное состояние. Ингибиторы HSP90 дестабилизировали известные онкоподдерживающие белки, включая MYC, одновременно парадоксально усиливая некоторые реакции теплового шока — ожидаемый побочный эффект при таргетировании этого пути. Пальбоциклиб, блокатор CDK4/6, снижал экспрессию генов, необходимых для точного деления хромосом и репарации ДНК, и повышал экспрессию генов, стимулирующих клеточную гибель. Во всех экспериментах усиленная фосфорилизация «стража» p53 и сильная активация сигнальных каскадов, связанных со стрессом, подкрепляли идею, что эти препараты выводят клетки рака полового члена за пределы их приспособительных возможностей.
Что это может означать для пациентов
Проще говоря, это исследование показывает, что клетки рака полового члена опираются на три уязвимые системы — упаковку ДНК, тайминг деления клеток и управление белковым стрессом — чтобы выживать. Блокирование дегацетилаз гистонов, CDK4/6 или HSP90 в лабораторных моделях останавливает деление этих клеток и подтолкивает их к самоуничтожению, часто более эффективно, чем некоторые текущие химиопрепараты, и с меньшим влиянием на нормальные клетки. Хотя результаты получены на клеточных моделях и моделях, полученных от мышей, а не в клинических испытаниях, они дают прочную научную основу для испытаний ингибиторов HDAC, CDK4/6 и HSP90 — по одиночке или в комбинации — в качестве более таргетных подходов для лечения мужчин с прогрессирующим раком полового члена.
Цитирование: Marson, L., Skowron, M.A., Pongratanakul, P. et al. Targeting histone deacetylation, cell cycle regulators and heat shock proteins as novel therapeutic strategies for penile cancers. npj Precis. Onc. 10, 140 (2026). https://doi.org/10.1038/s41698-026-01391-4
Ключевые слова: рак полового члена, таргетная терапия, эпигенетические препараты, ингибиторы клеточного цикла, белки теплового шока