Clear Sky Science · ru
Персонализированный анализ сигнальных путей при опухолях желудочно‑кишечного тракта для стратификации пациентов и оценки лекарственных мишеней на основе клинических кор‑биопсий
Почему это исследование важно для пациентов
Онкологи все чаще пытаются подбирать лечение в соответствии с уникальной биологией опухоли каждого пациента. Для злокачественных новообразований пищеварительной системы — например поджелудочной железы, толстой кишки, печени или желчных протоков — это особенно актуально: такие опухоли распространены, часто выявляются на поздних стадиях и трудно поддаются лечению. В исследовании изучают новый лабораторный метод, который позволяет считывать активность большого числа белков, связанных с раком, из крошечных образцов биопсии, с целью помочь врачам выбирать более точные терапии для отдельных пациентов.
От списков ДНК к живым сигналам
Сегодня большая часть «персонализированной» онкологической помощи опирается на анализ изменений в ДНК опухоли. Хотя это мощный инструмент, только по ДНК нельзя определить, какие сигналы внутри клетки фактически включены и стимулируют рост. Эти сигналы передаются белками, многие из которых можно непосредственно нацелить лекарствами. Исследователи использовали высокопроизводительный метод DigiWest — современный аналог классического вестерн‑блоттинга — чтобы одновременно измерить около 130–200 белков и их активированных форм. Важно, что для этого требуется примерно столько же материала, сколько дает одна пункционная биопсия, что делает метод применимым в реальной клинической практике.
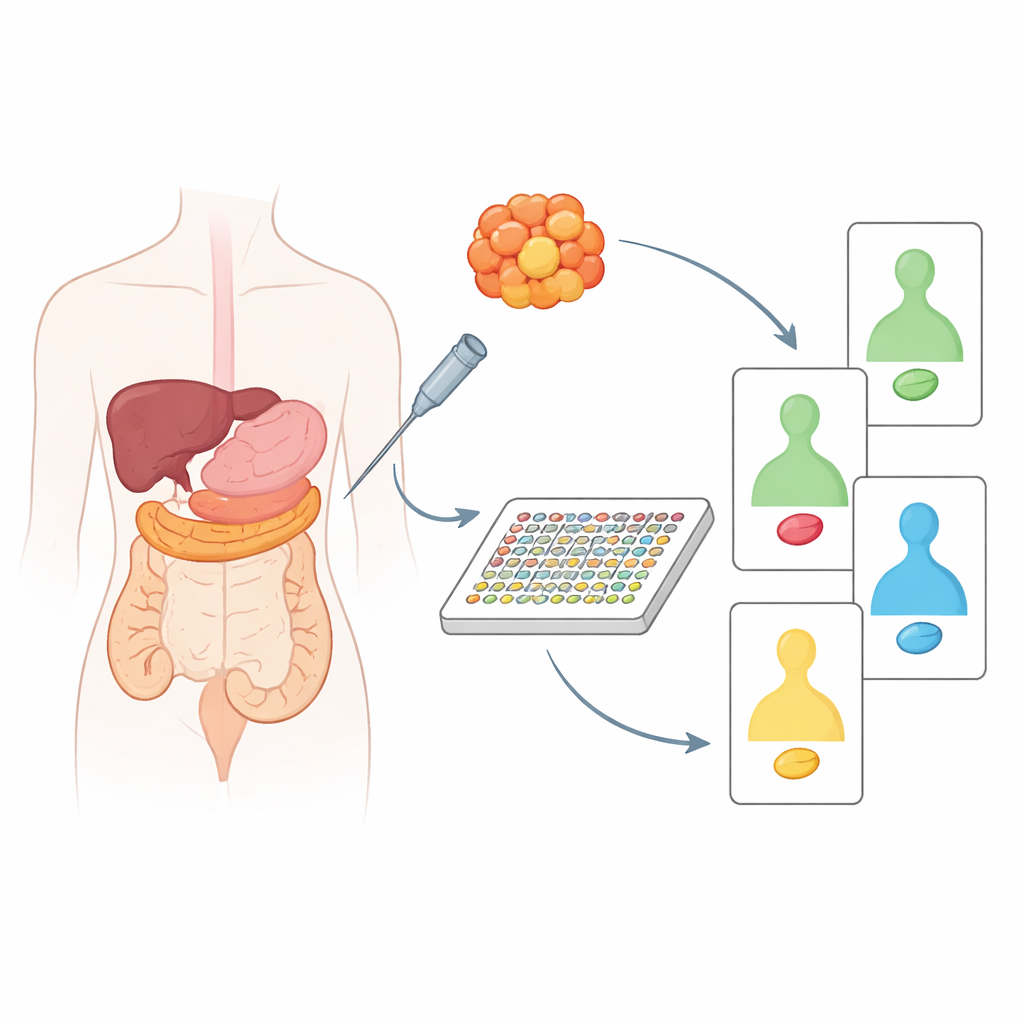
Сравнение опухолевой ткани с соседней здоровой
Команда сначала проанализировала архивные образцы тканей от 20 пациентов с раком поджелудочной железы или толстой кишки, всегда в паре с близлежащей нераковой тканью того же пациента. Сравнивая опухоль с собственными здоровыми тканями, они могли выявить белки, действительно измененные опухолью, а не отражающие нормальные отличия между органами. Это показало явные различия в поведении хорошо известных «стражей» и драйверов рака, таких как p53, Ras, PTEN и других. Например, в опухолях поджелудочной чаще наблюдались усиленные ростоподдерживающие сигналы и утрата защитных белков, тогда как в опухолях толстой кишки обнаруживался свой характерный набор нарушённых путей. Кластеризация образцов на основе этих изменений белков позволила разделить панкреатические карциномы на две биологически разные группы и выявить значимые различия среди колоректальных опухолей, связанные с возрастом пациентов и локализацией опухоли в кишечнике.
Индивидуальные «штрихкоды» tumor‑сигнальной активности
Взглянув дальше средних показателей по группам, учёные построили детализированный белковый профиль каждой опухоли. Эти профили показали, какие сигнальные пути — например вовлекающие mTOR, MAPK/Erk, Wnt или иммунные факторы — особенно активны или выключены. Многие измеренные белки являются прямыми мишенями существующих препаратов или расположены непосредственно ниже по потоку от таких мишеней, что позволило исследователям предположить, какие лекарства могут подавлять ключевые «двигатели» роста опухоли. В трёх четвертях ретроспективных случаев им удалось указать один или несколько путей, которые, вероятно, способствовали прогрессированию опухоли. Они также выделили опухоли, насыщенные маркерами иммунных клеток, указывающие на «горячие» ракые очаги, которые могут откликаться на иммунотерапию, а также необычные случаи с ярко выраженными уникальными сигнатурами.
Применение метода у реальных пациентов
Чтобы проверить его полезность у постели больного, исследователи применили DigiWest к свежим пункционным биопсиям от 14 пациентов с различными опухолями желудочно‑кишечного тракта, чьи случаи рассматривал Молекулярный опухолевый консилиум. У этих пациентов была сложная история болезни и, нередко, предшествующие лечения. Поскольку сопоставимая здоровая ткань была недоступна, уровни белков в каждой опухоли сравнивали с медианой по всей группе, чтобы определить, что считать аномально высоким или низким. Даже в таких более строгих условиях у 12 из 14 опухолей выявились чёткие, клинически значимые паттерны активности путей. В двух подробных примерах данные белкового профиля подтвердили амплификацию гена FGFR2 на уровне ДНК в колоректальной опухоли и утрату тормоза mTOR в опухоли печени, что сильно поддержало рассмотрение консилиумом препаратов‑блокаторов FGFR или mTOR. В целом выводы DigiWest согласовывались с ключевыми генетическими драйверами и указывали на лекарственные мишени в большинстве оцениваемых случаев.
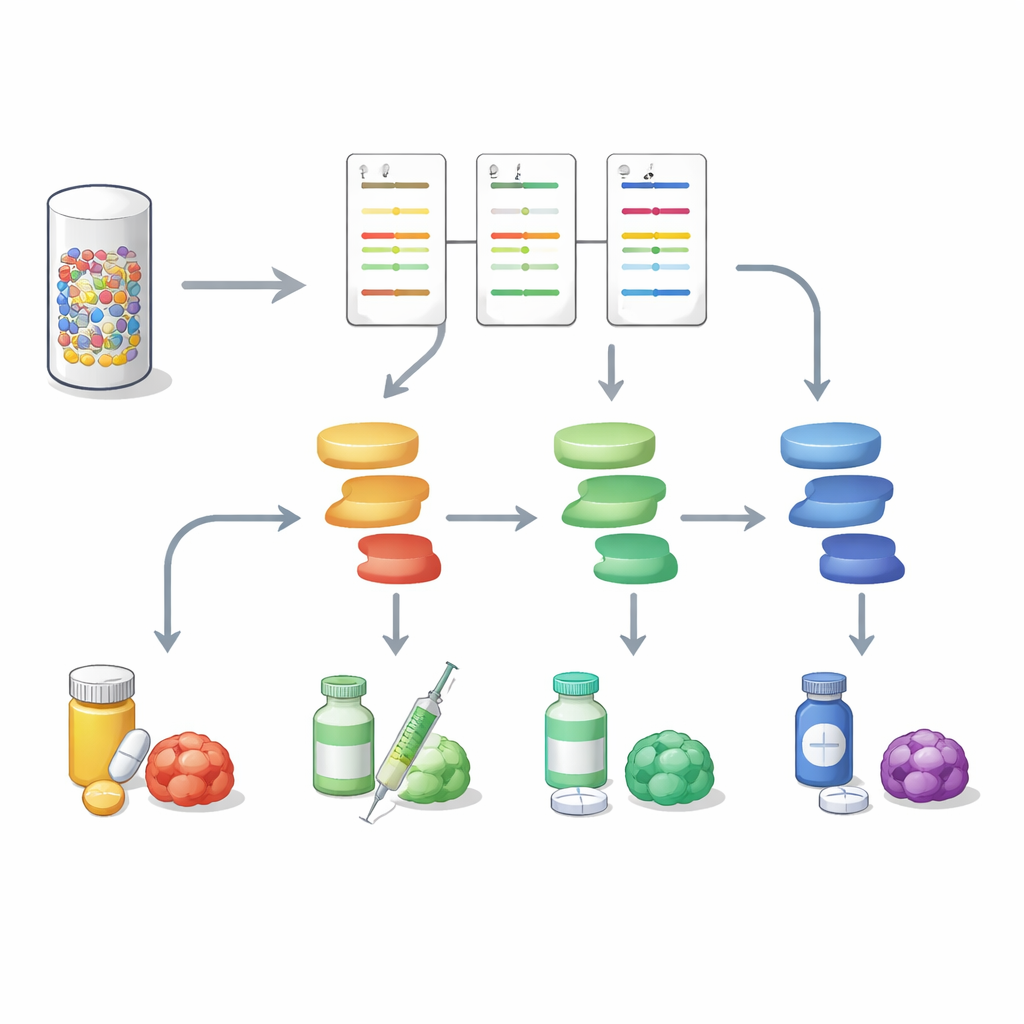
К более полным портретам опухоли
Эта работа демонстрирует, что анализ белковой сигнализации параллельно с секвенированием ДНК может дать более богатую и практически применимую картину опухолей желудочно‑кишечного тракта. Превращая крошечную биопсию в карту активности множества путей, DigiWest помогает отличить, какие молекулярные переключатели действительно включены в конкретном раке и какими препаратами их лучше всего поражать, а также может указывать на возникающие пути резистентности. Хотя требуются более крупные исследования, подход предлагает практичный способ внедрения высокоинформативного белкового профилирования в повседневную точную онкологию и приближает составление планов лечения, ориентированных на живую опухоль пациента, а не только на её генетическую карту.
Цитирование: Stahl, A., Büringer, K., Missios, P. et al. Personalized signaling pathway analysis of gastrointestinal tumors for patient stratification and drug target evaluation using clinically derived core biopsies. npj Precis. Onc. 10, 124 (2026). https://doi.org/10.1038/s41698-026-01304-5
Ключевые слова: точная онкология, раки желудочно‑кишечного тракта, протеомика, профилирование биопсий, таргетная терапия