Clear Sky Science · ru
Возможность автоматизированной контуризации на базе ИИ и оценка стабильности радиомических признаков с помощью HyperSight-CBCT для адаптивной высокоточной радиотерапии рака предстательной железы
Быстрее и умнее: планирование лечения рака
Для мужчин с раком предстательной железы современная лучевая терапия может быть исключительно точной, но такая точность требует большого труда: врачам приходится тщательно обводить предстательную железу и прилегающие органы на множестве срезов перед каждой фракцией. Это исследование ставит своевременный вопрос: может ли искусственный интеллект безопасно взять на себя большую часть этой работы по контурированию на новом высококачественном конусно‑лучевом КТ‑сканере, при этом обеспечивая надежные изображенческие показатели, которые в будущем могли бы направлять полностью персонализированное лечение?
Взгляд внутрь таза в реальном времени
Современная высокоточная радиотерапия часто опирается на плановую КТ, сделанную до лечения, и дополнительные сканы, выполняемые прямо на установке, непосредственно перед каждой дозой. Новая система HyperSight конусно‑лучевой КТ быстро получает детализированные изображения таза при более низкой дозе облучения, что делает её привлекательной для адаптивной радиотерапии, когда план корректируется под анатомию дня. В исследовании 50 мужчин с раком предстательной железы прошли как стандартную плановую КТ, так и сканирование на HyperSight. Исследователи сосредоточились на нескольких ключевых структурах таза: предстательной железе, мочевом пузыре, прямой кишке, семенных пузырьках, головке полового члена и обоих тазобедренных суставах.
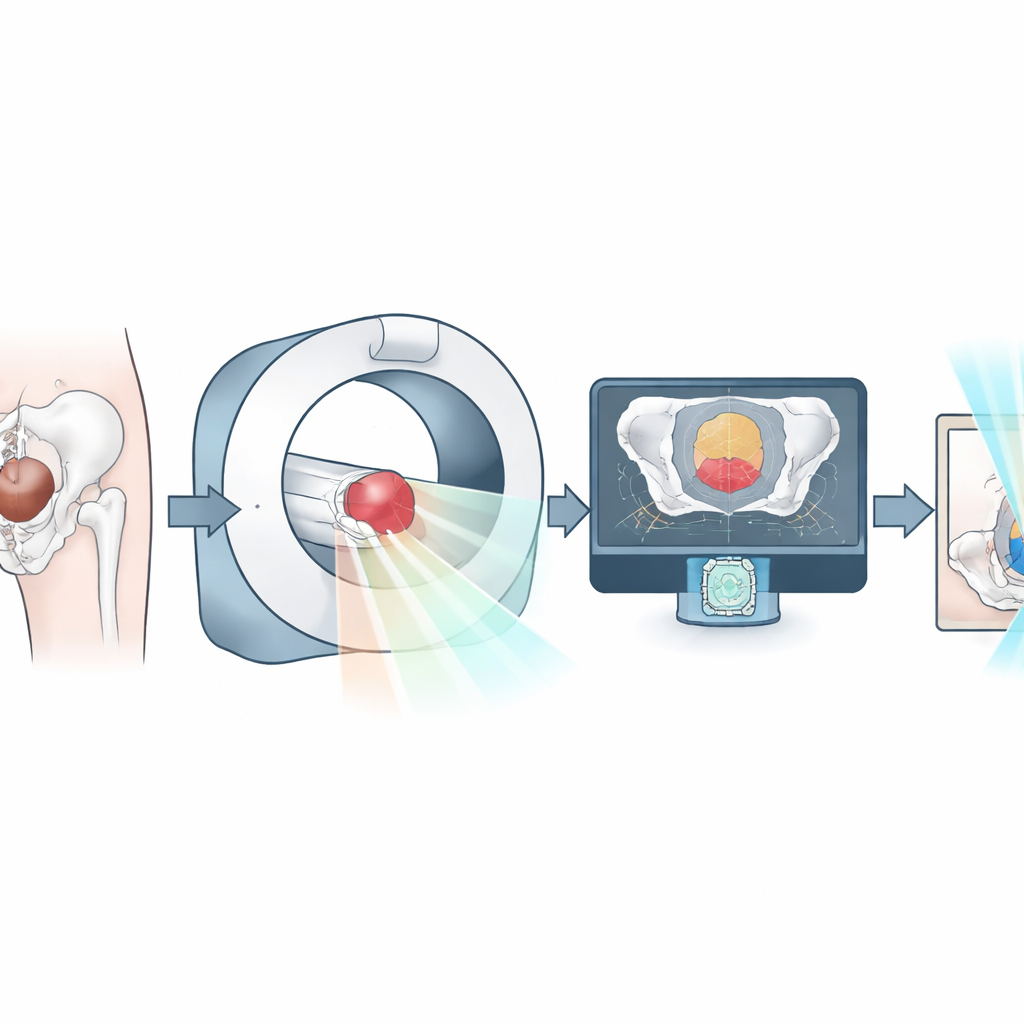
Доверить компьютеру очерчивание
Команда сравнила три способа выделения органов на изображениях. При полностью ручном подходе врачи сами проводили все контуры. В режиме только ИИ обучённый алгоритм автоматически создавал обводки. Гибридный режим начинался с контуров ИИ, которые затем проверяли и уточняли врачи. Для каждого метода исследователи измеряли, насколько близко совпадали разные контуры, как далеко расходились их границы и насколько смещались центры органов. Они также фиксировали время, требуемое на каждый подход. Для крупных хорошо видимых структур, таких как мочевой пузырь и тазовые кости, совпадение между всеми методами было очень высоким. Для предстательной железы и прямой кишки согласие было немного ниже, но всё ещё сильным. Небольшие или плохо различимые структуры, такие как семенные пузырьки и головка полового члена, оказались сложными для любого метода, включая ИИ.
От изображений к количественным отпечаткам
Помимо простого сравнения форм, в исследовании изучались радиомические признаки — сотни чисел, извлекаемых из изображений, описывающих яркость ткани, текстуру и форму. Эти признаки всё чаще рассматривают как потенциальные биомаркеры изображений, которые могут предсказывать ответ опухоли на лечение или риск побочных эффектов у пациентов. Исследователи проверяли, насколько стабильны эти числовые отпечатки при использовании контуров, полученных разными методами и разными типами сканирования. В целом радиомические признаки были высоко согласованными, особенно для крупных и высококонтрастных органов, таких как мочевой пузырь, предстательная железа, прямая кишка и тазовые кости. Текстурные признаки, описывающие закономерности интенсивностей пикселей, оказались особенно устойчивыми. Признаки, основанные на форме, а также признаки из очень маленьких органов оказывались более чувствительными к небольшим изменениям в контурах.
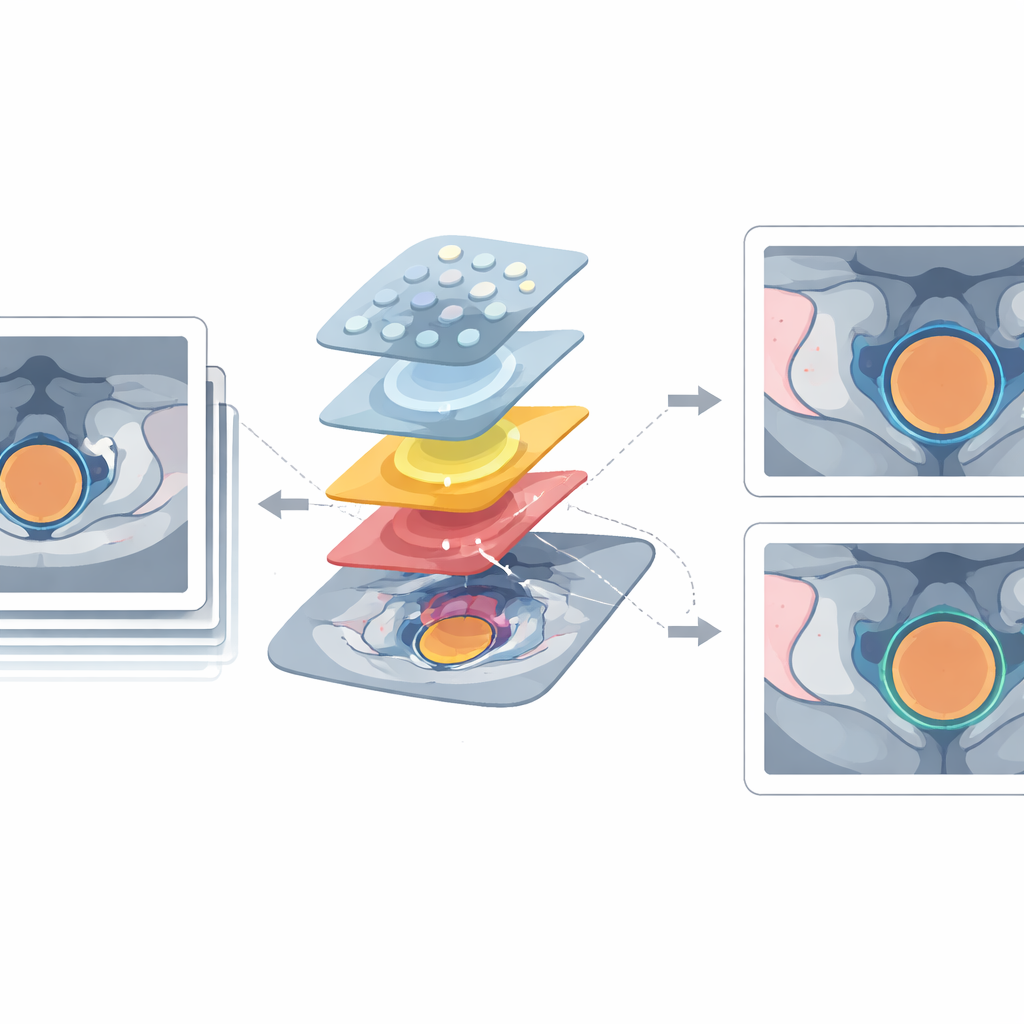
Экономия времени без потери качества
В адаптивной радиотерапии время критично: чем дольше идут контурирование и перерасчёт плана, тем выше вероятность изменения анатомии пациента между сканированием и лечением. В этом исследовании контурирование только с помощью ИИ сократило время сегментации более чем на 90% по сравнению с полностью ручной работой, тогда как гибридный подход ИИ плюс врач по-прежнему уменьшал время примерно на 60%. Важно, что эти преимущества были сходны как для плановой КТ, так и для сканов HyperSight, а межнаблюдательные тесты показали, что использование ИИ не добавляет дополнительного расхождения между разными врачами. Это указывает на то, что ИИ может значительно повысить эффективность рабочего процесса, сохраняя, а порой и улучшая согласованность.
Что это значит для пациентов
Проще говоря, исследование показывает, что интеллектуальное программное обеспечение может надёжно обводить предстательную железу и большинство соседних органов на современных изображениях конусно‑лучевой КТ, а получаемые изображенческие «отпечатки» тканей остаются достаточно стабильными, чтобы вызывать доверие в исследованиях и, потенциально, в будущих клинических решениях. Хотя небольшие, трудноразличимые структуры всё ещё выигрывают от человеческой доработки, ИИ‑управляемое и гибридное контурирование уже обеспечивают высокую точность и значительную экономию времени. Это открывает путь к по-настоящему адаптивным сеансам радиотерапии, когда лечение можно быстро подстраивать под анатомию и, возможно, со временем по радиомическим маркерам, сигнализирующим о реакции рака каждого пациента в реальном времени.
Цитирование: Schmidt, R., Bajerski, D., Bicu, A.S. et al. Feasibility of automated AI-based contouring and stable radiomic feature assessment by HyperSight-CBCT Imaging for adaptive high-precision radiotherapy of prostate cancer. Sci Rep 16, 12191 (2026). https://doi.org/10.1038/s41598-026-46359-3
Ключевые слова: радиотерапия рака предстательной железы, автоконтурирование ИИ, конусно-лучевая КТ, радиомика, адаптивная лучевая терапия