Clear Sky Science · ru
Модифицированный RGD альгинат повышает жизнеспособность, перенастройку метаболизма и профиль секреции цитокинов у инкапсулированных мезенхимальных стромальных клеток
Почему важны крошечные капсулы для клеток
Врачи стремятся использовать живые клетки в качестве лекарств для подавления воспаления и восстановления повреждённых органов, но после введения в организм эти клетки часто быстро исчезают. В этом исследовании рассмотрен простой способ поместить полезные клетки, похожие на стволовые, в крошечные гелевые шарики, чтобы они жили дольше, оставались активными и выделяли восстанавливающие сигналы, что делает будущие клеточные терапии более надёжными и удобными в применении.
Помещение «помощников» в мягкие оболочки
Учёные работали с мезенхимальными стромальными клетками — универсальным типом клеток, полученным здесь из донорских пуповинных канатиков. Эти клетки могут смягчать иммунные реакции и поддерживать восстановление тканей, что делает их перспективными для лечения серьёзных состояний, таких как острое печёночное повреждение. Вместо выращивания клеток на плоских пластиковых чашках команда инкапсулировала их в микросферы из альгината — геля, получаемого из морских водорослей и уже используемого в медицине. Сравнивали две версии материала: чистый высокопурифицированный альгинат и модифицированный вариант с короткими RGD-пептидами, которые действуют как небольшие «крючки», помогающие клеткам прикрепляться к окружению.
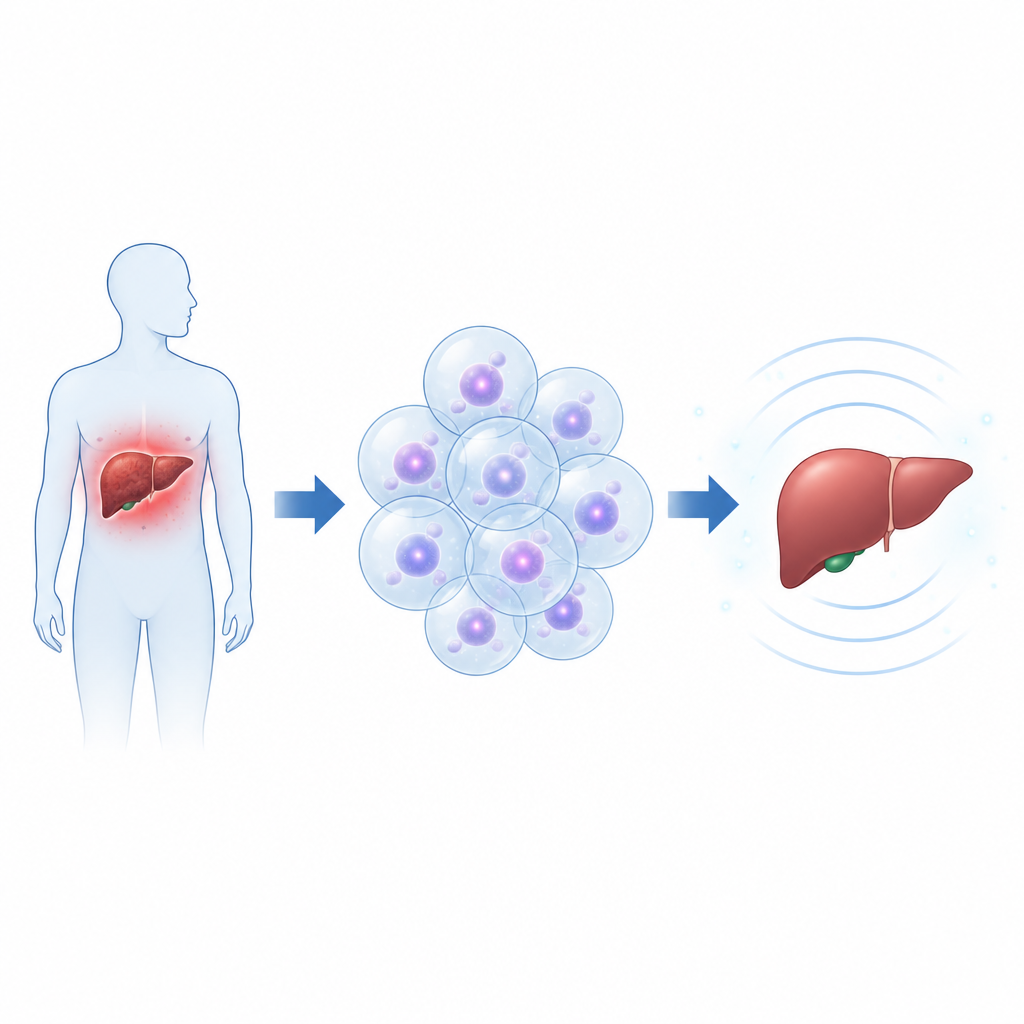
Жизнь внутри тесного микрошарика
После разморозки из запасов пуповинные клетки смешивали с растворами альгината и формировали в равномерные шарики диаметром около половины миллиметра — размер, выбранный с учётом прочности и способности кислорода и питательных веществ диффундировать внутрь. Под микроскопом клетки в RGD-покрытых шариках демонстрировали более высокую выживаемость и более развитый внутренний цитоскелет по сравнению с клетками в обычных шариках, что указывало на то, что они ощущают и захватывают модифицированный гель. Несмотря на это, клетки не образовывали прямых контактов друг с другом, а их форма сильно отличалась от распластанного вида в традиционной плоской культуре, что отражает более ограниченную трёхмерную среду.
Переключение метаболизма в кармане с низким содержанием кислорода
Живые клетки постоянно регулируют, как они производят энергию, переключаясь между путями в зависимости от условий. Детальные измерения потребления кислорода показали, что инкапсуляция сразу снижает скорость «дыхания» клеток по сравнению со стандартной ростовой культурой на блюдце, даже при добавлении веществ, стимулирующих максимальную работу митохондрий. В течение нескольких дней клетки в RGD-шариках последовательно поддерживали более высокий базальный и максимальный уровень дыхания, чем в обычных шариках, что указывает на небольшое энергетическое преимущество. Одновременно гены, связанные с ростом митохондрий, особенно PGC1A, были сильно активированы в инкапсулированных клетках, тогда как общее производство лактата и связанных с ним побочных продуктов снизилось, указывая на замедление и перераспределение метаболизма. Хотя тесты с красителями не выявили выраженной гипоксии внутри шариков, клетки включили программу ответа на гипоксию, обычно ассоциированную с их естественными низко-кислородными ниши в организме.
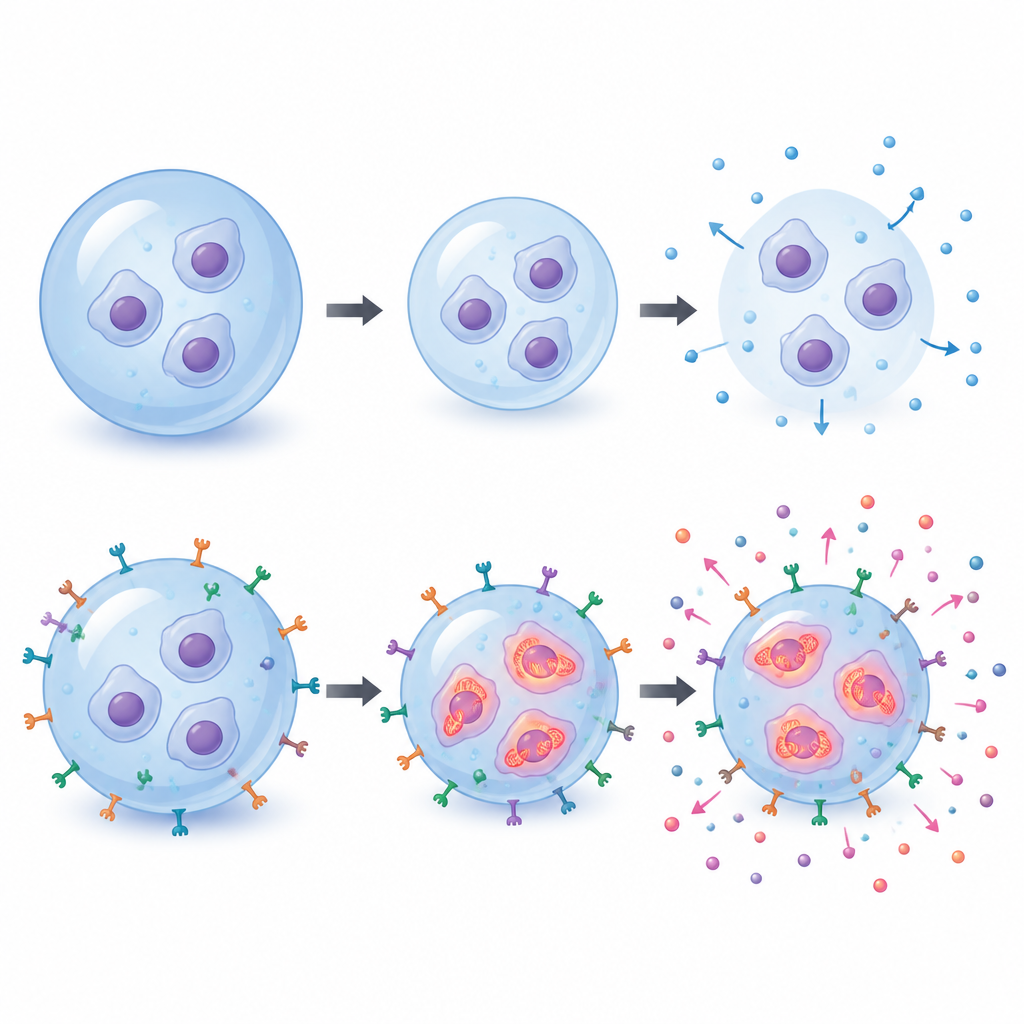
Формирование секреторных сообщений клеток
Мезенхимальные стромальные клетки влияют на заживление главным образом за счёт выделения коктейлей сигнальных белков, а не прямой замены повреждённых тканей. Команда измеряла несколько таких факторов в окружающей среде культуры вокруг шариков. Вскоре после инкапсуляции клетки секретировали значительно большие количества сосудистого эндотелиального ростового фактора (VEGF), поддерживающего рост сосудов, и иммунного посредника IL-6 по сравнению с клетками, выращенными на пластике. Эти всплески ослабевали в течение нескольких дней, но ранние уровни IL-6 были несколько выше в RGD-шариках по сравнению с обычными. Как правило провоспалительный молекула TNF-альфа оставалась низкой в целом, хотя на более поздних временных точках она была слегка повышена в RGD-шариках, в то время как противовоспалительный фактор IL-10 почти не менялся. Поверхностный маркер, связанный с «стволовостью», CD90, снижался у инкапсулированных клеток, что указывает на то, что жизнь в свободно плавающем геле меняет аспекты их идентичности, даже если основные поддерживающие функции сохраняются.
Что это значит для будущих лечений
В совокупности полученные данные показывают, что простое помещение пуповинных стромальных клеток в тщательно подобранные альгинатные шарики заметно изменяет их существование, дыхание и коммуникацию. Модифицированный RGD-гель даёт небольшие, но устойчивые преимущества для выживаемости клеток, энергетического обмена и ранней секреции сигналов по сравнению с обычным материалом, при этом используются высокопурифицированные, клинически одобренные компоненты и замороженные запасы клеток, похожие на те, что применяются в клинике. Для пациентов такая микроинкапсуляция в будущем может превратиться в более долговечные клеточные терапии, поставляемые в виде готовых к использованию крошечных капсул, которые могут оставаться в теле как защищённые мини‑фабрики, незаметно выделяющие целевые сигналы восстановления.
Цитирование: Güven, K., Dhawan, A. & Filippi, C. RGD-modified alginate enhances viability, metabolic reprogramming, and cytokine secretion profiles in encapsulated mesenchymal stromal cells. Sci Rep 16, 14927 (2026). https://doi.org/10.1038/s41598-026-42864-7
Ключевые слова: мезенхимальные стромальные клетки, альгинатные микрошарики, инкапсуляция клеток, клеточная терапия, RGD биоматериалы