Clear Sky Science · ru
Импедансное считывание отдельных клеток на интегральной схеме для быстрого диагноза опухоли
Почему важна более быстрая проверка опухолей
Когда хирурги удаляют подозрительное образование, им часто приходится принимать решение на месте — сколько ткани вырезать. Если вырезать слишком мало, опасные раковые клетки могут остаться. Если убрать слишком много, пациент может лишиться здоровой ткани органа, которая могла бы понадобиться. Современные лабораторные тесты медленные и сложные, поэтому врачи обычно не могут получить однозначный ответ, пока пациент все еще в операционной. В этом исследовании представлен новый чиповый тест, который считывает крошечные электрические сигналы от отдельных клеток, чтобы быстро оценить, скорее всего опухоль доброкачественная или злокачественная во время операции.
Ограничения нынешних тестов на опухоли
В настоящий момент врачи полагаются на сканирование, биомаркеры в крови и микроскопическое изучение ткани для постановки диагноза рака. Методы визуализации, такие как УЗИ, КТ, МРТ и ПЭТ, могут пропускать очень маленькие опухоли, а уровни биомаркеров в крови часто повышаются лишь на поздних стадиях болезни. Наиболее надежный метод предполагает фиксацию, разрезание и окрашивание ткани, что обычно занимает около недели. Более быстрый вариант — замороженные срезы — дает предварительный ответ примерно за час, но технически сложен, менее точен и требует опытных патологов и тщательной подготовки образцов. Новые оптические и масс-спектрометрические инструменты могут ускорить процесс, но они требуют дорогостоящего оборудования и сложных рабочих процессов, что ограничивает их широкое применение.
Считывание клеток по их электрическому отпечатку
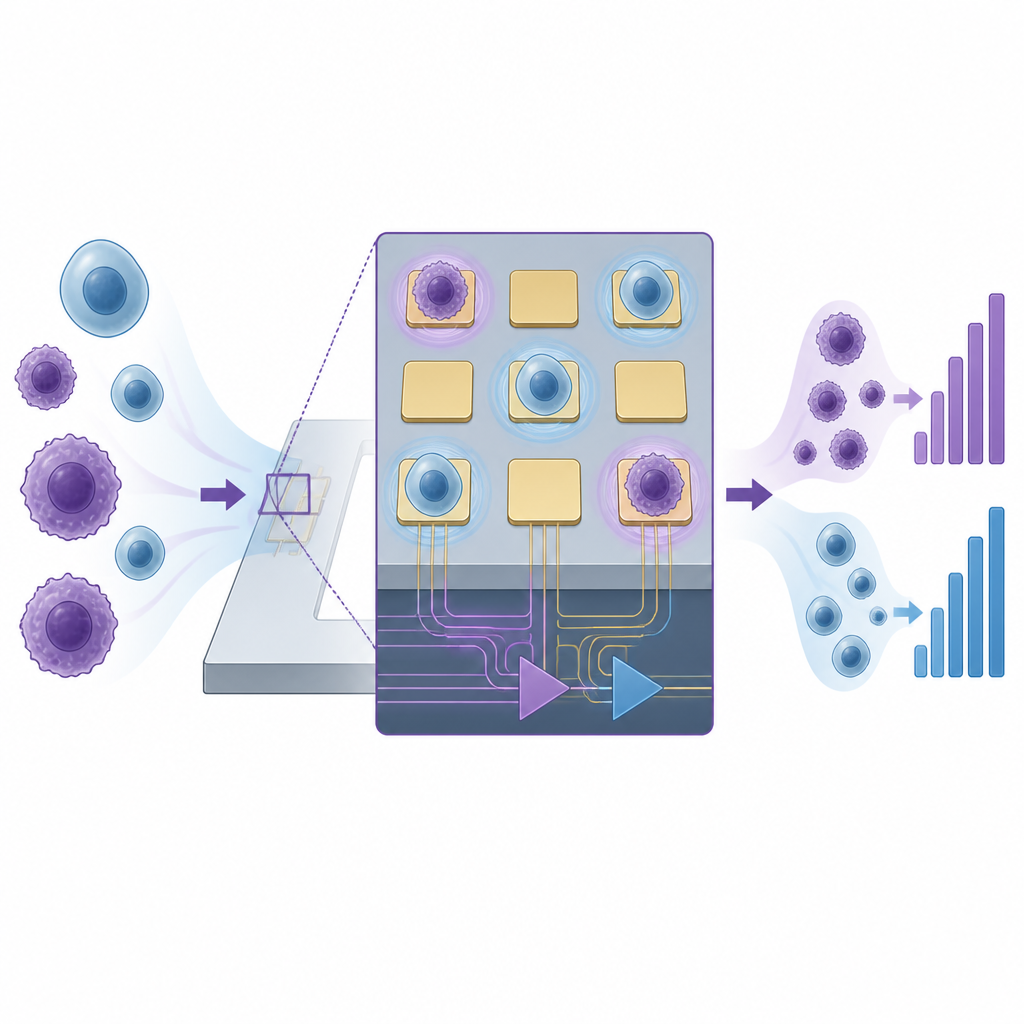
Авторы опираются на метод, известный как измерение электрического импеданса, который определяет, насколько легко электрический сигнал проходит через клетки, лежащие на крошечных электродах. Раковые клетки часто отличаются от нормальных по размеру, заряду мембраны и адгезии к поверхностям. Эти различия меняют электрический импеданс на контакте клетки и электрода. Традиционные системы требуют больших количеств клеток и длинных проводов к внешним приборам, что вносит шум и размывает сигналы от отдельных клеток. Чтобы решить эту проблему, исследователи разместили чувствительные электроды и электронику считывания прямо на одном полупроводниковом чипе, что позволяет фиксировать очень слабые сигналы от отдельных клеток с высокой точностью.
Низкозатратная фабрика чипов для сенсоров клеток
Чтобы сделать новый тест практичным, группе также нужно было массово и недорого изготовлять эти крошечные сенсорные чипы. Они использовали метод «полимер-имбэддед силикон фэн-аут» для размещения множества интегральных схем в вытравленных пазах на кремниевой пластине, затем покрывали и формировали их вместе. На каждом чипе сформировали очень маленькие платиновые электроды, едва достаточные, чтобы удержать отдельные клетки. На стандартной четырехдюймовой пластине можно обработать более двух тысяч чипов за один цикл. Такой подход удерживает стоимость постобработки ниже одного доллара за чип, что открывает путь к одноразовым сенсорным матрицам, которые можно использовать прямо в клинике без необходимости тщательной очистки или повторного использования.
От образца ткани до показателя риска рака
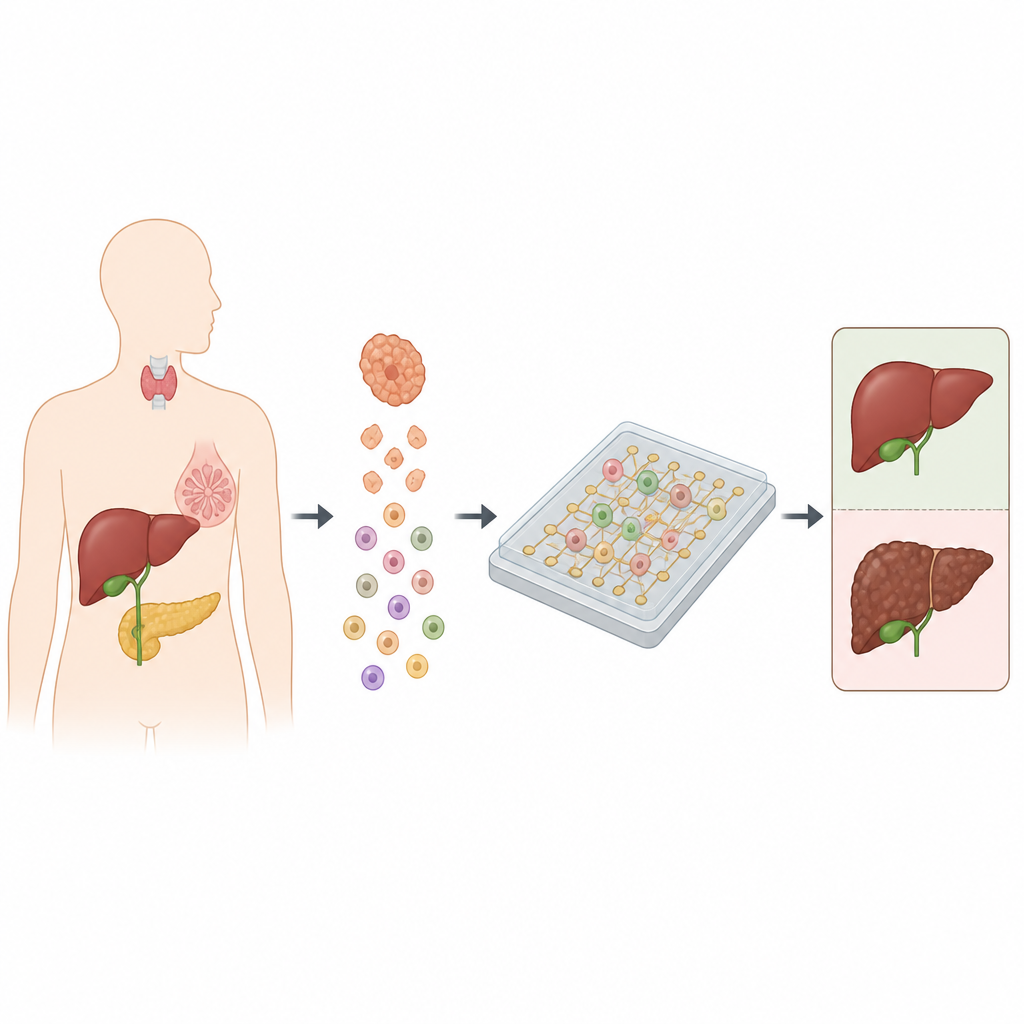
В рабочем режиме небольшой кусочек опухоли сначала диссоциируют до суспензии отдельных клеток. Эти клетки затем загружают на чип, где отдельные клетки случайным образом оседают на микроэлектродах. Система посылает мягкий переменный сигнал через электроды и регистрирует импеданс для каждой клетки. Раковые клетки демонстрируют устойчиво более высокий импеданс по сравнению с незлокачественными клетками, включая нормальные клетки ткани и иммунные клетки. Вместо оценки каждой клетки по отдельности метод анализирует общее распределение значений импеданса и подсчитывает, сколько клеток превышают порог, установленный на основе нормальной ткани. Доля клеток с высоким импедансом затем переводится в простой уровень риска: низкий, средний или высокий шанс того, что опухоль злокачественная.
Тестирование реальных опухолей в разных органах
Исследователи проверили платформу на культурах клеточных линий, чтобы подтвердить, что она может отделить клетки рака желудка от нормальных клеток желудка, достигнув примерно 80-процентной точности на уровне отдельных клеток. Затем они перешли к клиническим образцам от пациентов с опухолями щитовидной железы, печени, желчных протоков, груди, желчного пузыря и поджелудочной железы. Для каждого пациента клетки из опухоли и из рядом расположенной нормальной ткани измерялись на чипе. Опухоли, в которых более 40 процентов клеток показали аномальный импеданс, классифицировались как высокий риск и впоследствии подтверждались как злокачественные стандартной патологией. Опухоли с очень небольшим числом аномальных клеток оценивались как низкий риск и соответствовали доброкачественным результатам. Для рака печени доля клеток с высоким импедансом хорошо коррелировала с долей клеток, несущих известный маркер рака печени, измеренным отдельно методом проточной цитометрии, что дополнительно подтверждает надежность метода.
Что это означает для пациентов и хирургов
Исследование показывает, что маленький недорогой чип может быстро считывать электрическое поведение тысяч отдельных клеток, чтобы оценить, скорее всего опухоль доброкачественная или злокачественная. Весь процесс — от взятия ткани до выдачи результата риска — может быть завершен примерно за двадцать минут, что достаточно быстро, чтобы направлять решения, принимаемые пока пациент находится в операционной. Хотя необходима дальнейшая работа по улучшению позиционирования клеток, снижению затрат при масштабном производстве и повышению стабильности работы с живыми клетками на чипах, этот подход указывает на создание компактных инструментов, которые могут перенести сложный анализ опухолей непосредственно в операционные и помочь адаптировать лечение для каждого пациента в реальном времени.
Цитирование: Hui, W., Chen, L., Andaluz, S. et al. Single-cell impedance sensing on integrated circuit chip for fast tumor diagnosis. Microsyst Nanoeng 12, 173 (2026). https://doi.org/10.1038/s41378-026-01229-w
Ключевые слова: диагностика опухолей, анализ отдельных клеток, импедансное датирование, интегральная схема, внутриоперационное тестирование