Clear Sky Science · ru
Выявление сайтов ацетилирования Dnmt3L, которые регулируют стабильность белка и потенциал дифференцировки в эмбриональных стволовых клетках
Почему окружение стволовых клеток имеет значение
Эмбриональные стволовые клетки ценятся за то, что могут превратиться практически в любую клетку организма — от сердечной мышцы до нейронов. Однако в лаборатории их «идентификационные метки» — химические пометки на ДНК, которые направляют развитие — со временем могут дрейфовать, особенно при определённых условиях культивирования. В этом исследовании показано, как один небольшой белковый переключатель, молекула Dnmt3L, считывает условия культивирования и помогает определить, сохраняют ли стволовые клетки способность к развитию или её теряют. Понимание этого переключателя может сделать будущие терапии на основе стволовых клеток более безопасными и предсказуемыми.
Клеточный регулятор маркировки ДНК
Внутри каждой стволовой клетки ДНК покрыта небольшими химическими метками, которые помогают включать или выключать гены без изменения генетического кода. Одной из основных таких меток является метилирование ДНК, и Dnmt3L — вспомогательный белок, работающий с ферментами, которые метилируют ДНК. Исследователи выращивали эмбриональные стволовые клетки мыши в нескольких распространённых условиях культивирования, включая популярную схему «2i-LIF», используемую для поддержания клеток в очень раннем, наивном состоянии. Они обнаружили, что в отличие от родственных ферментов, которые оставались на низком уровне, уровни Dnmt3L колебались очень динамично и сильно зависели от того, как долго клетки содержались в 2i-LIF и переводились ли обратно в среду на сывороточной основе. Это выделило Dnmt3L как чувствительный индикатор того, как окружение перестраивает эпигенетический ландшафт клетки.
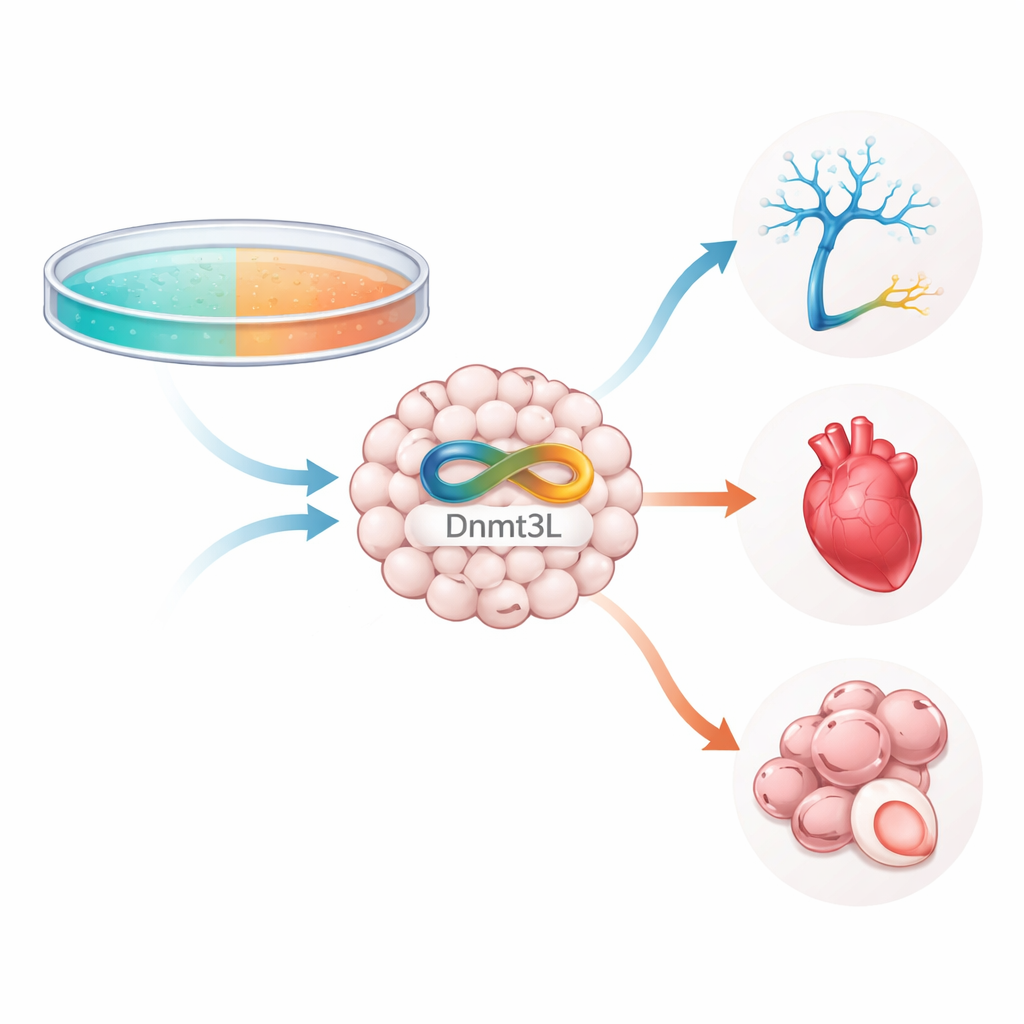
Химическая правка, защищающая хрупкий белок
Сам Dnmt3L модифицируется малыми химическими группами после синтеза белка. С помощью масс-спектрометрии команда картировала эти модификации и выявила два ключевых участка — определённые аминокислоты, обозначенные как K238 и K412, куда могут присоединяться ацетильные группы. Когда эти сайты изменяли так, чтобы они больше не могли быть ацетилированы, уровни белка Dnmt3L резко падали, хотя уровни его РНК не менялись, что указывает на проблему со стабильностью, а не с продукцией. Дальнейшие эксперименты показали, что без ацетилирования на этих участках Dnmt3L сильнее помечался убиквитином — сигналом на отправку белков в клеточную систему утилизации. Блокирование партнёрного фермента G9a или снижение другого фактора, Prdm14, уменьшало это разрушение, что говорит о том, что ацетилирование защищает Dnmt3L от маркировки на уничтожение.
От меток на ДНК к судьбе клетки
Стабилизация Dnmt3L имела заметные последствия для того, как стволовые клетки используют свои гены. Когда присутствовал дополнительный, способный к ацетилированию Dnmt3L, ключевые гены, поддерживающие наивное состояние стволовых клеток и раннее формирование герминативных клеток, выключались, при этом в регионах их регуляции увеличивалось метилирование ДНК. То же самое наблюдалось для генов, связанных с развитием нервной и сердечной тканей. Напротив, мутантные формы Dnmt3L, неспособные к ацетилированию, были менее представлены на ДНК и не могли обеспечить эти изменения метилирования, оставляя такие гены более активными. Несмотря на эти прицельные сдвиги, общее метилирование по всему геному менялось слабо, что указывает на то, что Dnmt3L действует как точный инструмент, перестраивая метки в конкретных, важных для развития участках, а не глобально.
Влияние на развивающиеся ткани
Чтобы понять, как эти молекулярные изменения сказываются на развитии, исследователи позволили стволовым клеткам формировать эмбриоидные тела — трёхмерные скопления, имитирующие ранние эмбрионы — и затем дифференцировали их в разные линии. Клетки с высоким уровнем Dnmt3L, способного к ацетилированию, формировали меньшие, плохо организованные структуры и демонстрировали задержку активации генетических программ для герминативных, нервных и кардиальных клеток. Они давали меньше герминативноподобных клеток, испытывали трудности с образованием зрелых нейронов и формировали сокращающиеся сердцеподобные скопления позже и менее устойчиво. При повторении тех же экспериментов на мышах тератомы, происходящие от таких клеток, содержали меньше нервных, сердечных и герминативных тканей, а их профили экспрессии генов отражали дефекты, наблюдавшиеся in vitro. Критично, эти проблемы в значительной мере исправлялись, когда Dnmt3L нес мутации, препятствующие стабилизирующему ацетилированию в K238 и K412.
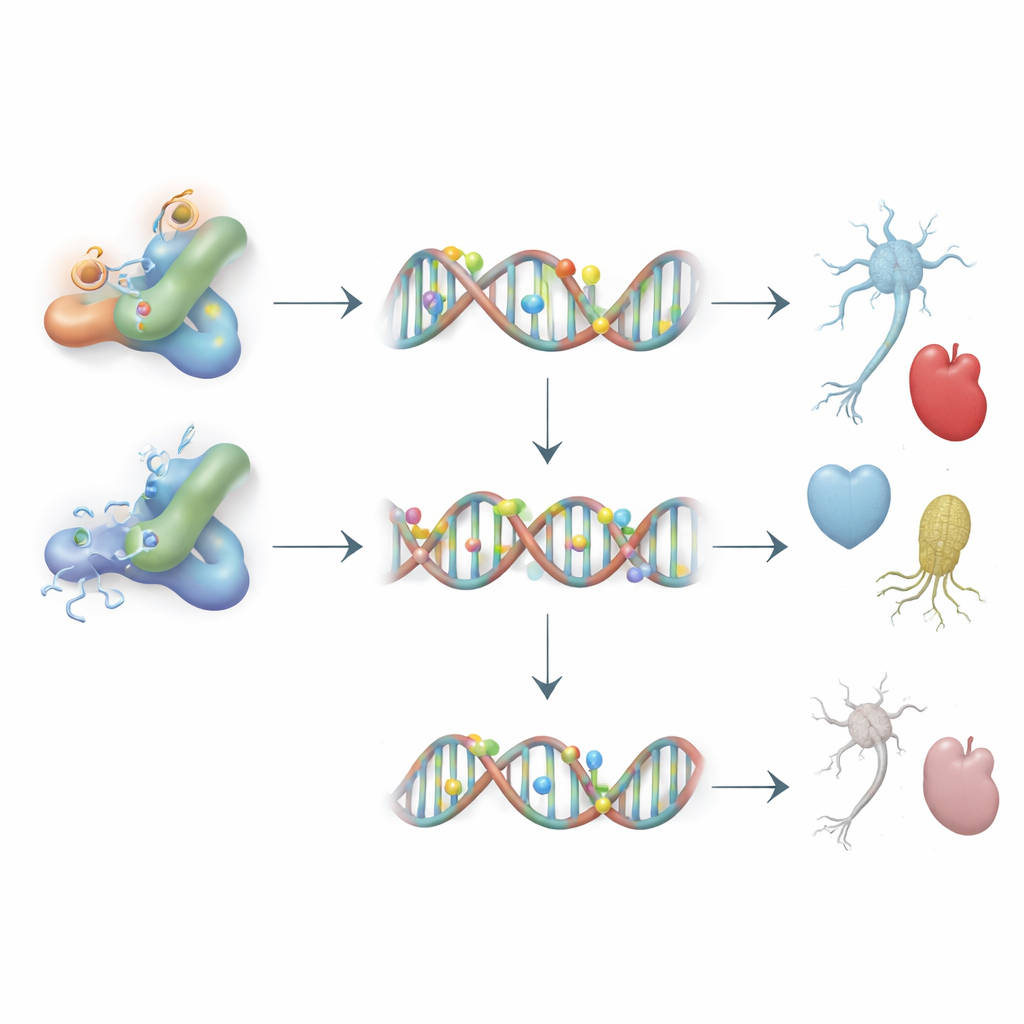
Последствия для безопасной регенеративной медицины
Проще говоря, эта работа показывает, что Dnmt3L ведёт себя как чувствительный к среде регулятор, который может либо помогать сохранять, либо разрушать развивающиеся опции эмбриональных стволовых клеток в зависимости от своей химической настройки. Ацетилирование в двух специфических сайтах делает Dnmt3L более стабильным, позволяя ему перестраивать метки ДНК у ключевых генов и сдвигать склонность стволовых клеток к образованию герминативных клеток, нейронов или клеток сердца. Рассматривая Dnmt3L одновременно как сенсор и точку управления, учёные могут разработать условия культивирования, которые лучше сохраняют «эпигенетическое здоровье» стволовых клеток, повышая шансы на точное моделирование болезней и безопасные клеточные терапии в будущем.
Цитирование: Nam, Y.J., Kwon, H., Im, H.J. et al. Uncovering the acetylation sites of Dnmt3L that regulate protein stability and differentiation potency in embryonic stem cells. Exp Mol Med 58, 709–724 (2026). https://doi.org/10.1038/s12276-026-01655-w
Ключевые слова: эмбриональные стволовые клетки, метилирование ДНК, эпигенетическая регуляция, Dnmt3L, клеточная дифференцировка